Clear Sky Science · pt
Uma Rede Neural Informada por Metabolismo Identifica Vias que Influenciam a Potência e a Toxicidade de Combinações Antimicrobianas
Por que isso importa para a saúde cotidiana
À medida que mais infecções deixam de responder aos nossos antibióticos de primeira linha, os médicos recorrem cada vez mais a combinações de fármacos. Mas misturar medicamentos pode ser uma faca de dois gumes: o par certo pode eliminar bactérias persistentes, enquanto a combinação errada pode prejudicar órgãos como rins e fígado. Este estudo apresenta uma nova abordagem computacional, chamada CALMA, projetada para ajudar cientistas e clínicos a encontrar combinações de medicamentos que sejam ao mesmo tempo eficazes contra microrganismos e mais gentis para os pacientes.
Combater germes sem depender de tentativa e erro
Tradicionalmente, descobrir boas combinações de antibióticos significava testar um grande número de pares ou trios de medicamentos no laboratório e em pacientes. O número de misturas possíveis cresce de forma explosiva a cada droga adicional, tornando testes experimentais completos pouco realistas. Além disso, a maioria das ferramentas existentes foca apenas em quão fortemente as combinações matam bactérias, ignorando como elas podem danificar tecidos humanos. Os autores argumentam que, para desenhar tratamentos melhores, devemos considerar os dois lados da equação: potência contra patógenos e segurança para as pessoas.
Um modelo inteligente que entende a química celular
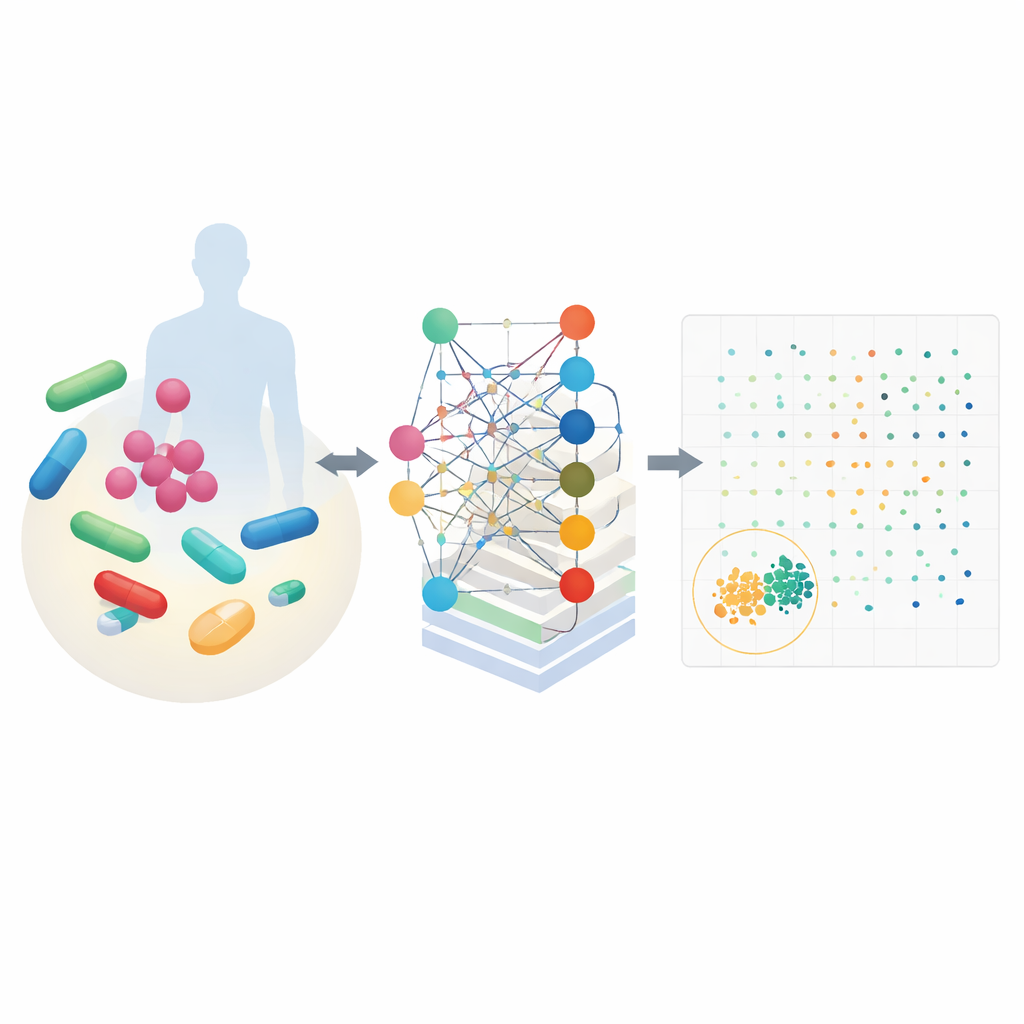
CALMA combina duas ideias poderosas. Primeiro, usa mapas detalhados do metabolismo celular que descrevem como organismos convertem nutrientes em energia e blocos de construção. Esses mapas, construídos para bactérias como Escherichia coli e o germe da tuberculose, simulam como milhares de reações químicas mudam quando um fármaco está presente. Segundo, o CALMA alimenta essas simulações em uma rede neural artificial cuja estrutura espelha vias metabólicas. Agrupando informações de acordo com rotas biológicas conhecidas — como produção de energia ou reciclagem de nucleotídeos — o modelo aprende padrões que ligam vias específicas tanto à eficácia na eliminação bacteriana quanto a efeitos colaterais nocivos em células humanas.
Mapeando a paisagem das misturas de medicamentos
Usando dados de experimentos anteriores e grandes bases de dados de segurança, os pesquisadores treinaram o CALMA para atribuir a cada combinação de medicamentos duas pontuações: uma para quão fortemente ataca bactérias e outra para a probabilidade de ser tóxica em humanos. Traçar essas pontuações cria uma paisagem onde os melhores candidatos ficam no canto inferior esquerdo — fortes contra microrganismos e suaves nas células humanas. Ao aplicar o CALMA a 35 medicamentos clinicamente relevantes, a ferramenta reduziu quase 600 pares possíveis a um pequeno conjunto de opções promissoras, diminuindo o espaço de busca experimental em cerca de 97%. Entre as principais sugestões estavam combinações envolvendo antibióticos comuns como azitromicina, vancomicina, isoniazida e trimetoprim.
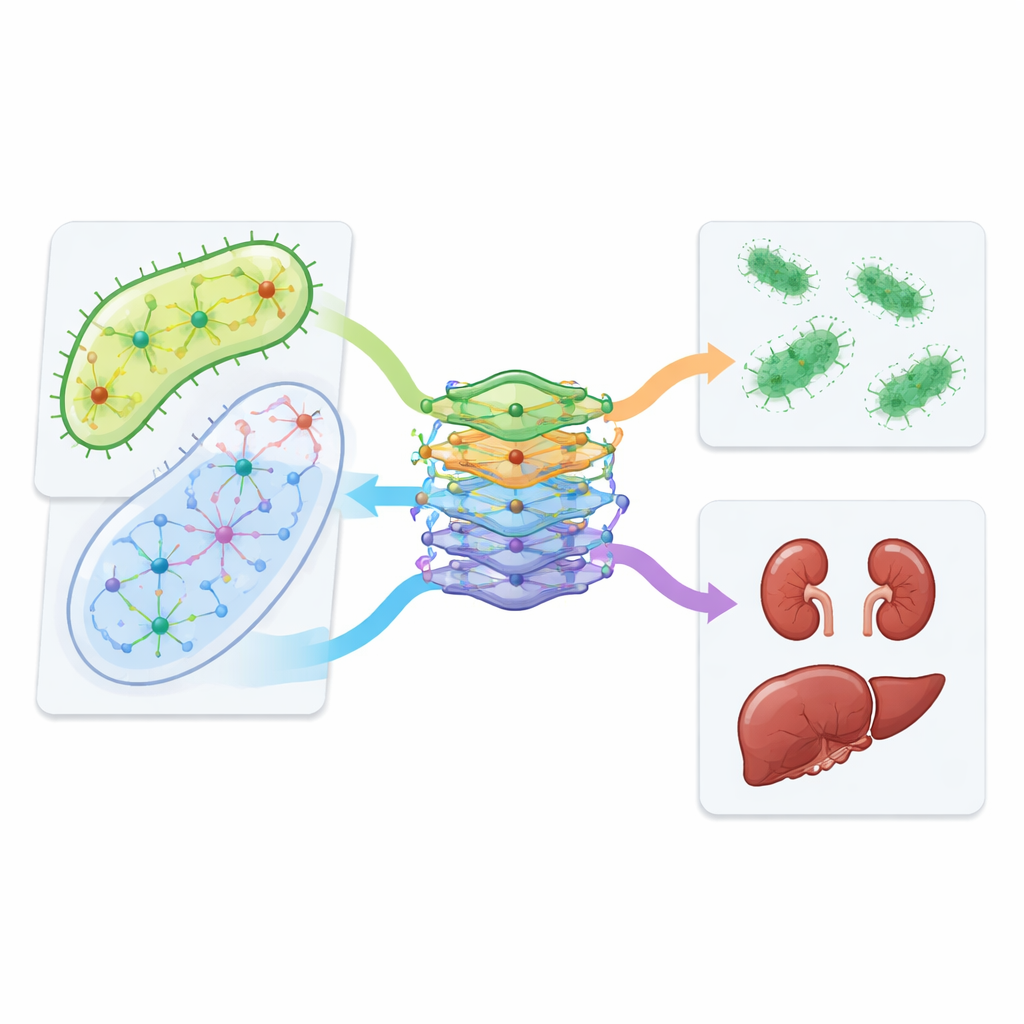
Das previsões computacionais aos testes em laboratório e em pacientes reais
A equipe foi além das simulações para testar várias combinações previstas em linhas celulares de rim e fígado. Eles descobriram que certos pares, incluindo azitromicina com vancomicina e isoniazida com trimetoprim, foram menos tóxicos para células humanas do que os medicamentos isolados, mantendo ainda atividade contra E. coli. O desenho do CALMA também permitiu aos pesquisadores investigar quais rotas metabólicas impulsionam a toxicidade. Uma via que recicla blocos de construção do DNA, conhecida como salvamento de nucleotídeos, emergiu como um ator-chave: modulá-la em experimentos celulares alterou o grau de dano de algumas combinações. Finalmente, os autores analisaram registros de saúde de centenas de milhares de pacientes e observaram que pessoas que receberam azitromicina junto com vancomicina tiveram menos problemas renais documentados do que pacientes semelhantes em vancomicina isolada, ecoando os achados laboratoriais.
O que isso significa para tratamentos futuros
Para um não especialista, o CALMA pode ser visto como um filtro inteligente que entende o suficiente de biologia para sugerir quais misturas de medicamentos valem a pena testar primeiro. Em vez de misturar antibióticos às cegas e torcer pelo melhor, os pesquisadores podem se concentrar em combinações que os modelos preveem que atinjam pontos fracos bacterianos enquanto preservam vias humanas vulneráveis. Embora o método dependa dos dados disponíveis e não seja perfeito, oferece uma rota mais racional para projetar terapias combinadas. Com o tempo, ferramentas como o CALMA podem ajudar médicos a tratar infecções resistentes com mais segurança, reduzir tentativa e erro no desenvolvimento de medicamentos e até ser adaptadas para outras doenças em que combinações de tratamentos e efeitos colaterais são preocupações importantes.
Citação: Arora, H.S., Lev, K., Robida, A. et al. A Metabolism-Informed Neural Network Identifies Pathways Influencing the Potency and Toxicity of Antimicrobial Combinations. npj Drug Discov. 3, 11 (2026). https://doi.org/10.1038/s44386-026-00042-9
Palavras-chave: combinações de antibióticos, toxicidade de medicamentos, redes neurais artificiais, metabolismo, resistência antimicrobiana