Clear Sky Science · pt
Geração 3D molecular com restrição por interações usando um modelo de difusão permite modelagem farmacófora baseada em estrutura para desenho de fármacos
Por que é tão difícil projetar medicamentos melhores
A descoberta moderna de fármacos geralmente depende de convencer uma pequena molécula a encaixar-se em uma proteína como uma chave em uma fechadura. Mas a chave precisa fazer mais do que caber: ela deve formar o conjunto certo de pequenas atrações — como fracas forças elétricas e regiões que evitam a água — para que o fármaco permaneça ligado com afinidade e especificidade. O universo químico é astronomicamente grande, muito além do que os bancos de dados atuais contêm, então os pesquisadores buscam maneiras mais inteligentes de criar novas chaves do zero preservando esses padrões cruciais de contato.
Ensinar a um computador o que realmente importa
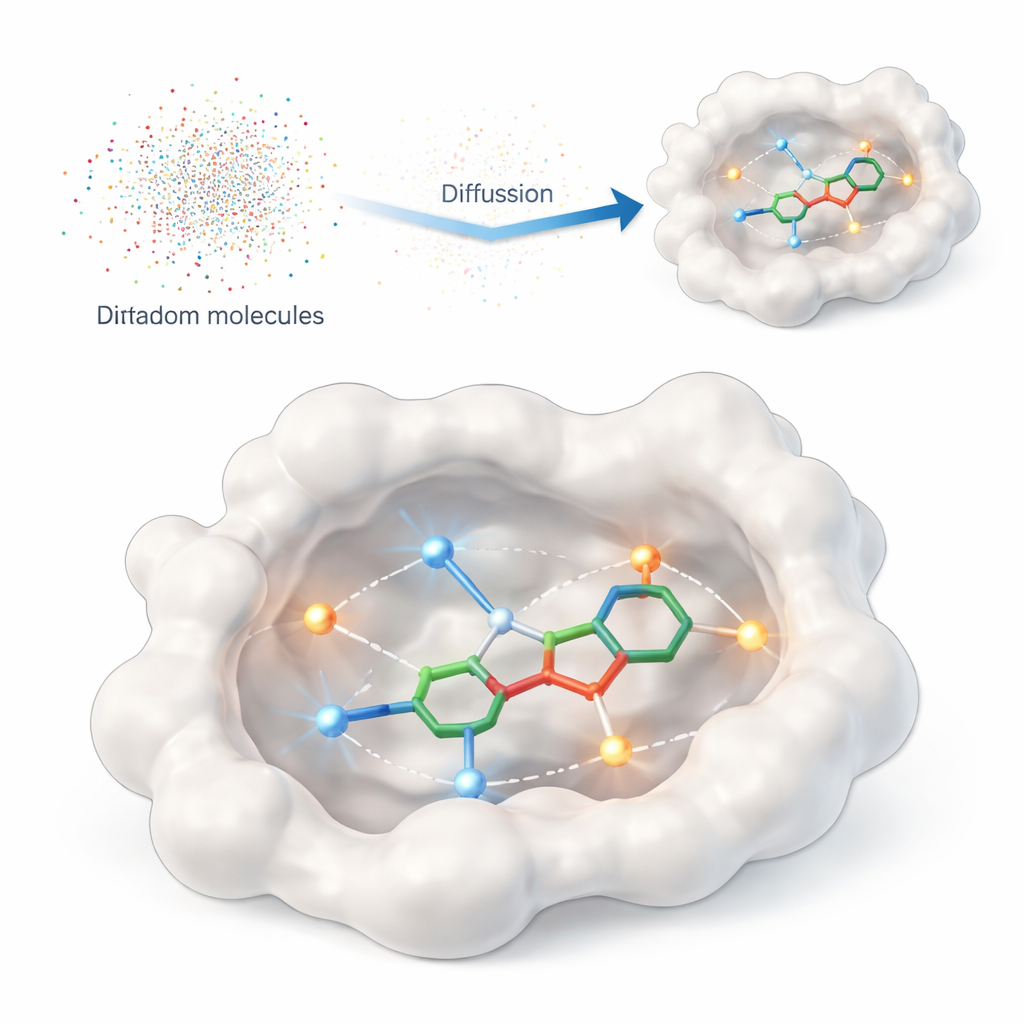
Este estudo apresenta o DiffPharma, uma estrutura computacional que gera moléculas 3D com características de fármacos diretamente dentro do sítio de ligação de uma proteína. Em vez de pedir ao algoritmo que vasculhe grandes catálogos de compostos existentes, o DiffPharma cria novos átomos a átomo, guiado por como eles devem interagir com a proteína. O método baseia-se em uma classe moderna de modelos generativos chamados modelos de difusão, que partem de ruído aleatório e gradualmente “remoção de ruído” até formar um objeto estruturado — neste caso, uma molécula 3D acomodada no bolso da proteína.
Codificando o aperto de mão da proteína
Para dizer ao modelo o que importa na superfície da proteína, os autores representam contatos-chave como pequenas “partículas de interação” espalhadas ao longo dos caminhos entre a proteína e uma molécula de referência. Dois tipos comuns de interação são enfatizados: ligações de hidrogênio, que atuam como ímãs direcionais entre átomos específicos, e contatos hidrofóbicos, onde regiões oleosas se agrupam afastando-se da água. Redes neurais separadas aprendem a geometria e a química de cada tipo de interação, assim como a forma global do bolso de ligação, e então uma arquitetura de fusão especial combina esses pontos de vista em uma única imagem coerente que orienta a geração molecular.
Quão bem isso imita padrões reais de ligação?
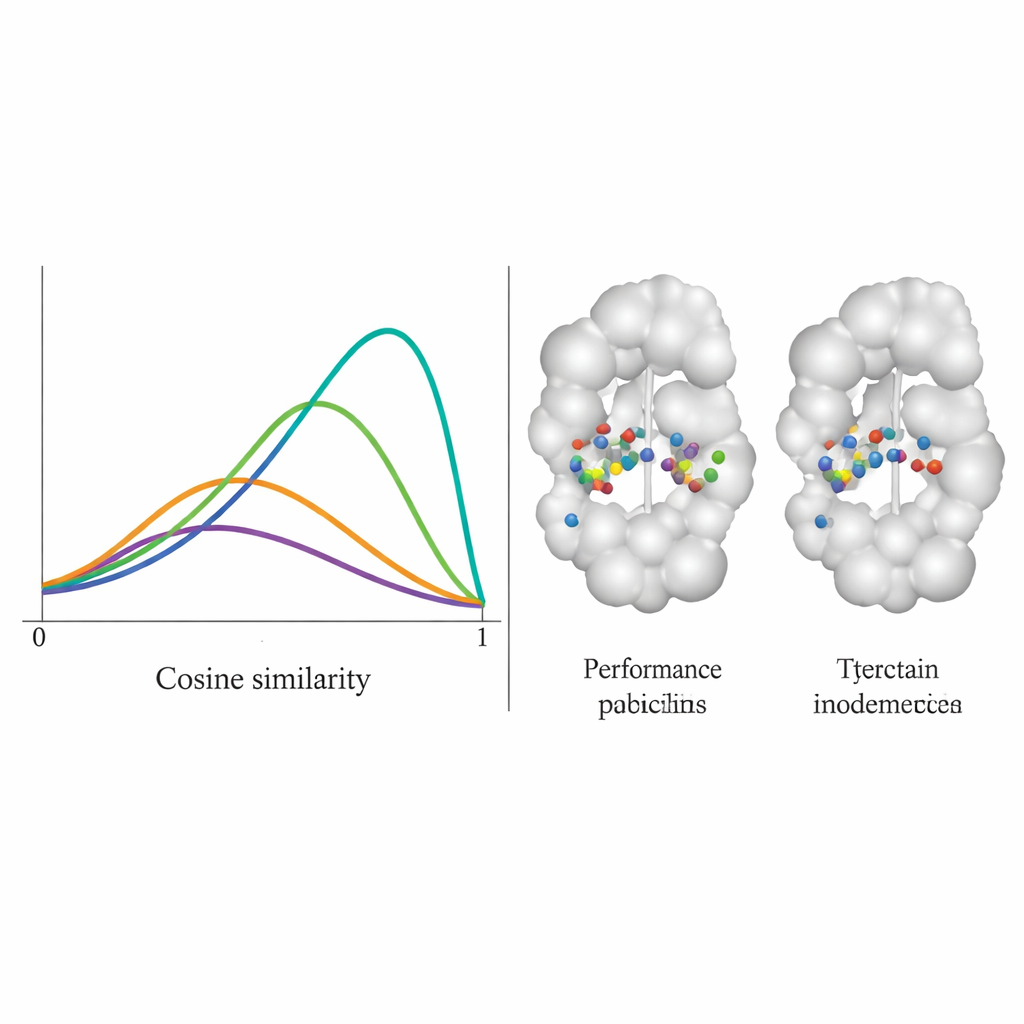
A equipe testou o DiffPharma em 100 pares diferentes proteína–molécula e avaliou o quão fielmente as novas moléculas reproduziam os padrões originais de contato, resíduo por resíduo. Eles mediram isso usando uma pontuação de similaridade de cosseno entre 0 e 1, onde 1 significa concordância perfeita. A distribuição do DiffPharma apresentou um pico em torno de 0,9, o que significa que, em média, os mesmos resíduos da proteína formaram os mesmos tipos de interações-chave que nas estruturas de referência — substancialmente melhor do que seis métodos concorrentes. Importante, o modelo alcançou isso mantendo uma variedade de formas moleculares, e os compostos gerados preservaram comprimentos de ligação, ângulos e geometria 3D gerais realistas, típicos de moléculas reais e estáveis.
Da teoria a candidatos farmacêuticos práticos
Além dos testes comparativos, os autores investigaram se o DiffPharma poderia projetar candidatos a fármacos plausíveis para alvos reais. Para duas enzimas bem estudadas — quinase AKT e uma β‑lactamase ligada à resistência a antibióticos — o método gerou moléculas que preservaram os padrões essenciais de interação de ligantes conhecidos, mas frequentemente usaram esqueleto químico diferente, uma forma desejável de “troca de scaffolds” em química medicinal. Em um estudo de caso mais exigente na protease principal do SARS‑CoV‑2, o DiffPharma foi orientado com escolhas de interação específicas e depois examinado com simulações de dinâmica molecular e estimativas de energia de ligação. Moléculas geradas sob restrições de interação mais estritas formaram complexos mais estáveis e às vezes apresentaram energias de ligação preditas mais favoráveis do que um inibidor de referência conhecido. Notavelmente, o sistema até redescobriu esse composto de referência — apesar de ele nunca ter aparecido no treinamento — unicamente a partir da estrutura da proteína e das instruções de interação.
O que isso significa para medicamentos futuros
Para um não especialista, o DiffPharma pode ser visto como uma ferramenta de projeto inteligente e com noção 3D para moléculas medicamentosas: dada a forma de um bolso de proteína e um padrão desejado de “apertos de mão”, ele propõe chaves quimicamente razoáveis que se encaixam e interagem da maneira certa. Embora ainda não otimize todas as propriedades que um medicamento precisa, como solubilidade ou metabolismo, o método preserva de forma confiável o mapa crucial de contatos na superfície da proteína e explora novas regiões do espaço químico além dos catálogos atuais. Essa abordagem guiada por interações pode ajudar os pesquisadores a avançar mais rapidamente de dados estruturais de proteínas relacionadas a doenças para pontos de partida diversos e realistas para o desenvolvimento experimental de fármacos.
Citação: Sako, M., Yasuo, N. & Sekijima, M. Interaction-constrained 3D molecular generation using a diffusion model enables structure-based pharmacophore modeling for drug design. npj Drug Discov. 3, 8 (2026). https://doi.org/10.1038/s44386-026-00040-x
Palavras-chave: desenho de fármacos baseado em estrutura, modelos generativos moleculares, modelagem farmacófora, interações proteína–ligante, protease principal do SARS-CoV-2