Clear Sky Science · pt
Desenvolvendo um protocolo para neutralizar a ativação espontânea in vitro de fibroblastos intestinais usando design de experimentos
Por que é importante manter as células de reparo intestinal calmas
Em doenças intestinais crônicas como a de Crohn, o tecido cicatricial pode estreitar o intestino progressivamente até que o alimento quase não passe, frequentemente levando à cirurgia. Essa formação de cicatriz, chamada fibrose, é impulsionada por células de suporte conhecidas como fibroblastos, que ficam hiperativas e depositam tecido conjuntivo em excesso. Para entender e, um dia, prevenir esse processo, os cientistas dependem de fibroblastos cultivados em laboratório. Mas há um problema: as placas plásticas simples usadas na maioria dos laboratórios induzem essas células a um estado ativado de forma artificial, dificultando o estudo dos primeiros passos que levam de um intestino saudável a um intestino fibrótico.
Quando o prato de laboratório manda o sinal errado
Os autores mostraram primeiro com que rapidez os fibroblastos intestinais se agitam em plástico padrão para cultura de tecidos. Em apenas 24 horas, tanto uma linhagem celular estabelecida quanto células primárias de doadores masculinos e femininos passaram de um estado silencioso para uma forma ativada, semelhante a músculo. Elas produziram altos níveis de proteínas associadas à contração e à cicatrização, como a actina α-suave e a proteína de ativação de fibroblastos, mesmo sem qualquer gatilho inflamatório adicionado. Isso significa que muitos modelos de laboratório existentes podem começar a partir de um estado que já se assemelha a uma doença em estágio avançado, em vez de mudanças iniciais e reversíveis.
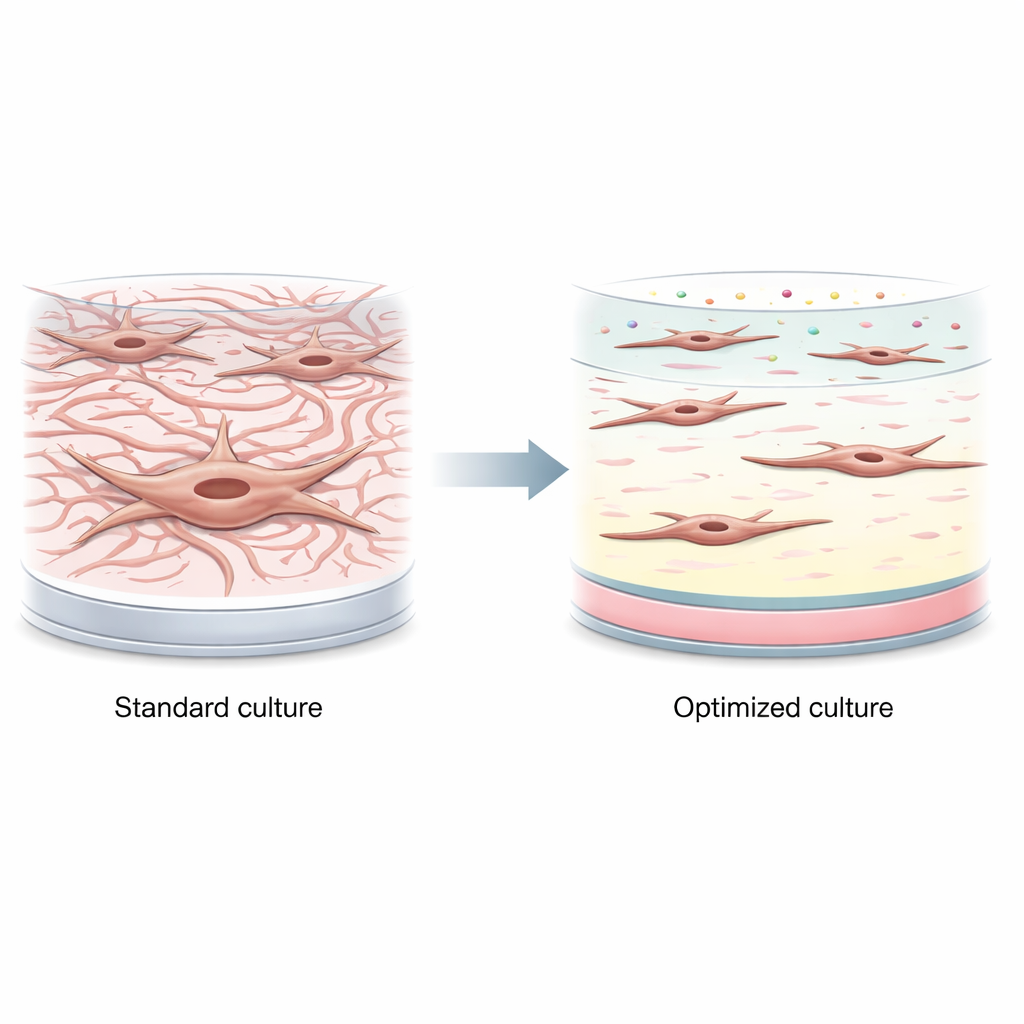
Testar ingredientes isolados não basta
Para acalmar as células novamente, a equipe explorou componentes do entorno natural dos fibroblastos no intestino, incluindo proteínas-chave da matriz (colágeno tipos I e III e laminina) e fatores solúveis (vitamina D e o fator de crescimento fibroblástico básico, FGF). Eles testaram esses elementos um a um, seja como revestimentos de superfície ou como aditivos ao meio de cultura. Algumas condições reduziram marcadores de ativação: por exemplo, doses moderadas de vitamina D diminuíram um marcador importante de cicatriz várias vezes, e certas densidades de revestimento tiveram efeitos leves. Mas esses benefícios foram compensados por problemas, como menor sobrevivência celular em níveis mais altos de vitamina D; de modo geral, os ajustes isolados não foram suficientes para manter os fibroblastos consistentemente em um estado de baixa atividade.
Deixar a estatística procurar o espaço de possibilidades
Em vez de mexer em um controle por vez, os pesquisadores utilizaram uma abordagem formal de “design de experimentos” para pesquisar muitas combinações de forma eficiente. Variaram cinco entradas — as três proteínas da matriz mais vitamina D e FGF — em uma ampla faixa de doses, gerando 42 condições de cultura cuidadosamente escolhidas. Para cada uma, mediram quatro desfechos ligados à cicatrização: um marcador-chave de ativação, secreção de uma proteína matricial importante (fibronectina), crescimento celular e sobrevivência celular. Modelos estatísticos então revelaram quais fatores, e quais pares entre eles, tiveram a maior influência. A vitamina D emergiu como um agente potente, porém sensível à dose, afetando todas as leituras, enquanto o FGF tendia a reduzir a ativação e a apoiar crescimento e sobrevivência celular. Colágeno I, colágeno III e laminina moldaram como esses sinais solúveis eram interpretados, com certas combinações atenuando a ativação muito mais do que qualquer fator isolado.
Elaborando uma receita para fibroblastos calmos, porém saudáveis
Usando esses modelos, a equipe pediu ao software que identificasse condições que ao mesmo tempo reduzissem marcadores de ativação e produção matricial, mantendo as células vivas, sem exigir que a proliferação fosse baixa. A melhor receita combinou alta densidade de colágeno I, baixo colágeno III e alta laminina na superfície de cultura, juntamente com vitamina D em faixa média e FGF em alta concentração no meio. Sob esse protocolo, os fibroblastos permaneceram delgados e fusiformes em vez de espalhados e estrelados, expressaram níveis muito menores de genes e proteínas ligados à contração e fibrose, e secretaram muito menos colágeno e fibronectina. Ao mesmo tempo, sua viabilidade manteve-se tão alta quanto — ou melhor que — a das células em plástico simples. Importante, esses efeitos se mantiveram não apenas na linhagem modelo, mas também em fibroblastos primários de doadores humanos masculinos e femininos, mostrando que o protocolo é robusto.
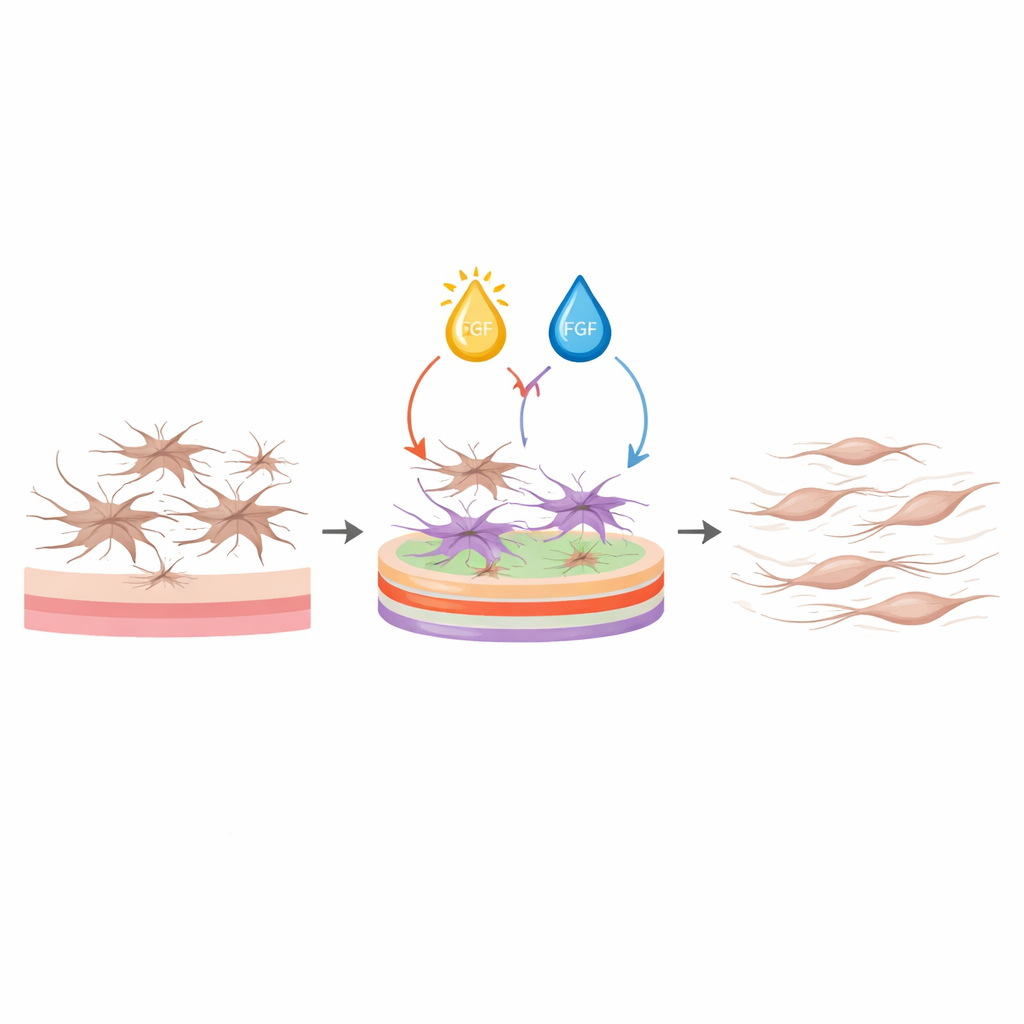
O que isso significa para pesquisas futuras sobre fibrose intestinal
Ao ajustar cuidadosamente o “vizinhança” ao redor dos fibroblastos intestinais — tanto a superfície à qual eles se aderem quanto os fatores que os banham — este estudo entrega um protocolo direto que mantém essas células em um estado não ativado, porém saudável, usando materiais de laboratório padrão. Para os pesquisadores, isso fornece um ponto de partida limpo para adicionar sinais inflamatórios ou mecânicos específicos e observar como a fibrose começa, em vez de trabalhar com células que já são parecidas com tecido cicatricial. Mais amplamente, o trabalho demonstra como o design estatístico pode descobrir combinações sutis e não intuitivas de ingredientes que domam comportamentos celulares complexos, abrindo caminho para melhores modelos de cicatrização e, eventualmente, estratégias mais específicas para prevenir ou reverter a fibrose intestinal.
Citação: Mohammadalizadeh, Z., Sudi, S., Basto Moreno, D.A. et al. Developing a protocol to counteract spontaneous in vitro activation of intestinal fibroblasts using design of experiments. npj Biomed. Innov. 3, 25 (2026). https://doi.org/10.1038/s44385-026-00079-5
Palavras-chave: fibrose intestinal, ativação de fibroblastos, protocolo de cultura celular, vitamina D e FGF, design de experimentos