Clear Sky Science · pt
Inferindo anomalias em vias de sinalização a partir de imagens histopatológicas via grafo heterogêneo gene-via com restrições lógicas
Vendo sinais celulares ocultos em lâminas de câncer
Quando médicos examinam câncer ao microscópio, eles enxergam principalmente formas e cores, não as complexas conversas moleculares que ocorrem dentro das células. Ainda assim, essas “conversas” invisíveis de sinalização entre genes e vias muitas vezes determinam como um tumor cresce e como pode responder ao tratamento. Este estudo apresenta um novo sistema de inteligência artificial que lê imagens de rotina da patologia e infere quais rotas de comunicação celular, ou vias, estão falhando — oferecendo uma maneira de vislumbrar o comportamento molecular sem exames laboratoriais adicionais.
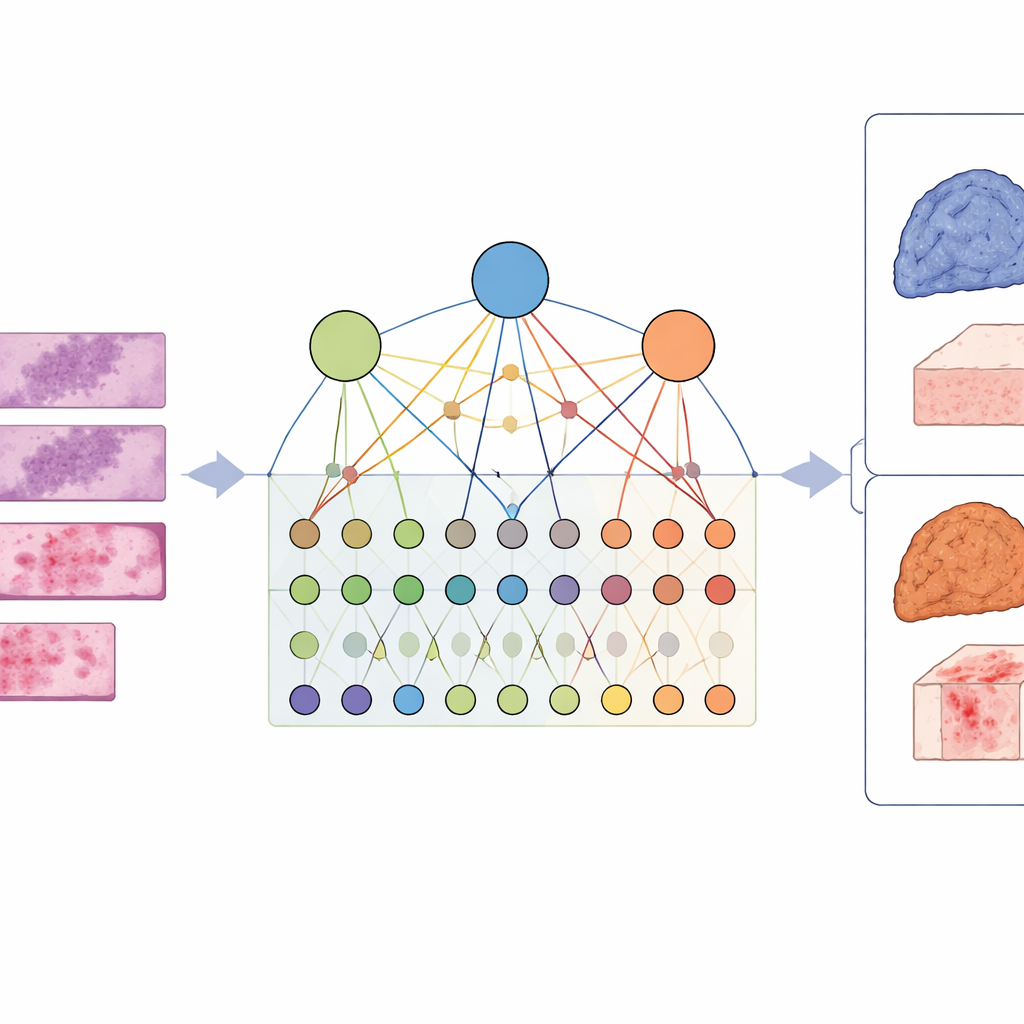
De pistas de genes isolados ao panorama maior
Abordagens tradicionais tentam prever o estado de genes individuais a partir de imagens de tecido: um gene específico está mutado ou não? Isso é útil, mas o câncer raramente depende de um único gene defeituoso. Em vez disso, grupos de genes atuam em conjunto para perturbar vias de sinalização inteiras que controlam crescimento, sobrevivência e imunidade. Os autores argumentam que focar em genes isolados perde esse comportamento cooperativo e pode não explicar por que tumores se parecem e agem de determinada maneira ao microscópio.
Construindo um mapa entre imagens, genes e vias
Para capturar essa complexidade, os pesquisadores projetaram uma estrutura chamada LCG-HGNN que liga três camadas de informação. Primeiro, eles dividem cada lâmina inteira de adenocarcinoma pulmonar em muitos pequenos pedaços e representam esses fragmentos como um grafo, onde regiões próximas ou de aparência similar são conectadas. Segundo, conectam marcadores genéticos às vias de sinalização usando bases de dados biológicas estabelecidas, construindo um segundo grafo que codifica quais genes pertencem a quais vias. Finalmente, permitem que um modelo de IA passe informação por esse grafo combinado, de modo que padrões de imagem, genes e vias influenciem-se mutuamente em vez de serem tratados isoladamente.
Ensinando ao sistema a biologia conhecida
Uma inovação chave é que o modelo não pode aprender livremente sem orientação. Os autores incorporam declarações claras, na forma de regras, derivadas de décadas de pesquisa sobre câncer. Por exemplo, algumas mutações quase nunca aparecem juntas no mesmo tumor, e algumas vias estão a montante ou a jusante de outras. Eles codificam tais regras como restrições lógicas que orientam suavemente as conexões internas e as previsões da IA. Se o modelo propõe uma combinação de alterações genéticas e de vias que conflita com a biologia conhecida ou com similaridades entre lâminas de pacientes, essas regras o empurram em direção a alternativas mais realistas.
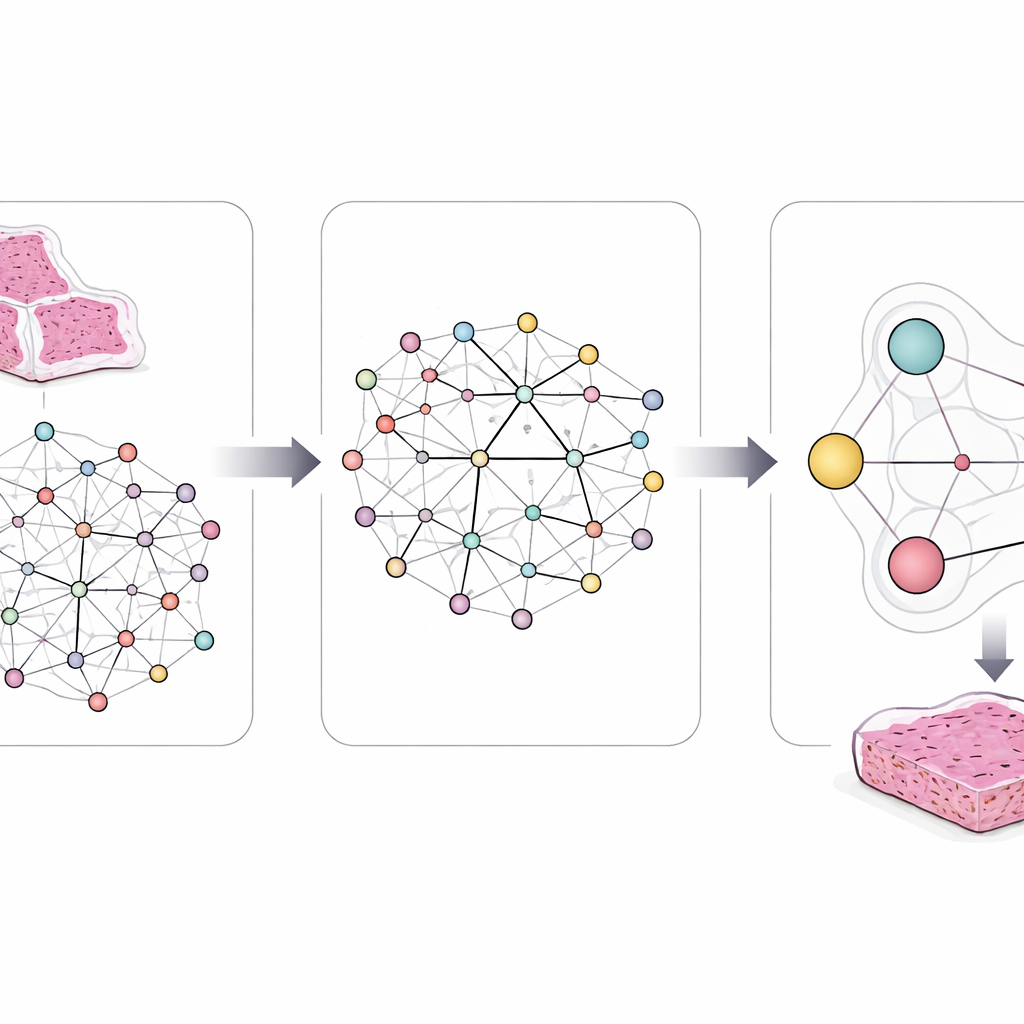
Testando a acurácia em relação a métodos existentes
A equipe avaliou seu sistema em mais de 1.600 lâminas de câncer de pulmão vinculadas a dados genéticos. Eles o compararam com modelos padrão de aprendizado profundo que focam em genes individuais e com métodos mais avançados que lidam com muitos genes ao mesmo tempo, mas ignoram a estrutura das vias. Em várias vias importantes, incluindo aquelas relacionadas a sinais de crescimento celular e à matriz de suporte do tecido, o novo modelo previu alterações em grupos de genes e anomalias em vias com maior precisão. Ele também produziu fragmentos de imagem cuja aparência correspondia de perto a exemplos clínicos reais conhecidos por estarem associados a mutações específicas, sugerindo que estava focando em padrões microscópicos significativos em vez de peculiaridades espúrias da imagem.
Por que isso importa para os pacientes
Para um não especialista, o resultado principal é que essa abordagem transforma uma lâmina de patologia de rotina em uma fonte rica de informação molecular. Em vez de solicitar testes genéticos separados, muitas vezes caros, para cada possível alvo, médicos poderiam eventualmente usar tais modelos para triagem de vias perturbadas diretamente a partir das imagens que já coletam. Embora o método ainda precise de validação maior em cenários do mundo real e não substitua por ora o teste genômico, ele aponta para um futuro em que a visão ao microscópio funciona também como uma janela para a fiação interna do tumor — ajudando a orientar um cuidado oncológico mais preciso e biologicamente informado.
Citação: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
Palavras-chave: vias do câncer, IA em histopatologia, redes neurais em grafos, adenocarcinoma pulmonar, patologia digital