Clear Sky Science · pt
Engenharia de macrófagos para imunoterapia contra o câncer: novas percepções e potencial terapêutico
Transformando a equipe de limpeza do corpo em combatentes do câncer
Nossos corpos estão cheios de macrófagos — células “faxineiras” que patrulham e engolem germes e tecidos mortos. Este artigo de revisão explora como os cientistas estão aprendendo a redirecionar essas células contra o câncer. Porque os macrófagos são abundantes dentro dos tumores, inclusive naqueles que resistem às principais imunoterapias atuais, compreender e engenheirá‑los pode abrir novas opções para pacientes com cânceres de difícil tratamento.
As muitas faces de um único tipo de célula
Macrófagos não são um tipo celular fixo; eles mudam de forma. Podem chegar pela corrente sanguínea ou já residir nos tecidos e, uma vez estabelecidos, respondem a sinais locais. Em tumores, esses macrófagos associados ao tumor podem tanto ajudar a matar células cancerosas quanto, de forma contraintuitiva, favorecer o crescimento e a disseminação do tumor. Antigamente, os pesquisadores tentavam encaixá‑los em duas categorias — “M1” (modo de ataque) e “M2” (modo de reparo ou suporte). Novas ferramentas de mapeamento genético e espacial mostram agora um espectro muito mais rico de estados, com múltiplos subgrupos e comportamentos que variam de um tumor e local para outro. Mesmo células antes consideradas firmemente “pró‑tumor” podem, em certos contextos, mobilizar células T e apoiar a imunidade antitumoral.
Sensando o ambiente e engolindo células cancerosas
Macrófagos não apenas escutam sinais químicos; eles também sentem o mundo físico ao seu redor. Ao rastejar pela densa malha proteica de um tumor, apertar-se entre células e suportar forças fluidas, eles percebem rigidez e tensão por meio de receptores especializados como o Piezo1. Esses sinais mecânicos, juntamente com sinais imunes clássicos, podem inclinar os macrófagos para papéis mais inflamatórios ou mais calmantes. Funcionalmente, os macrófagos podem engolfar células cancerosas, degradá‑las e exibir fragmentos (antígenos) às células T, conectando a imunidade inata e adaptativa. As células tumorais reagem enviando sinais de “não me coma”, notavelmente por meio da molécula de superfície CD47, que ativa um freio nos macrófagos. Medicamentos que bloqueiam essa interação estão em vários ensaios clínicos, aumentando a eliminação de células cancerosas, mas exigindo ajuste cuidadoso para evitar dano a células saudáveis.
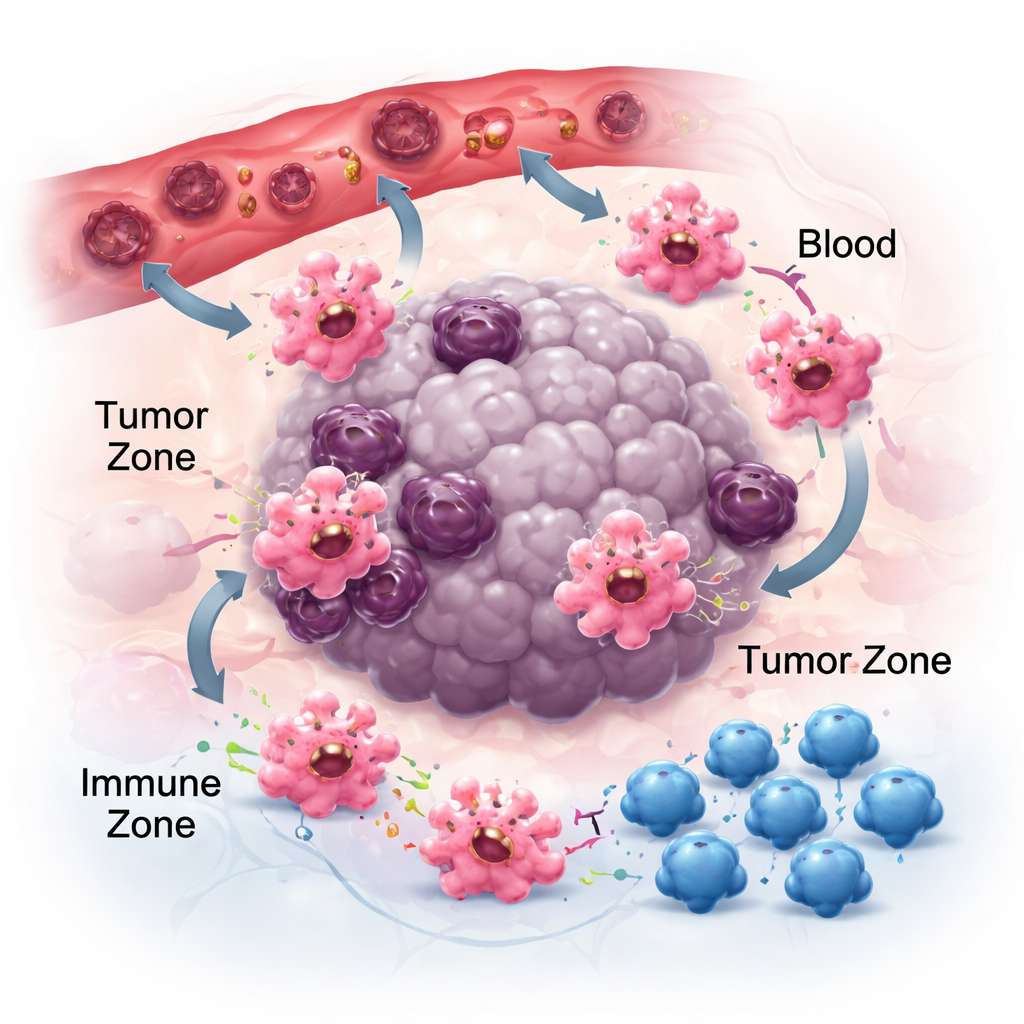
Movendo‑se, aderindo e comunicando no bairro tumoral
Para ter efeito no câncer, os macrófagos devem primeiro alcançar os tumores e depois posicionar‑se nos nichos certos. Eles seguem trilhas químicas — quimiocinas e fatores de crescimento — liberadas por células tumorais e circundantes. Pares como CCR2–CCL2 ajudam a atraí‑los para os tumores, e drogas que bloqueiam esses sinais podem reduzir o acúmulo de macrófagos, embora não completamente, apontando para outros atraentes como CSF‑1 e VEGF. Uma vez no local, a forma como os macrófagos aderem à matriz também molda seu comportamento. Seus receptores de adesão, chamados integrinas, não atuam apenas como cola; amplificam sinais inflamatórios e podem empurrar as células para estados mais antitumorais. Ao mesmo tempo, os macrófagos liberam pequenas bolsas chamadas vesículas extracelulares que transportam RNA e proteínas para células vizinhas. Dependendo do tipo tumoral, essas vesículas podem tanto atenuar a imunidade e favorecer a disseminação quanto reforçar respostas antitumorais, destacando a natureza dependente do contexto da comunicação macrófago‑célula.
Reprogramando macrófagos com genes e materiais
Como os macrófagos infiltram tumores sólidos naturalmente melhor do que muitas células T, os pesquisadores estão reengenheirando‑os como medicamentos vivos. Uma estratégia genética toma emprestado da terapia com células T de receptor de antígeno quimérico (CAR): adicionar um receptor sintético para criar macrófagos CAR (CAR‑M). Essas células projetadas reconhecem marcadores tumorais, engolfam células cancerosas com mais eficiência, digerem a matriz circundante, liberam sinais inflamatórios e ativam células T apresentando antígenos tumorais. Ensaios iniciais em humanos com CAR‑M direcionados a HER2 mostram segurança e atividade biológica encorajadoras, embora mais trabalho seja necessário para demonstrar benefícios fortes e duradouros. Em paralelo, abordagens não genéticas usam partículas e “mochilas” feitas de lipídios ou polímeros. Macrófagos podem engolir nanopartículas carregadas de fármacos e levá‑las profundamente aos tumores como cavalos de troia, ou usar adesivos na superfície que liberam lentamente sinais que estimulam a imunidade, ajudando‑os a manter uma identidade antitumoral sem sobrecarregar seu interior. Vesículas derivadas de macrófagos também estão sendo testadas como veículos naturais e sem células para entrega.
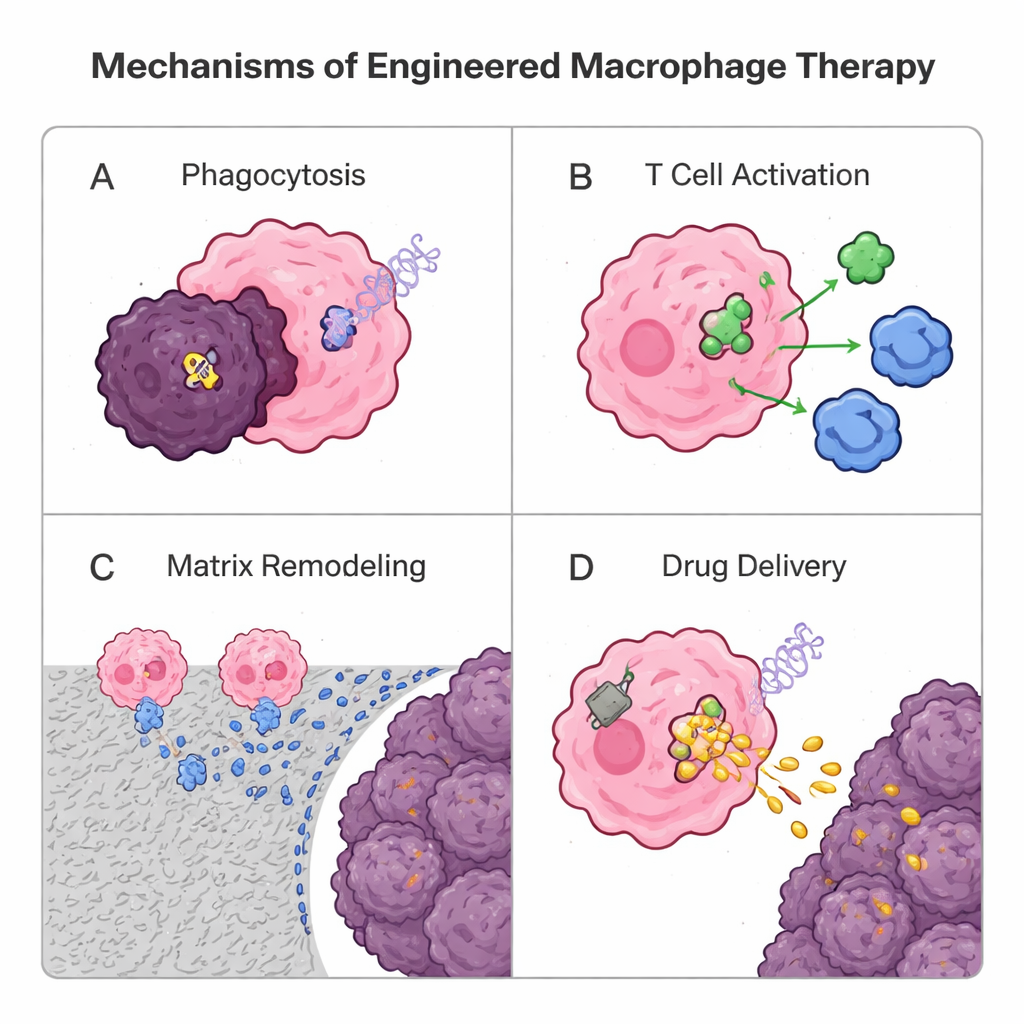
Desafios pela frente e motivos para otimismo
Apesar do potencial, as terapias com macrófagos precisam superar obstáculos práticos. Leva tempo e custa caro gerar células consistentes o suficiente a partir de pacientes, e uma vez infundidas, essas células não vivem ou se multiplicam indefinidamente. Sua flexibilidade inerente, embora biologicamente útil, pode dificultar mantê‑las travadas em um modo antitumoral dentro de um microambiente tumoral complexo e supressor. Os autores argumentam que modelos bioengenheirados avançados — culturas 3D, organoides e sistemas organ‑on‑a‑chip que imitam a mecânica dos tecidos reais — serão cruciais para entender e prever como macrófagos engenheirados se comportam em pacientes. Ainda assim, sua habilidade natural de penetrar tumores sólidos, comer células cancerosas e despertar células T, combinada com um histórico inicial de segurança, sugere que terapias baseadas em macrófagos podem se tornar uma nova arma importante, especialmente contra tumores “frios” que hoje resistem à maioria dos tratamentos imunológicos.
Citação: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
Palavras-chave: imunoterapia com macrófagos, microambiente tumoral, macrófagos CAR, fagocitose, liberação de fármacos por nanopartículas