Clear Sky Science · pt
Otimização da indução de inflamação em organoides epiteliais intestinais derivados de recém‑nascidos prematuros
Por que isso importa para recém‑nascidos frágeis
Bebês nascidos muito prematuros enfrentam uma combinação perigosa: um intestino imaturo e uma comunidade microbiana em rápida mudança. Juntos, esses fatores podem provocar uma inflamação descontrolada que danifica o intestino e leva a quadros potencialmente fatais, como a enterocolite necrosante. Como não é possível experimentar diretamente em prematuros, os cientistas precisam de modelos laboratoriais realistas dos seus intestinos para testar o que impulsiona a inflamação e como detê‑la. Este estudo refina um desses modelos usando tecidos intestinais cultivados em laboratório, oferecendo uma maneira mais clara de investigar quais sinais microbianos deslocam o equilíbrio da defesa normal para uma inflamação prejudicial.
Cultivando um intestino prematuro em uma placa
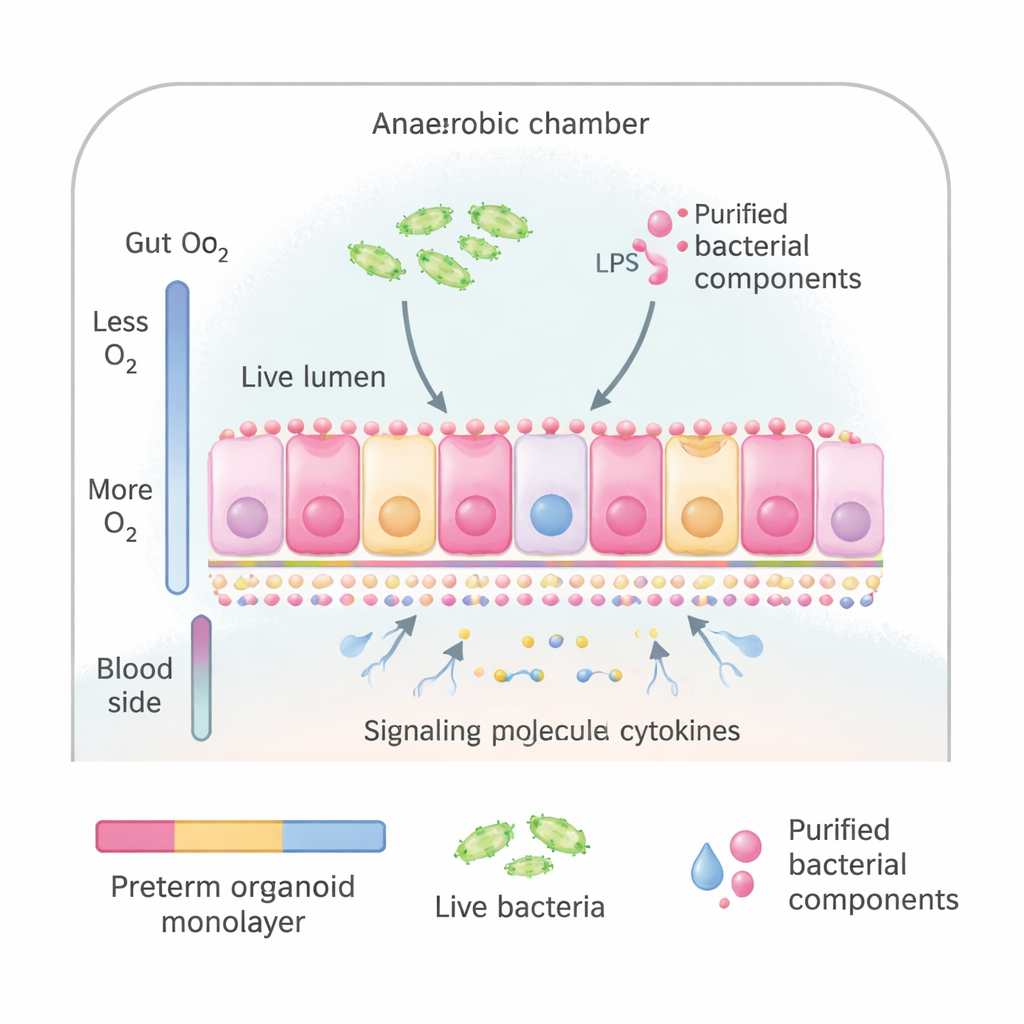
Os pesquisadores utilizaram organoides intestinais—versões em miniatura do revestimento intestinal cultivadas a partir de células‑tronco obtidas de recém‑nascidos prematuros durante cirurgia. Esses organoides podem ser achatados em uma lâmina fina de células que se assemelha e funciona muito como a superfície interna do intestino delgado, incluindo a orientação correta do lado apical (voltado ao conteúdo intestinal) e do lado basal (voltado ao sangue). A equipe colocou essas lâminas em um sistema de cultura especial que imita o gradiente natural de oxigênio do intestino: baixa oxigenação no lado exposto aos microrganismos e maior oxigenação no lado sanguíneo. Isso permitiu expor a superfície “intestinal” tanto a bactérias integrais obtidas de bebês prematuros quanto a componentes bacterianos purificados conhecidos por ativar o sistema imune.
Testando o que mais desencadeia um alarme inflamatório
Os cientistas compararam várias formas de provocar inflamação: uma mistura de bactérias vivas comumente encontradas em prematuros doentes; as mesmas bactérias após terem sido mortas por calor; e dois sinais bacterianos purificados, lipopolissacarídeo (LPS) da parede celular bacteriana e flagelina das estruturas filamentosas bacterianas. Mediram a liberação de IL‑8, uma proteína sinalizadora que atrai células imunes e serve como marcador geral de inflamação, e usaram análises proteômicas em larga escala para observar como a maquinaria interna das células intestinais mudava. Surpreendentemente, bactérias vivas ou mortas não aumentaram fortemente a IL‑8 nesse sistema, mesmo após 24 horas. Em contraste, a flagelina e, especialmente, a combinação de flagelina com LPS desencadearam um aumento claro de IL‑8 em apenas três horas, mostrando que esses sinais purificados podiam ativar de forma confiável um estado inflamatório.
Encontrando a configuração mais realista e eficiente
Para melhor corresponder à biologia intestinal real, a equipe prestou atenção aonde cada sinal age naturalmente. O LPS é normalmente percebido no lado do epitélio que enfrenta o conteúdo intestinal, enquanto a flagelina é detectada principalmente no lado tecidual. Usando doses muito mais baixas e mais fisiologicamente realistas do que em experimentos anteriores, aplicaram LPS ao lado superior (voltado ao lúmen) e flagelina ao lado inferior (voltado ao sangue) da lâmina de organoide. Essa simples alteração produziu uma resposta forte e ampla em três horas: múltiplos mediadores inflamatórios—incluindo IL‑8, TNF e várias quimiocinas—foram secretados de ambos os lados do tecido. Ao mesmo tempo, centenas de proteínas celulares tiveram alterações de abundância, indicando ativação em larga escala de vias de defesa.
Inflamação, freios e reparo no mesmo modelo
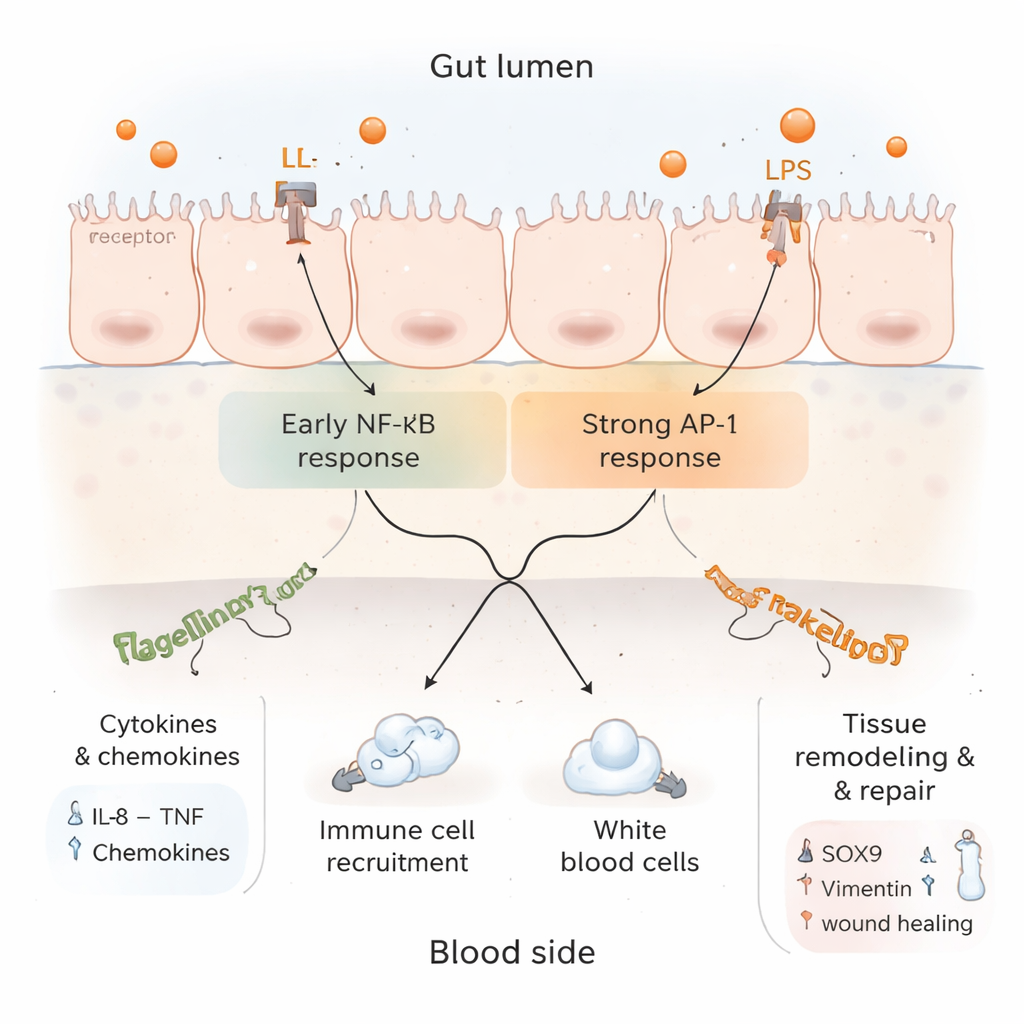
Ao aprofundar a análise proteômica, os pesquisadores encontraram um quadro complexo. Por um lado, marcadores de inflamação ativa e recrutamento de células imunes foram aumentados, e rotas de sinalização ligadas a TNF e IL‑17—ambas centrais na defesa imunológica intestinal—foram ativadas. Por outro lado, vários componentes da via clássica NF‑κB, que impulsiona muitos genes inflamatórios, foram atenuados, enquanto uma rota alternativa envolvendo AP‑1 manteve‑se ativa. Isso sugere que, após o alarme inicial, o tecido começa a aplicar freios para evitar danos descontrolados. Paralelamente, proteínas associadas à regeneração tecidual, remodelação estrutural e morte celular controlada aumentaram, indicando que o revestimento intestinal não estava apenas inflamado, mas também tentando remodelar‑se e reparar‑se.
O que isso significa para tratamentos futuros
Ao comparar sistematicamente diferentes estímulos microbianos, doses, posições e tempos de exposição, os autores concluem que uma exposição de três horas a LPS em baixa dose no lado intestinal, combinada com flagelina no lado sanguíneo, é a forma mais robusta e reprodutível de induzir inflamação em organoides intestinais derivados de prematuros. Esse modelo refinado captura não apenas o surto inflamatório, mas também os mecanismos inatos de controle, tolerância e respostas de reparo do frágil intestino prematuro. Fornece um roteiro prático para outros laboratórios estudarem como microrganismos específicos, fármacos ou fatores nutricionais podem agravar ou acalmar a inflamação intestinal em bebês muito prematuros—um passo essencial rumo a estratégias direcionadas e mais seguras para prevenir doenças intestinais devastadoras nesse grupo vulnerável.
Citação: Chapman, J.A., Frey, A.M., Dueñas, M.E. et al. Optimising the induction of inflammation within preterm infant-derived intestinal epithelial organoids. npj Gut Liver 3, 5 (2026). https://doi.org/10.1038/s44355-026-00054-2
Palavras-chave: intestino de recém‑nascido prematuro, organoides intestinais, inflamação intestinal, microbioma, enterocolite necrosante