Clear Sky Science · pt
Transdução quimio-mecânica fora do equilíbrio do desdobramento de proteínas movido por ATP no proteassoma 26S
Como uma Máquina Minúscula Mantém Nossas Proteínas na Linha
Dentro de cada célula, um trituradores microscópico chamado proteassoma 26S destrói constantemente proteínas danificadas ou desnecessárias, mantendo a célula saudável. No coração dessa máquina há um motor em forma de anel que queima combustível químico (ATP) para agarrar, desdobrar e puxar proteínas para uma câmara central onde são fragmentadas. Este artigo usa simulações computacionais avançadas para revelar como esse motor converte energia química em movimento mecânico, oferecendo um retrato detalhado e quantitativo de um processo que sustenta o envelhecimento, doenças cerebrais, imunidade e câncer.
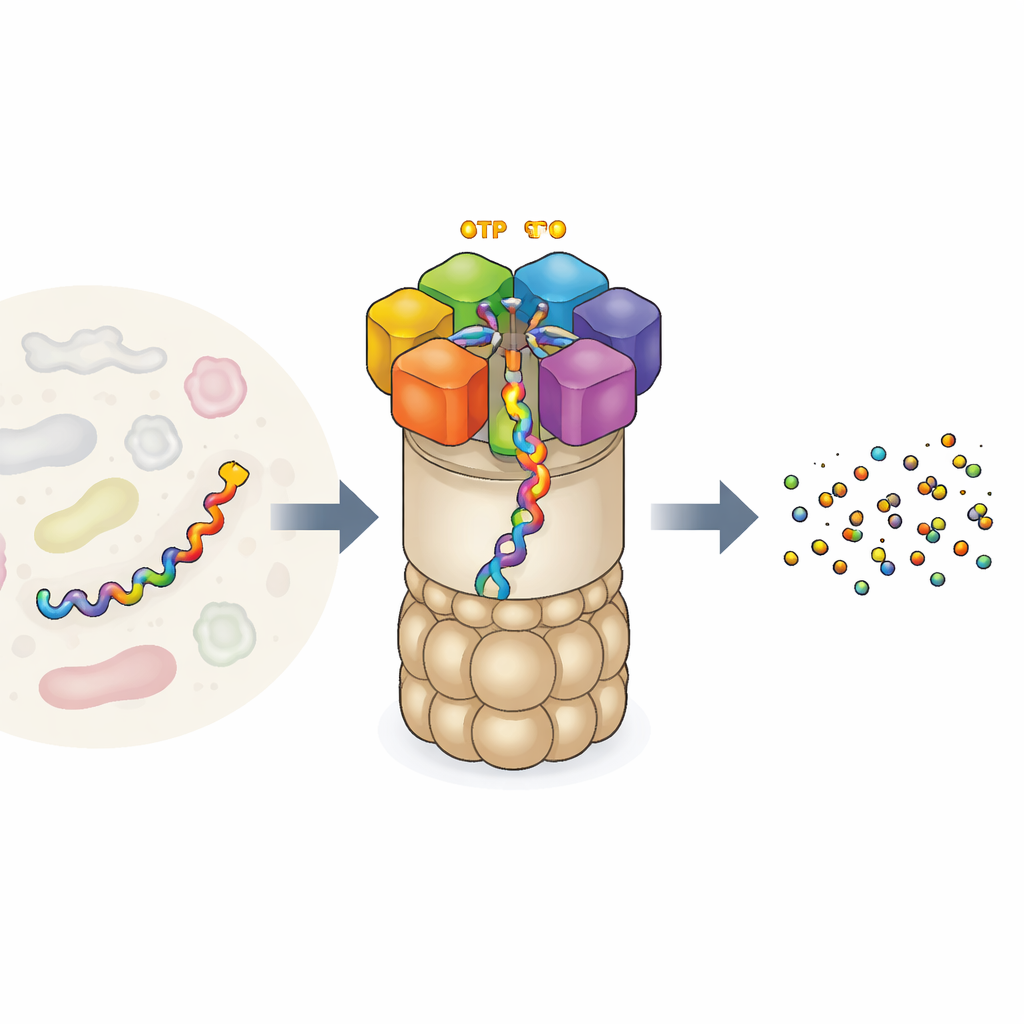
A Fábrica de Reciclagem de Proteínas da Célula
O proteassoma 26S é uma das maiores e mais intrincadas máquinas proteicas nas nossas células. Consiste em um núcleo em forma de barril que corta proteínas e uma tampa reguladora que reconhece quais proteínas devem ser destruídas. No portal há um anel de seis unidades motoras diferentes. Cada unidade pode ligar ATP, a moeda energética universal da célula, e usa essa energia para segurar uma cadeia proteica e puxá‑la para o núcleo para degradação. Esse motor não age de forma aleatória: experimentos anteriores sugeriram que as seis unidades trabalham de maneira coordenada, em um movimento “mão a mão”, passando a proteína adiante como alpinistas numa corda. Mas os experimentos só conseguiam ver alguns instantâneos dessa ação, deixando em aberto questões sobre a sequência completa de movimentos e como exatamente a queima do combustível se liga ao trabalho mecânico.
Simulando uma Corda de Guerra Molecular
Os autores construíram um modelo computacional probabilístico que trata o motor como um sistema que salta entre muitas formas possíveis enquanto moléculas de ATP e seus produtos se ligam e desligam. Eles definiram 30 conformações principais do anel nas quais uma, duas ou três subunidades motoras perdem o aperto sobre a proteína, além de um estado especial estreitamente fechado em que todas as seis mantêm a aderência. Usando um algoritmo padrão para simular eventos químicos aleatórios, eles acompanharam centenas de milhares de passos nos quais ocorre ligação de ATP, quebra de ATP e mudanças de forma do motor. A partir dessas simulações, puderam prever quão rápido uma proteína é puxada em diferentes condições, como variações nas quantidades de ATP, sua forma gasta ADP, e um análogo de ATP não quebrável frequentemente usado em experimentos.
Quando Combustível em Excesso Retarda o Motor
As simulações reproduziram várias descobertas experimentais intrigantes. Conforme os níveis de ATP aumentam a partir de valores baixos, o motor puxa as proteínas mais rápido, porque a ligação do combustível é a etapa mais lenta. Mas além de cerca de 1 milimolar de ATP, a velocidade atinge um pico e então cai: o anel passa mais tempo em uma conformação emperrada, não translocante, em que as seis subunidades estão ocupadas por ATP, mas a proteína não se move. Adicionar ADP ou o análogo não quebrável de ATP desacelera o motor de forma contínua, porque essas moléculas competem com o ATP pelos bolsões de ligação, mas não conseguem completar o golpe de força. O modelo também prevê como o motor se comporta quando encontra regiões muito bem dobradas de uma proteína, que atuam como obstáculos. Nesses casos, o motor passa mais tempo lutando contra a resistência, e a taxa geral de degradação cai, concordando com medidas feitas com domínios proteicos artificialmente estabilizados.
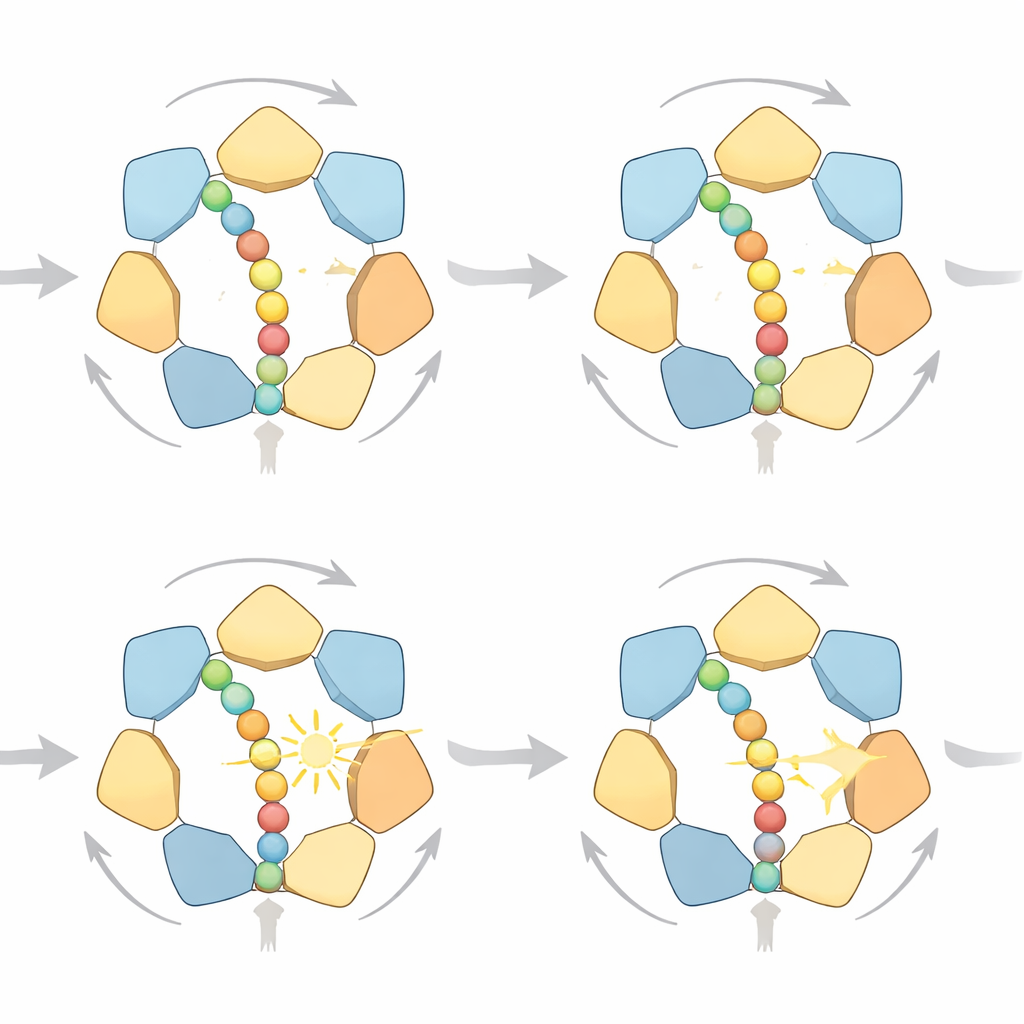
Muitas Maneiras de Dar um Passo
Ao examinar em detalhe as trajetórias simuladas, os pesquisadores descobriram que o anel não segue um único ciclo rígido. Em vez disso, existem múltiplas vias de alta probabilidade que todas respeitam a mesma regra direcional “mão a mão”: subunidades próximas à saída do anel liberam a proteína após a quebra do ATP, movem‑se para o topo de uma escada em espiral de subunidades e reapertam a cadeia mais adiante. Às vezes a proteína avança por um pequeno passo, às vezes por dois, dependendo de quantas subunidades soltam juntas. Com combustível em abundância, movimentos de um passo predominam porque desperdiçam menos trabalho contra forças opostas; quando o combustível é escasso, o modelo prevê saltos de dois passos com mais frequência. As simulações também conectam a carga mecânica ao estado químico do motor: à medida que a resistência aumenta e a proteína trava, o ADP tende a se acumular em mais bolsões de ligação — exatamente o que estudos estruturais de alta resolução observam.
Uso de Energia e Regras de Projeto Compartilhadas
O modelo permite aos autores mapear como a energia do motor aumenta quando o ATP é quebrado e diminui quando essa energia é convertida em movimento. Eles calculam uma curva de eficiência mostrando que o motor funciona melhor sob uma força opositora intermediária: resistência muito baixa e ele queima ATP de forma desperdiçadora; resistência demais e ele praticamente para. Quando a equipe comparou suas previsões com dados de máquinas relacionadas de degradação proteica em bactérias e leveduras, encontrou tendências muito semelhantes em como um análogo de ATP não quebrável desacelera esses motores. Isso sugere que muitos membros da mesma família de enzimas em forma de anel compartilham provavelmente um mecanismo comum e conservado para puxar proteínas.
Por Que Isso Importa para Saúde e Doença
Ao transformar instantâneos estruturais dispersos e medições bioquímicas em uma única estrutura testável, este trabalho mostra em detalhe quantitativo como um pequeno motor molecular traduz combustível químico em força para reciclar as proteínas da célula. O modelo não só explica uma ampla gama de experimentos existentes, como também faz previsões sobre como mudanças nos níveis de combustível, na carga mecânica ou em mutações do motor podem alterar a destruição de proteínas. Como máquinas semelhantes operam em todas as formas de vida e são centrais em condições que vão da neurodegeneração ao câncer, entender seu funcionamento interno nesse nível pode, em última análise, orientar o desenho de drogas que ajustem, aumentem ou bloqueiem seletivamente esses trituradores microscópicos.
Citação: Wu, D., Ouyang, Q., Wang, H. et al. Nonequilibrium chemomechanical transduction of ATP-driven protein unfolding in the 26S proteasome. npj Biol. Phys. Mech. 3, 4 (2026). https://doi.org/10.1038/s44341-026-00034-w
Palavras-chave: proteassoma, motor AAA+ ATPase, degradação de proteínas, máquinas moleculares, acoplamento quimio-mecânico