Clear Sky Science · pt
Detecção ultrassensível de proteínas sem enzimas usando ensaio de proximidade imunológica com microscopia de absorção por ressonador fotônico
Por que encontrar traços minúsculos de proteínas importa
Médicos e pesquisadores dependem cada vez mais de proteínas no sangue para sinalizar câncer, doenças cardíacas, infecções ou inflamação prejudicial muito antes dos sintomas se tornarem graves. Mas muitos desses sinais moleculares aparecem em níveis tão baixos que os testes laboratoriais padrão de hoje têm dificuldade para detectá‑los de forma rápida ou barata. Este estudo apresenta um novo método de teste, chamado PINATA, que pode identificar quantidades extremamente pequenas de uma proteína associada à inflamação usando equipamento simples e etapas à temperatura ambiente, abrindo caminho para diagnósticos mais acessíveis e sensíveis.
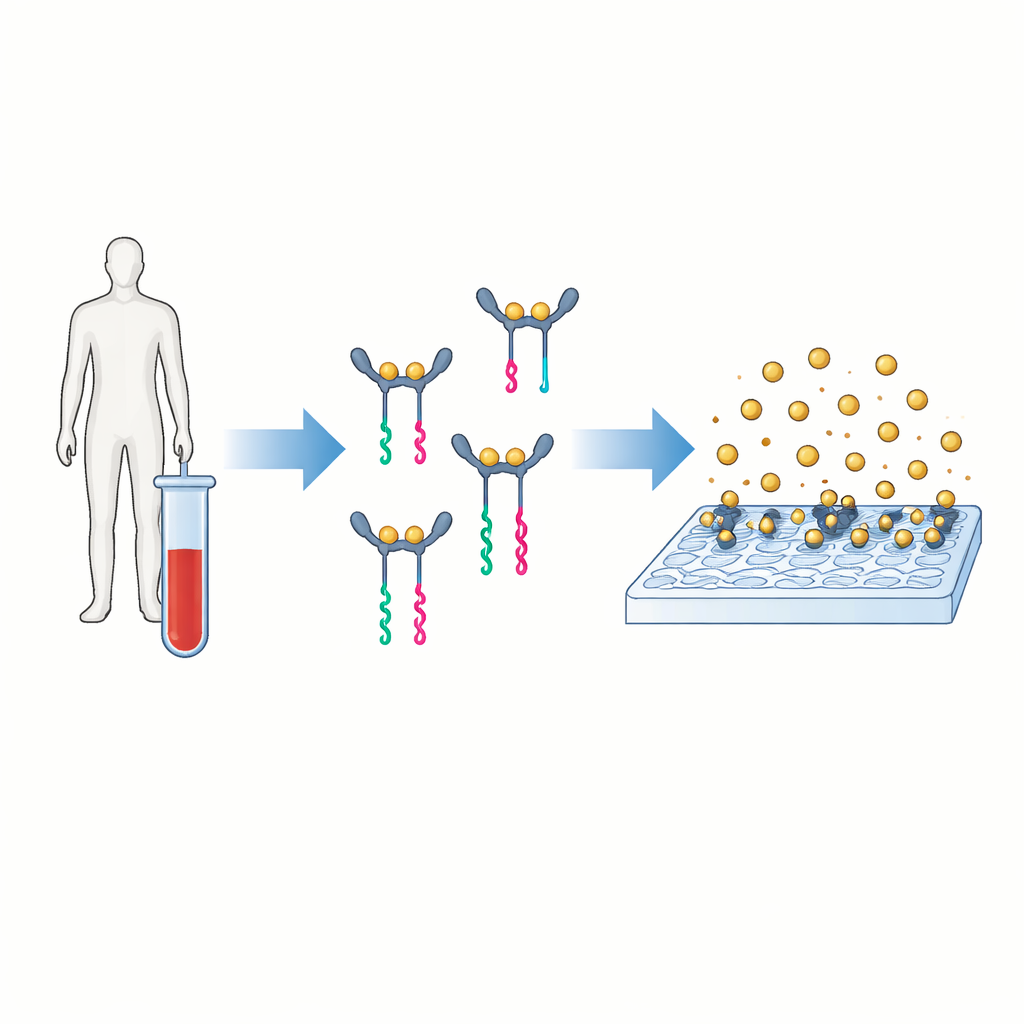
Uma nova forma de transformar proteínas em sinais legíveis
A ideia central do PINATA é traduzir a presença de uma proteína em um pequeno fragmento de DNA que é fácil de amplificar e contar. Os autores focam na interleucina‑6, uma molécula de sinalização no sangue que aumenta em condições que vão de infecção a câncer. Em testes convencionais, dois anticorpos se prendem à proteína e carregam uma enzima que gera um sinal colorido ou fluorescente. O PINATA mantém a noção básica de dois anticorpos reconhecendo a mesma proteína, mas em vez de enzimas anexa fitas curtas de DNA a cada anticorpo. Quando ambos os anticorpos se ligam à mesma proteína e se aproximam, seus parceiros de DNA cooperam para liberar um fragmento de DNA separado chamado repórter. Cada molécula de proteína pode assim desencadear a liberação de muitos repórteres de DNA idênticos.
Usando "regras de trânsito" de DNA em vez de enzimas
No cerne do método estão circuitos de DNA cuidadosamente projetados que se comportam como sistemas moleculares de tráfego, dirigindo quando fitas podem se ligar, se desligar ou trocar de parceiros. Esses circuitos são construídos de forma que, a menos que uma proteína aproxime as duas peças de DNA ligadas aos anticorpos, o DNA repórter permaneça travado e nenhum sinal seja gerado. Quando a proteína está presente, sua ação de ponte libera o repórter. Esse repórter liberado participa então de um processo secundário de amplificação em uma superfície preparada. Lá, ele se envolve repetidamente em reações de troca de fitas que permitem que uma única molécula repórter recrute muitas nanopartículas de ouro para a superfície, criando um sinal digital forte sem usar enzimas ou ciclos de temperatura.
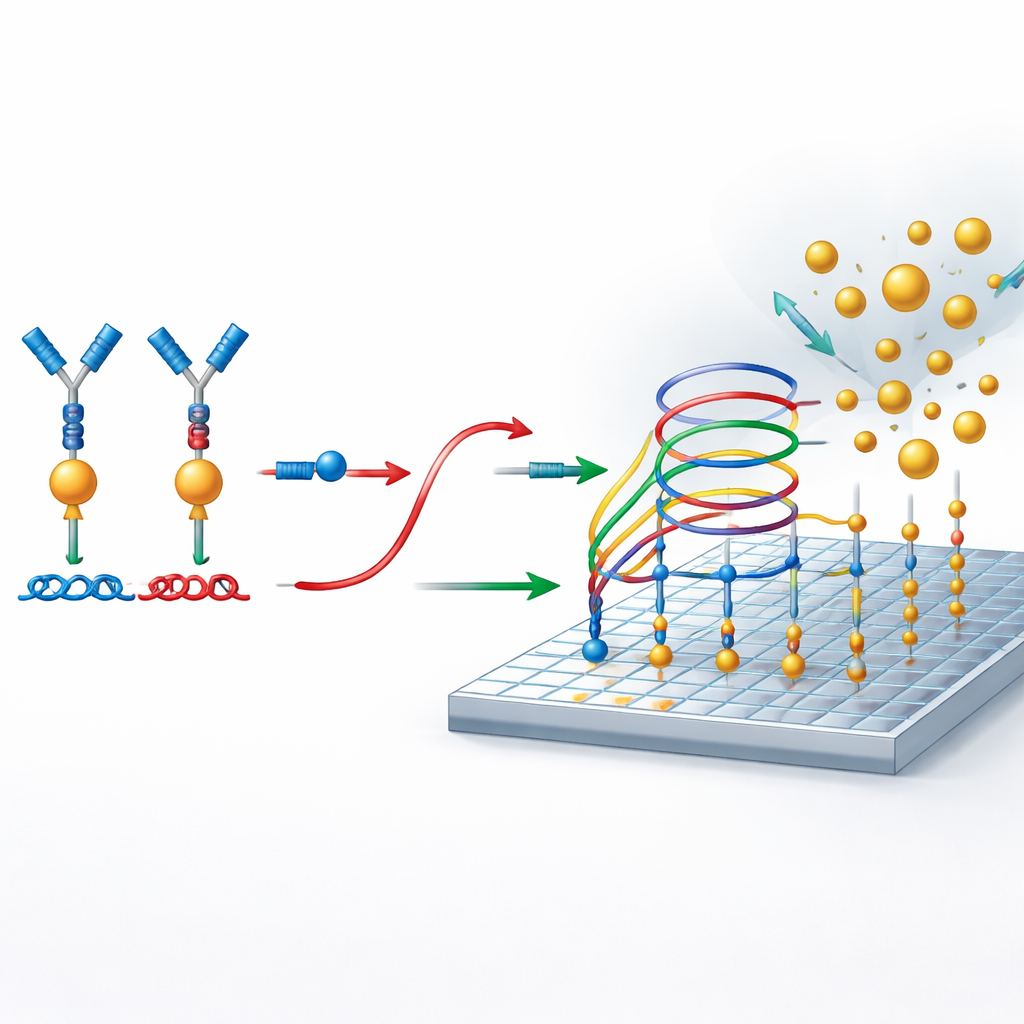
Contando nanopartículas individuais como eventos sim-não
Para ler o resultado, os pesquisadores usam microscopia de absorção por ressonador fotônico, ou PRAM. A superfície sensora é um material padronizado especialmente que reflete fortemente a luz em uma cor particular. Quando nanopartículas de ouro pousam nessa superfície, elas absorvem essa luz e aparecem como pontos escuros na imagem do microscópio. Como o sistema é projetado para que as nanopartículas só se liguem quando o DNA repórter está presente, cada ponto escuro representa um evento de detecção bem‑sucedido vinculado a uma molécula de proteína. Um conjunto óptico simples e de baixo custo e um software de processamento de imagem são então usados para contar esses pontos pela superfície, transformando o número de nanopartículas em uma medida precisa da concentração de proteína.
Quão sensível e seletivo é o ensaio?
Usando essa abordagem, a equipe mostra que pode detectar interleucina‑6 em níveis tão baixos quanto 37 femtogramas por mililitro — aproximadamente algumas dezenas de moléculas em uma gota — ao longo de uma faixa dinâmica que abrange seis ordens de magnitude. O ensaio funciona em um protocolo direto de duas etapas, com 90 minutos de duração, realizado inteiramente à temperatura ambiente. Os autores também demonstram que o teste permanece preciso mesmo quando a interleucina‑6 é misturada em amostras complexas como soro e plasma humanos, que tipicamente interferem em medições sensíveis. Eles confirmam ainda que os anticorpos direcionados à interleucina‑6 não respondem a outras proteínas relacionadas, enfatizando a seletividade do ensaio.
O que isso pode significar para diagnósticos futuros
Para um não especialista, a principal conclusão é que o PINATA oferece uma forma de detectar proteínas relacionadas a doenças em níveis extremamente baixos usando um instrumento óptico compacto em vez de equipamentos laboratoriais volumosos e caros. Ao combinar circuitos de DNA inteligentes com contagem digital de nanopartículas, o método evita enzimas frágeis e etapas de aquecimento, alcançando ou superando a sensibilidade de muitos testes avançados de proteínas. Com desenvolvimento adicional e adaptação para outros alvos, essa estratégia pode permitir diagnóstico mais precoce, monitoramento mais frequente e testes ponto‑de‑atendimento para uma ampla gama de condições em que pequenas variações nos níveis de proteínas têm grande importância clínica.
Citação: Shepherd, S., Bhaskar, S., Xu, H. et al. Ultrasensitive non-enzymatic protein detection using proximity immunoassay with photonic resonator absorption microscopy. npj Biosensing 3, 21 (2026). https://doi.org/10.1038/s44328-026-00090-1
Palavras-chave: detecção de biomarcadores proteicos, diagnósticos ultrassensíveis, deslocamento de fita de DNA, ensaio de interleucina-6, biossensoriamento digital