Clear Sky Science · pt
Vesículas extracelulares de neurônios e astrócitos isoladas por nanomagnetismo microfluídico para diferenciar doença de corpos de Lewy e doença de Alzheimer
Por que isso importa para famílias e médicos
Demência é um termo guarda-chuva que abrange várias doenças cerebrais com sintomas semelhantes, mas causas subjacentes bem diferentes. Duas das mais comuns, a doença de Alzheimer e a doença de corpos de Lewy, podem se apresentar de forma quase idêntica na clínica, porém respondem de modo distinto a medicamentos e envolvem riscos diferentes. Hoje, a única maneira de saber com certeza qual doença uma pessoa teve é examinar o cérebro após a morte. Este estudo descreve um novo tipo de exame de sangue que lê mensagens minúsculas liberadas por células cerebrais, com o objetivo de distinguir essas duas demências enquanto as pessoas ainda estão vivas.
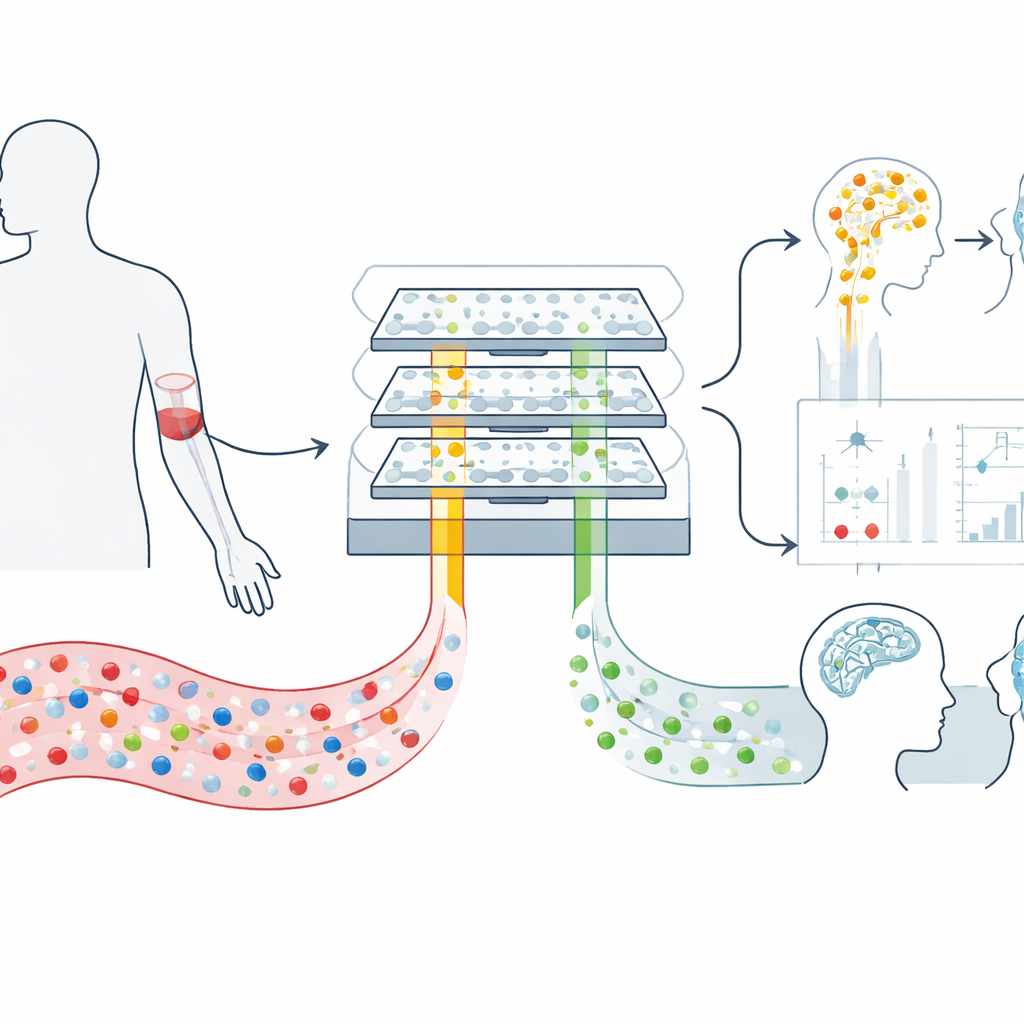
Pacotes minúsculos que viajam do cérebro para o sangue
Nossos cérebros constantemente liberam bolhas microscópicas chamadas vesículas extracelulares na corrente sanguínea. Essas vesículas são como envelopes acolchoados enviados por neurônios e suas células de suporte, carregando fragmentos de material genético e proteínas que refletem o que está ocorrendo dentro do cérebro. Como elas podem atravessar a barreira hematoencefálica e sobreviver na circulação, oferecem uma janela rara e minimamente invasiva para a biologia cerebral. O desafio é que um mililitro de sangue contém centenas de bilhões de vesículas de todo o corpo, de modo que as de origem cerebral estão em grande minoria e são difíceis de separar com métodos laboratoriais padrão.
Um chip magnético que separa sinais cerebrais
Para enfrentar esse problema, os pesquisadores construíram um dispositivo microfluídico chamado mTENPO que combina um chip do tamanho de um cartão com um ímã potente. Antes de a amostra de sangue entrar no chip, as vesículas são marcadas com nanopartículas magnéticas usando anticorpos que se ligam a proteínas de superfície tipicamente encontradas em vesículas de neurônios (GluR2) ou de astrócitos (GLAST). À medida que a mistura marcada flui por milhões de poros minúsculos no chip, o campo magnético puxa as vesículas cerebrais fortemente marcadas em direção às paredes dos poros, retendo-as enquanto o restante passa. Dessa forma, a equipe consegue enriquecer de forma independente duas populações de vesículas — aquelas majoritariamente de neurônios e aquelas majoritariamente de astrócitos — diretamente a partir de uma pequena amostra de plasma.
Lendo as impressões digitais moleculares
A partir de 137 voluntários cujos diagnósticos cerebrais foram confirmados após a morte, a equipe isolou esses dois tipos de vesículas e também mediu proteínas clássicas do Alzheimer no sangue, como diferentes formas de beta-amiloide e tau. Em seguida, sequenciaram pequenos RNAs regulatórios (miRNAs) dentro das vesículas e investigaram quais deles diferiam entre pessoas com doença de corpos de Lewy pura, Alzheimer puro, patologias mistas ou sem demência. Vários miRNAs transportados por vesículas de origem neuronal e astrociitária, juntamente com várias proteínas relacionadas à tau no plasma, mostraram padrões distintos entre os grupos de Lewy e Alzheimer. Quando os pesquisadores mapearam os genes alvo desses miRNAs, encontraram ligações fortes com vias envolvidas em sobrevivência celular, inflamação e manejo de proteínas — processos já implicados na neurodegeneração.
Construindo um exame de sangue combinado e poderoso
Como nenhum marcador isolado separou claramente as doenças, a equipe usou ferramentas de aprendizado de máquina para montar um painel compacto com os sinais mais informativos extraídos de todos os três compartimentos: vesículas neuronais, vesículas de astrócitos e proteínas sanguíneas. O painel final de 15 características incluiu 14 miRNAs específicos de vesículas mais duas proteínas tau fosforiladas. Testado com validação cruzada repetida para reduzir sobreajuste, esse painel multimarcador distinguiu doença de corpos de Lewy de Alzheimer com cerca de 95% de acurácia e área sob a curva de 0,96 — substancialmente melhor do que qualquer medida individual isolada. Pessoas cujos cérebros exibiam misturas de patologias tendiam a apresentar níveis intermediários dos marcadores, sugerindo que tais painéis podem um dia ajudar a reconhecer doenças mistas em vez de forçar um rótulo binário.
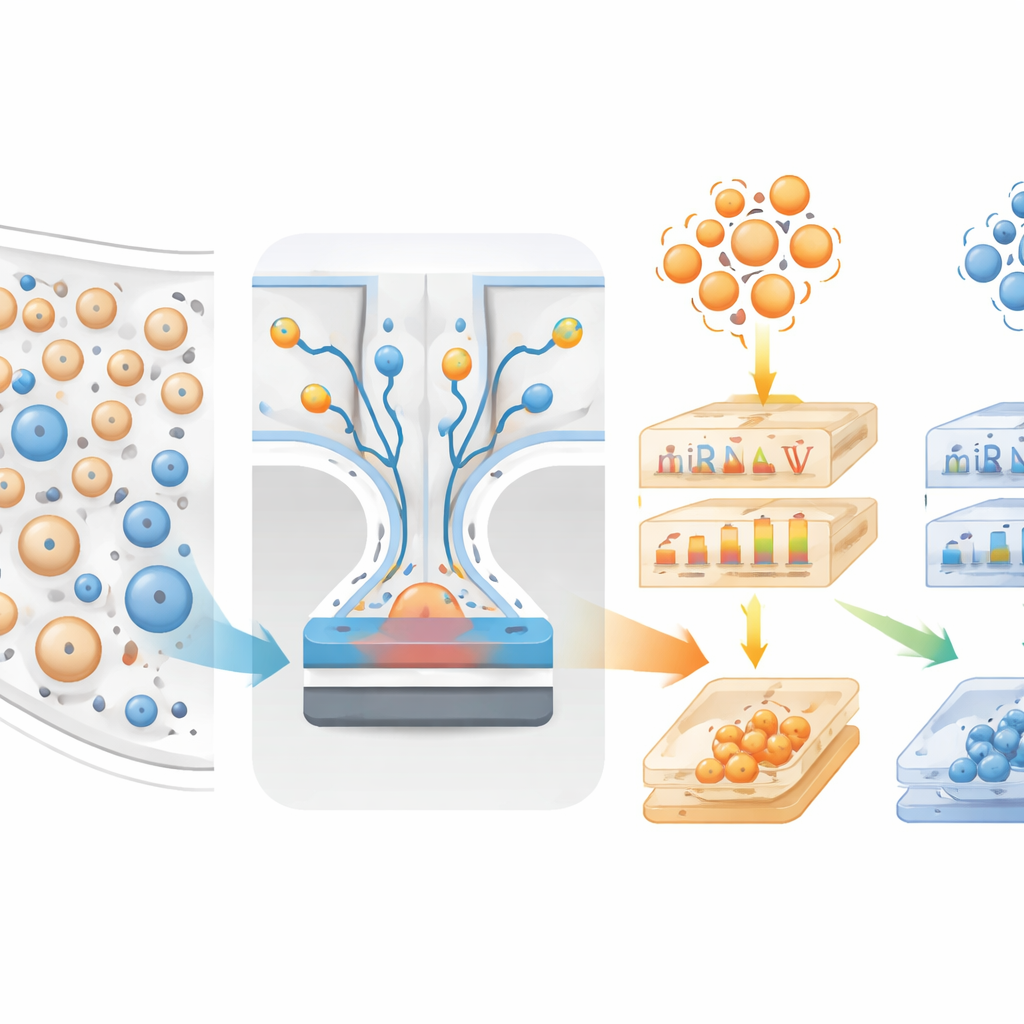
Do prova de conceito ao uso clínico futuro
O estudo é uma demonstração inicial, mas importante, de que vesículas de células cerebrais no sangue podem transportar informações detalhadas suficientes para separar os principais tipos de demência. O trabalho ainda precisa ser confirmado em grupos maiores e mais diversos e em pacientes acompanhados ao longo do tempo, e os autores enfatizam limites atuais para identificar com precisão a célula exata de origem de cada vesícula. Ainda assim, a combinação de um chip magnético escalável e um painel multimarcador cuidadosamente escolhido oferece um roteiro para futuros exames de sangue que poderiam orientar escolhas terapêuticas, melhorar ensaios clínicos e dar às famílias respostas muito mais claras sobre a doença específica por trás da demência de um ente querido.
Citação: Yang, S.J., Lin, A.A., Shen, H. et al. Microfluidic nanomagnetically isolated neuron- and astrocyte-derived extracellular vesicles to differentiate Lewy body and Alzheimer’s disease. npj Biosensing 3, 19 (2026). https://doi.org/10.1038/s44328-026-00086-x
Palavras-chave: vesículas extracelulares, doença de corpos de Lewy, doença de Alzheimer, biomarcadores em sangue, diagnósticos microfluídicos