Clear Sky Science · pt
Detecção multiplexada ponto de atendimento de citocinas usando uma matriz de eletrodos HexaPie para endotipagem da asma
Por que testar asma com saliva pode transformar a atenção domiciliar à saúde
A asma afeta centenas de milhões de pessoas, mas os médicos ainda têm dificuldade em ajustar o tratamento certo para cada paciente. Este estudo apresenta um pequeno sensor eletrônico, chamado HexaPie, capaz de ler sinais imunológicos a partir de uma amostra simples de saliva em vez de sangue. Ao medir simultaneamente várias moléculas relacionadas à inflamação, ele pode, no futuro, permitir que as pessoas monitorem sua asma — e outros problemas imunológicos — de forma rápida e indolor, em casa ou em uma clínica. 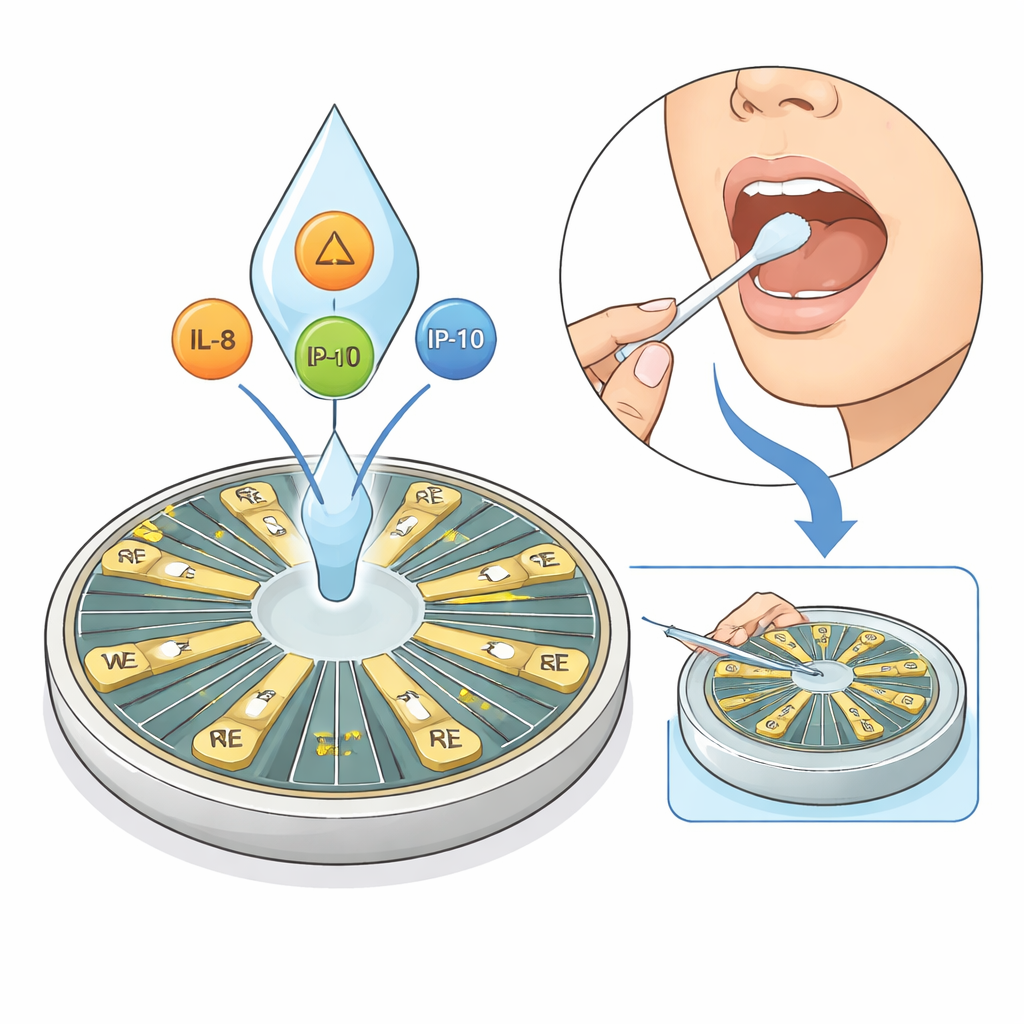
Uma nova forma de escutar o sistema imunológico
A asma não é uma única doença, mas uma coleção de diferentes “tipos” impulsionados por vias imunológicas distintas. Testes tradicionais frequentemente enfocam um marcador por vez e normalmente exigem punções venosas e equipamentos de laboratório centralizados, que são lentos e inconvenientes para checagens frequentes. O sistema HexaPie busca resolver isso detectando três mensageiros imunes-chave na saliva — IL-8, IL-10 e IP-10 — que, em conjunto, delineiam um quadro mais amplo da inflamação das vias aéreas, incluindo formas não eosinofílicas e de difícil tratamento. Como a coleta de saliva é não invasiva e simples, ela se presta bem ao monitoramento repetido fora de grandes hospitais.
Uma pequena matriz de ouro que detecta sem reagentes adicionais
O HexaPie é construído sobre uma placa de circuito impressa personalizada que abriga seis pares de pequenos eletrodos de ouro dispostos como fatias de uma torta. Cada eletrodo de trabalho é revestido com um anticorpo diferente que se liga especificamente a uma das citocinas-alvo, enquanto o eletrodo de referência pareado permanece nu. Em vez de usar corantes ou agentes redox adicionados, o dispositivo se apoia em um método elétrico sem rótulo: quando as citocinas na saliva se ligam aos seus anticorpos, elas reorganizam sutilmente partículas carregadas e água na superfície metálica. Isso altera a dupla camada elétrica — uma região fina bem na interface — e a mudança resultante na impedância elétrica pode ser lida diretamente, permitindo a medição simultânea das três citocinas a partir de uma única e pequena gota.
Testando o projeto por simulações e em laboratório
Antes de fabricar dispositivos completos, a equipe usou simulações computacionais para verificar se a geometria do HexaPie distribuiria campos elétricos e correntes de forma controlada entre cada eletrodo de trabalho e referência. Os modelos mostraram que a tensão aplicada permanece bem confinada perto das regiões sensoriais e que a corrente flui principalmente através das lacunas pretendidas — condições necessárias para leituras estáveis e repetíveis. No laboratório, os pesquisadores então verificaram a química em eletrodos de ouro adicionando cada camada — ligante, anticorpo e antígeno — enquanto acompanhavam sinais eletroquímicos padrões. À medida que mais material biológico cobria a superfície, o fluxo de elétrons diminuiu e a impedância aumentou em passos previsíveis, confirmando que as camadas de anticorpo se formaram corretamente e podiam capturar seus alvos. 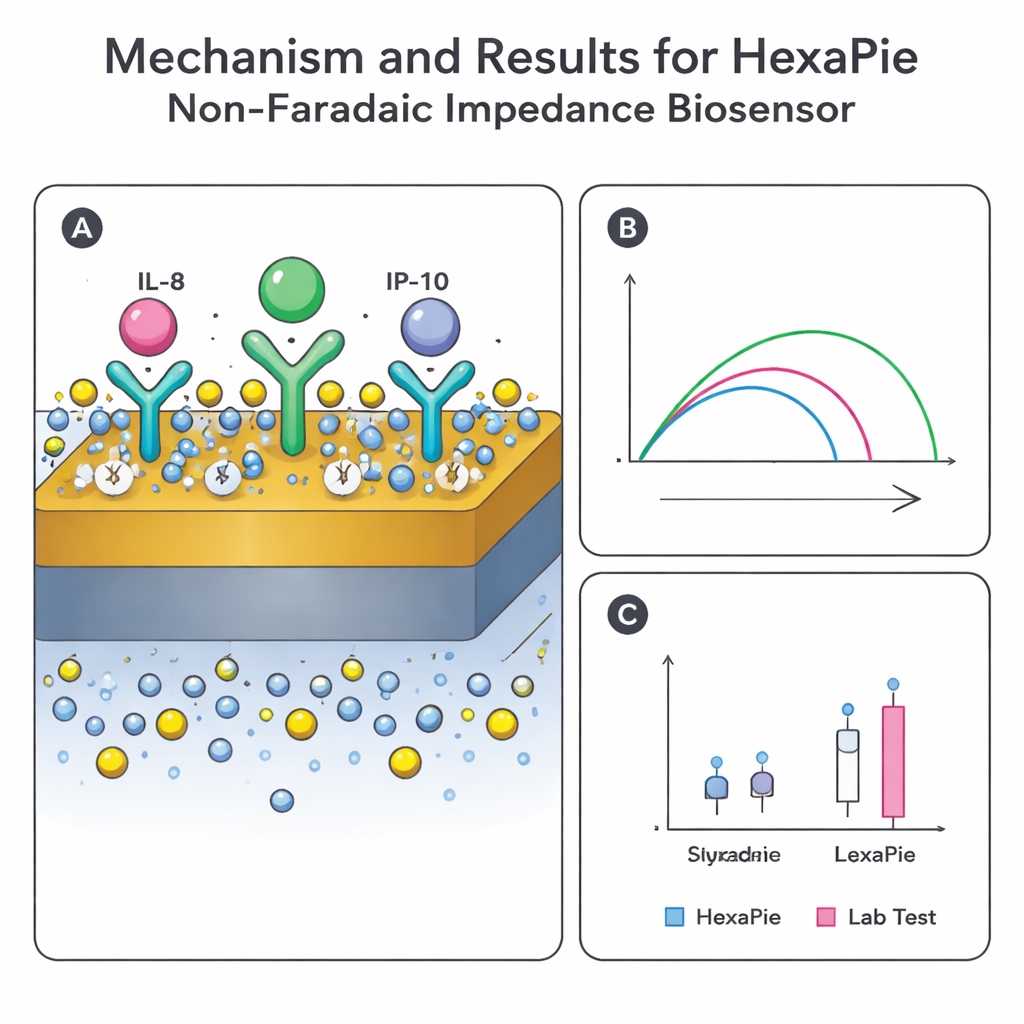
Quão bem o sensor mede amostras reais de saliva
Para avaliar se o HexaPie poderia fornecer números confiáveis na prática, os autores adicionaram quantidades conhecidas das três citocinas em saliva humana agrupada e mediram as mudanças de impedância resultantes. Os sinais mudaram de maneira ordenada e dependente da concentração e, ao ajustar os dados, a equipe construiu curvas de calibração que convertem leituras elétricas em níveis de citocinas. O dispositivo alcançou limites de detecção baixos — até trilionésimos de grama por mililitro para alguns marcadores — dentro das faixas relatadas para pessoas com vias aéreas inflamadas. Medições repetidas no mesmo chip e entre chips diferentes variaram menos de 15%, atendendo aos padrões clínicos aceitos. Quando os pesquisadores adicionaram componentes comuns da saliva, como albumina, ácido úrico e vitamina C, em níveis altos, as respostas do sensor quase não mudaram, indicando que interferentes do dia a dia provavelmente não confundiriam as leituras.
Comparação com testes de padrão hospitalar
O teste final foi comparar o HexaPie com plataformas laboratoriais estabelecidas. Saliva de pessoas com asma (durante crises e em fases estáveis) e de fumantes e não fumantes saudáveis foi analisada em paralelo usando HexaPie, um sistema automatizado de imunoensaio (ELLA) e um teste multiplex baseado em esferas (Luminex). Embora este estudo pequeno não tenha encontrado diferenças claras entre grupos nos níveis de citocinas — provavelmente devido ao timing e ao tamanho da amostra — os valores do novo sensor para IL-8 e IP-10 corresponderam de perto aos obtidos por ambos os métodos de referência, com apenas pequenos desvios médios. A IL-10, que é naturalmente escassa e difícil de medir, mostrou maior discordância entre as plataformas, ressaltando um desafio mais amplo em detectar de forma confiável moléculas de baixa abundância na saliva.
O que isso significa para o cuidado cotidiano
Para não especialistas, a conclusão é que o HexaPie traz medições imunes ao nível de laboratório para um dispositivo compacto e sem reagentes que funciona diretamente com saliva. Ele acompanha de forma confiável aumentos clinicamente relevantes em três citocinas relacionadas à asma sem rótulos ou manipulação complexa da amostra, e suas leituras concordam bem com testes-padrão para duas delas. Embora sejam necessários mais trabalhos para refinar a detecção de IL-10 e validar o sistema em grupos maiores de pacientes, essa tecnologia aponta para um futuro em que pessoas com asma e outras doenças inflamatórias poderiam monitorar seu estado imune de forma rápida e indolor no ponto de atendimento, ajudando médicos a ajustar tratamentos ao perfil imune único de cada pessoa.
Citação: Churcher, N.K.M., Rizvi, F.Z., Qureshi, A. et al. Point-of-care multiplexed detection of cytokines using a HexaPie electrode array for asthma endotyping. npj Biosensing 3, 16 (2026). https://doi.org/10.1038/s44328-026-00081-2
Palavras-chave: monitoramento da asma, biossensor de saliva, detecção de citocinas, diagnóstico ponto de atendimento, impedância eletroquímica