Clear Sky Science · pt
Bioensaio potencializado por plasmons para detecção e quantificação de RNA do SARS-CoV-2 sem amplificação
Por que testes virais mais rápidos e simples importam
A pandemia de COVID-19 mostrou o quanto dependemos de testes laboratoriais que são lentos, caros e difíceis de ampliar quando milhões de pessoas precisam de respostas rápidas. O trabalho descrito aqui apresenta um novo tipo de ensaio laboratorial capaz de detectar e contar quantidades muito pequenas de material genético do coronavírus sem a etapa de amplificação usada no PCR. Essa abordagem busca aproximar a precisão de nível hospitalar de testes simples e de baixo custo que possam ser implantados mais amplamente em surtos futuros.
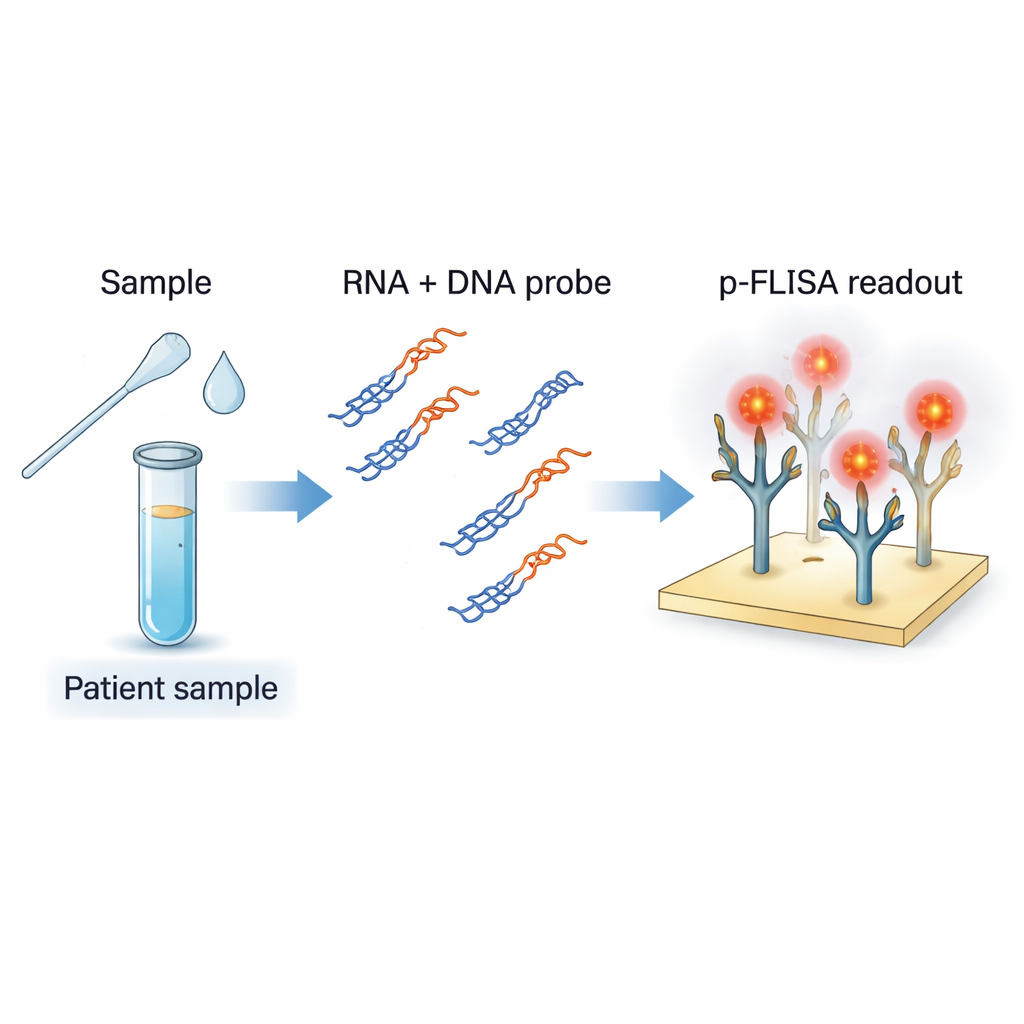
Uma nova maneira de ver rastros genéticos virais
O diagnóstico padrão da COVID-19 usa RT-PCR, que copia muitas vezes fragmentos do RNA viral para que possam ser detectados. Embora muito sensível, o PCR exige equipamentos complexos, pessoal treinado e tempo, e geralmente fornece uma resposta “sim ou não” em vez de uma carga viral precisa. Os autores propuseram construir um ensaio que funcione mais como uma versão altamente aprimorada de um teste ELISA de sangue: um formato simples em placa, porém ajustado para detectar RNA viral diretamente e quantificar sua quantidade. O método tem como alvo o RNA do SARS-CoV-2 em amostras como swabs nasais e saliva, mas foi projetado para ser facilmente adaptado a outros vírus de RNA.
Transformando RNA em um alvo capturável
A equipe usa pequenos trechos de DNA projetados para corresponder a regiões específicas do genoma do SARS-CoV-2. Quando misturados com RNA extraído de uma amostra do paciente e aquecidos e resfriados suavemente, essas sondas de DNA emparelham-se com qualquer RNA viral correspondente para formar híbridos DNA–RNA, como um pequeno zíper com uma fita de RNA e uma de DNA. Um anticorpo especial chamado S9.6 atua como o capturador: reconhece e se liga firmemente a esses híbridos, mas não ao DNA simples ou duplo comum nem a RNA não relacionado. Ao revestir o fundo de uma placa com S9.6, o ensaio captura seletivamente apenas aqueles híbridos que contêm as sequências genéticas de interesse do vírus, filtrando o restante da bagunça genética da amostra.
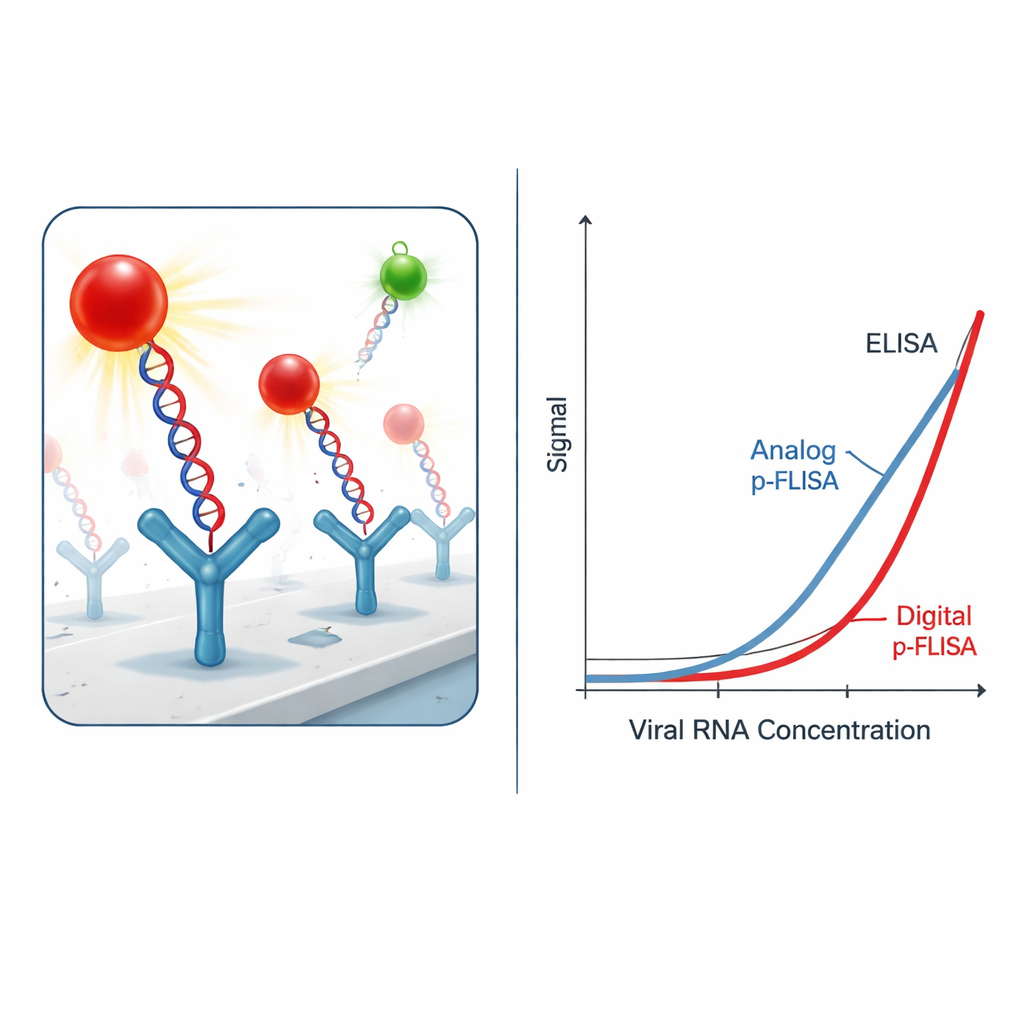
Tornando o sinal ultrabrilhante
Capturar os híbridos virais não basta; o desafio é enxergá-los acima do ruído de fundo. Em vez de corantes fluorescentes convencionais, os pesquisadores usam nanorótulos “plasmonic-fluor”—nanopartículas projetadas que atuam como pequenas antenas para a luz. Cada rótulo combina um nanorretângulo metálico com múltiplas moléculas fluorescentes e um revestimento que permite que ele se ligue a marcas de biotina no DNA ou no anticorpo. Esses rótulos plasmônicos emitem luz mais de mil vezes mais brilhante do que corantes padrão nas mesmas condições. Na prática, isso significa que são necessários muito menos híbridos virais para produzir um brilho detectável, melhorando dramaticamente a sensibilidade do teste e reduzindo a concentração mínima de RNA viral que pode ser medida.
Do brilho analógico à contagem digital
Na sua forma “analógica” mais simples, o ensaio mede o brilho total de cada poço da placa, muito parecido com um teste fluorescente clássico. Mesmo nesse modo, o sistema potencializado por plasmons melhora o limite de detecção e o nível mais baixo quantificável de RNA do SARS-CoV-2 em uma a três ordens de magnitude em comparação com um ELISA tradicional usando enzimas ou fluoróforos padrão. Os autores foram além ao mudar para um formato “digital”: em vez de fazer a média da luz em todo o poço, eles imageiam a superfície com um microscópio de fluorescência e contam nanorótulos individuais brilhantes usando um software de análise de imagem personalizado. Essa abordagem de contagem de partículas únicas proporciona um ganho adicional de sensibilidade de dez a trinta vezes, resultando em limites de detecção cerca de 2.300 vezes melhores e limites de quantificação aproximadamente 460 vezes melhores que os do ELISA globalmente.
Aplicando o teste em amostras reais
Para avaliar se o método se mantém além das misturas controladas de laboratório, os pesquisadores testaram RNA extraído de swabs nasais e saliva de pacientes com COVID-19, incluindo infecções por variantes como alfa/beta e delta, além de amostras de pessoas com outros vírus respiratórios. O ensaio potencializado por plasmons detectou RNA do SARS-CoV-2 em todas as amostras PCR-positivas, sem sinal acima do ruído de fundo em amostras PCR-negativas ou contendo outros vírus, indicando excelente sensibilidade e especificidade clínicas comparáveis ao RT-PCR. Além disso, as concentrações de RNA medidas mostraram uma relação inversa com os valores de limiar de ciclo do PCR: amostras que precisaram de menos ciclos de PCR (indicando maior carga viral) apresentaram níveis de RNA mais altos pelo novo ensaio, consistente com expectativas biológicas e sugerindo que ele pode fornecer informações quantitativas significativas sobre a carga viral.
O que isso pode significar para surtos futuros
Para não especialistas, a mensagem principal é que esse ensaio oferece uma maneira de medir quanto vírus está presente sem a etapa extra de cópia que torna o PCR lento e dependente de equipamentos. Ao combinar um anticorpo seletivo para híbridos RNA–DNA com fontes de luz nanoscalas ultrabrilhantes e contagem digital, o método aproxima-se do desempenho do PCR mantendo um fluxo de trabalho simples baseado em placas. Com validação e engenharia adicionais, tais ensaios potencializados por plasmons poderiam ser adaptados a muitos alvos de RNA e possivelmente convertidos em formatos rápidos de ponto de atendimento, ajudando clínicos não só a diagnosticar infecções, mas também a avaliar o estágio da doença e a contagiosidade a partir de uma medida absoluta de RNA viral.
Citação: Liu, L., Seth, A., Liu, Y. et al. Plasmon-enhanced bioassay for amplification-free detection and quantification of SARS-CoV-2 RNA. npj Biosensing 3, 13 (2026). https://doi.org/10.1038/s44328-026-00078-x
Palavras-chave: detecção de RNA do SARS-CoV-2, nanorótulos plasmônicos, imunoensaio digital, diagnósticos sem amplificação, quantificação da carga viral