Clear Sky Science · pt
Um biossensor microfluídico baseado em micro-órgãos para monitoramento contínuo de níveis de glicose in vivo
Por que isso importa para pessoas com diabetes
Para pessoas que vivem com diabetes tipo 1, os sistemas atuais de “pâncreas artificial” ainda exigem atenção constante — anunciar refeições, lidar com alarmes e preocupar-se com hipoglicemia noturna. Este estudo explora um tipo radicalmente diferente de sensor de glicose que não depende de uma única enzima ou de uma equação computacional, mas que em vez disso recorre a um pequeno pedaço vivo da própria maquinaria corporal de controle do açúcar: aglomerados de células pancreáticas chamados ilhotas. Ao deixar que esses mini-órgãos façam aquilo para o qual a evolução os otimizou, os pesquisadores buscam construir monitores de glicose mais inteligentes e seguros, que um dia poderiam operar de forma mais independente em segundo plano.
Um pequeno órgão como sensor vivo
A maioria dos biossensores atuais detecta substâncias químicas usando moléculas purificadas ou linhas celulares únicas. Eles respondem a um único composto específico e então transmitem o sinal bruto para um software que tenta interpretá-lo. Os autores argumentam que essa abordagem ignora um “computador” embutido e poderoso: micro-órgãos, como as ilhotas pancreáticas, que naturalmente detectam muitos sinais ao mesmo tempo e os convertem em uma resposta coordenada. Cada ilhota contém vários tipos celulares produtores de hormônios que constantemente se comunicam entre si. Juntas, elas mantêm a glicemia dentro de uma faixa estreita e segura, reagindo não apenas à glicose, mas também a aminoácidos, hormônios intestinais e do estresse, e ao histórico recente do corpo de picos e quedas. Essa complexidade intrínseca, sugerem, poderia ser aproveitada para produzir informações mais ricas e confiáveis do que um simples sensor de glicose oxidase.
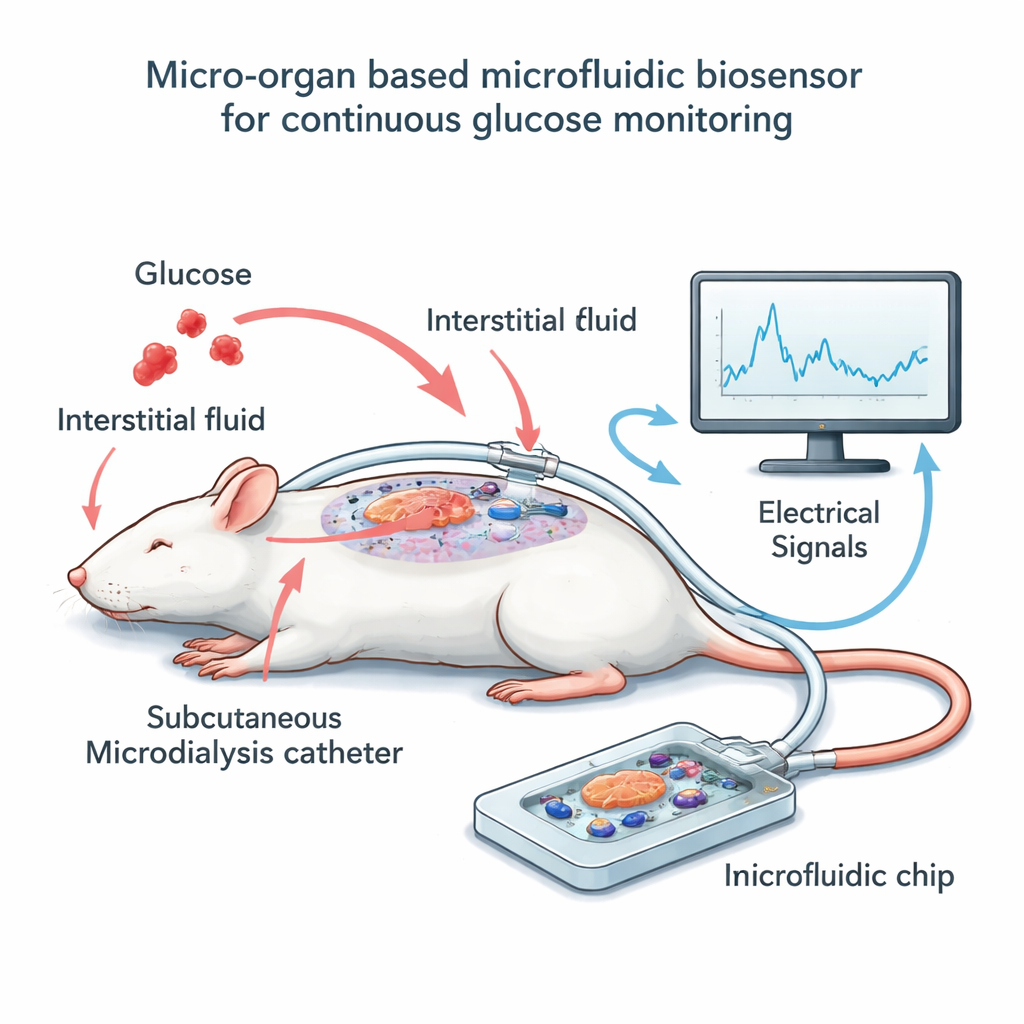
Construindo o sistema chip-e-cateter
Para testar essa ideia, a equipe construiu um pequeno dispositivo fora do corpo que abriga algumas dezenas de ilhotas de camundongo sobre uma grade de eletrodos microscópicos. Em vez de banhar essas células diretamente no sangue, usaram uma técnica chamada microdiálise: um cateter fino e flexível fica logo abaixo da pele de ratos anestesiados e coleta lentamente o fluido tecidual ao redor, que acompanha de perto a glicemia, embora com um pequeno atraso. Um fluxo baixo e constante carrega esse fluido por um canal estreito sobre as ilhotas no chip. À medida que os níveis de glicose no dialisado sobem e descem, as ilhotas mudam sua atividade elétrica, que os eletrodos capturam como sinais lentos em forma de onda. Em paralelo, os pesquisadores mediram periodicamente a glicose no sangue dos ratos e no dialisado, permitindo alinhar a leitura elétrica com os níveis reais de açúcar ao longo do tempo.
Como o sensor vivo respondeu às variações de açúcar
Primeiro, os cientistas testaram se as ilhotas sobre os eletrodos podiam responder a componentes sanguíneos reais em vez de soluções simples de laboratório. Exporam-nas a soro humano e de rato com diferentes níveis de glicose e observaram mudanças claras e graduais tanto na frequência quanto no tamanho de suas ondas elétricas. As respostas foram suficientemente fortes para distinguir pequenos passos na concentração de açúcar na faixa relevante para diabetes. Em seguida, passaram para experimentos em ratos, administrando uma injeção de glicose para elevar a glicemia e, mais tarde, injetando insulina para reduzi-la. Após levar em conta o tempo que a glicose leva para passar do sangue para o fluido tecidual e através da tubulação, descobriram que a frequência dos sinais elétricos lentos das ilhotas subia e descia quase em sincronia com a glicemia. Análises estatísticas em vários animais mostraram uma relação notavelmente estreita e repetível entre a frequência do sinal e o nível de glicose, enquanto a amplitude do sinal, embora informativa, foi um tanto mais variável.
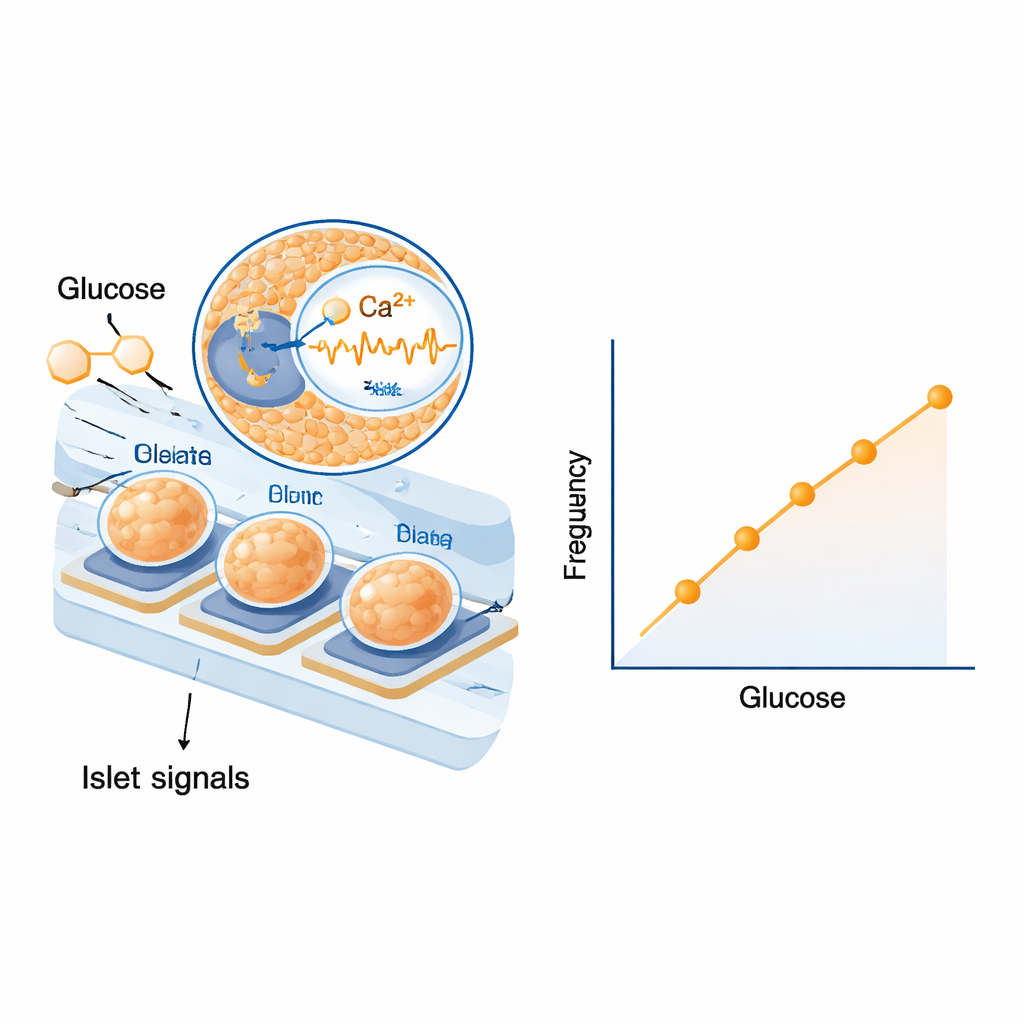
Recursos de segurança incorporados pela biologia
Uma vantagem importante de usar ilhotas inteiras, em vez de uma única molécula, é que seu comportamento já inclui mecanismos de segurança moldados pela evolução. Trabalhos anteriores, e indícios deste estudo, mostram que as ilhotas reagem mais fortemente quando a glicose está caindo do que quando está subindo — uma forma de “histerese” que ajuda a proteger contra hipoglicemia perigosa. Os padrões elétricos também são moldados por tipos celulares vizinhos que amplificam ou amortecem a liberação de insulina dependendo das necessidades do corpo. Como o chip simplesmente escuta esses sinais integrados sem adicionar corantes ou modificações genéticas, ele pode registrar por dias sem prejudicar as células. Os autores notam desafios técnicos a seguir, como evitar bolhas de ar, garantir desempenho de microdiálise a longo prazo e decidir qual tipo de ilhotas humanas ou derivadas de células-tronco deveria ser usado eventualmente. Ainda assim, simulações computacionais usando um modelo estabelecido de diabetes sugerem que um sensor baseado em ilhotas poderia igualar ou até superar os monitores de glicose atuais em condições difíceis.
O que isso pode significar para o cuidado futuro do diabetes
Este trabalho mostra que um punhado de micro-órgãos pancreáticos, mantidos vivos em um pequeno chip e conectados ao corpo por um cateter fino, pode rastrear a glicemia continuamente em animais vivos por meio de sua conversa elétrica natural. Para um público não especializado, a mensagem principal é que, em vez de pedir a um sensor químico simples que meça glicose e depois forçar um computador a adivinhar o que isso significa para o corpo, essa abordagem escuta diretamente o mesmo tipo de tecido vivo que normalmente decide quanta insulina liberar. Se refinados e tornados práticos para uso humano, esses biossensores vivos poderiam se tornar o núcleo de sistemas verdadeiramente autônomos de pâncreas artificial — dispositivos que antecipam silenciosamente as necessidades do corpo e reduzem o ônus diário do manejo do diabetes.
Citação: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
Palavras-chave: monitoramento contínuo de glicose, pâncreas artificial, ilhotas pancreáticas, biossensor microfluídico, diabetes tipo 1