Clear Sky Science · pt
Imagem multimodal correlativa para mapeamento espacial em microescala das interações entre colágeno e atividade gênica em tecidos humanos
Por que olhar dentro dos músculos importa
Doenças que cicatrizam lentamente nossos órgãos, como a distrofia muscular de Duchenne (DMD), se desenrolam em escalas pequenas demais para o olho nu. A atividade gênica ocorre dentro de células individuais, enquanto o tecido de sustentação ao redor delas é formado por minúsculos filamentos proteicos. Até agora, cientistas raramente conseguiram ver esses dois mundos juntos numa mesma lâmina de tecido humano. Este estudo apresenta uma forma de fazer exatamente isso, revelando como as mensagens dos genes e a estrutura de suporte do corpo interagem em microescala.
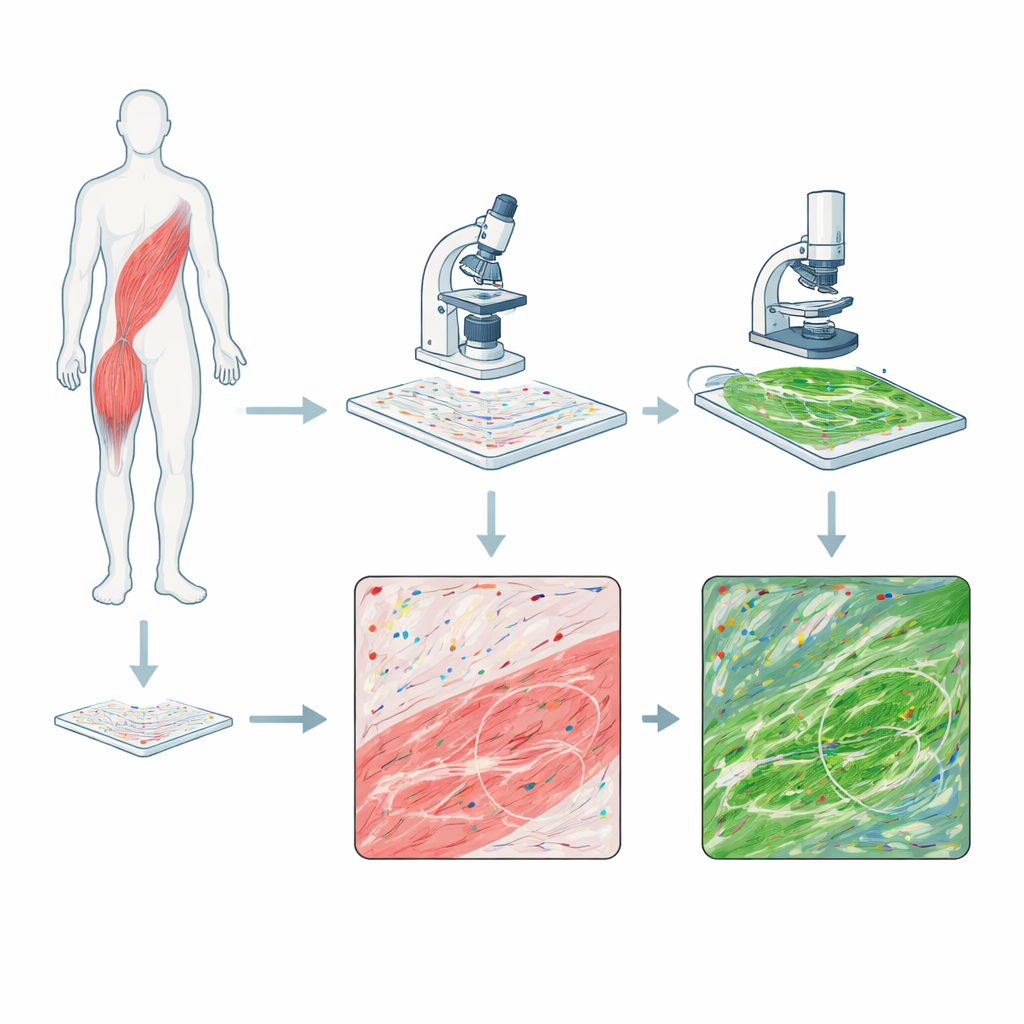
Duas câmeras na mesma peça de tecido
Os pesquisadores combinaram dois métodos de imagem poderosos em cortes únicos de biópsias de músculo esquelético humano de pessoas com DMD e de um voluntário saudável. Um método, chamado RNAscope, cora moléculas individuais de RNA — as cópias funcionais dos genes — como pontos coloridos, mostrando onde mensagens genéticas específicas estão presentes. O segundo método, microscopia multiphoton, usa luz de laser para fazer os filamentos de colágeno do tecido fluorescerem sem corante adicional, capturando a arquitetura do tecido conjuntivo que se espessa durante a cicatrização e a fibrose. Ao imagear primeiro os sinais de RNA e depois os sinais de colágeno na mesma lâmina exata, eles puderam alinhar as duas imagens de modo que cada ponto de atividade gênica fosse comparado com a rede de fibras ao redor, pixel por pixel.
O que as visões separadas já nos dizem
Analisar cada método de imagem isoladamente já destacou diferenças claras entre músculo doente e saudável. O RNAscope mostrou que músculos dos pacientes com DMD continham menos transcritos de distrofina — as mensagens de RNA necessárias para produzir a proteína distrofina ausente — do que a amostra saudável. Os sinais remanescentes também diferiram em tamanho dependendo de qual parte do gene foi alvo, sugerindo diferenças em como a longa mensagem da distrofina é processada. Enquanto isso, as imagens multiphoton mostraram que músculos com DMD estavam repletos de fibras de colágeno longas e densas, um sinal visual de cicatrização fibrótica, enquanto o músculo saudável apresentava menos fibras, mais distribuídas de forma uniforme. Essas descobertas coincidem com a experiência clínica: na DMD, o tecido muscular é gradualmente substituído por gordura e cicatriz.
Ampliando o campo: padrões amplos através do tecido
Após registrar digitalmente os dois tipos de imagem, a equipe dividiu cada seção de tecido em uma grade, tratando cada quadrado como uma pequena vizinhança. Em cada quadrado eles mediram tanto características do colágeno — comprimento das fibras, orientação e quão sinuosas ou retas eram — quanto a densidade local de pontos de RNA de distrofina. Essa visão em “mapa de calor” revelou variação em manchas, de região para região, tanto na atividade gênica quanto na estrutura do colágeno dentro do músculo com DMD. No entanto, quando essas medidas foram comparadas usando testes estatísticos, a abundância de transcritos e as propriedades do colágeno mostraram quase nenhuma relação consistente nessa escala grosseira. Em outras palavras, ao se fazer médias sobre regiões relativamente grandes, áreas ricas em RNA de distrofina não eram de forma confiável mais ou menos fibróticas do que áreas com menos sinais de RNA.
Ampliando o zoom: relações na escala celular
Os resultados mais reveladores surgiram quando os cientistas focaram em vizinhanças medidas em apenas algumas dezenas de micrômetros — aproximadamente o tamanho de fibras musculares individuais e suas imediações imediatas. Para cada ponto de RNA, eles desenharam uma série de círculos crescentes e perguntaram quantas fibras de colágeno estavam dentro e qual era o comprimento dessas fibras. Tanto nos tecidos com DMD quanto nos saudáveis, as fibras de colágeno eram mais longas bem próximas aos sinais de RNA de distrofina e ficavam progressivamente mais curtas à medida que se afastavam. Nas amostras mais severamente cicatrizadas, os pontos de transcritos quase sempre tinham colágeno nas proximidades, mesmo em distâncias muito pequenas, enquanto na amostra saudável muitos pontos de RNA estavam em regiões com pouco ou nenhum colágeno próximo. Análises de controle usando pontos colocados aleatoriamente e configurações de processamento de imagem ligeiramente alteradas mostraram que esse padrão não podia ser explicado simplesmente pelo acaso ou por peculiaridades do software.
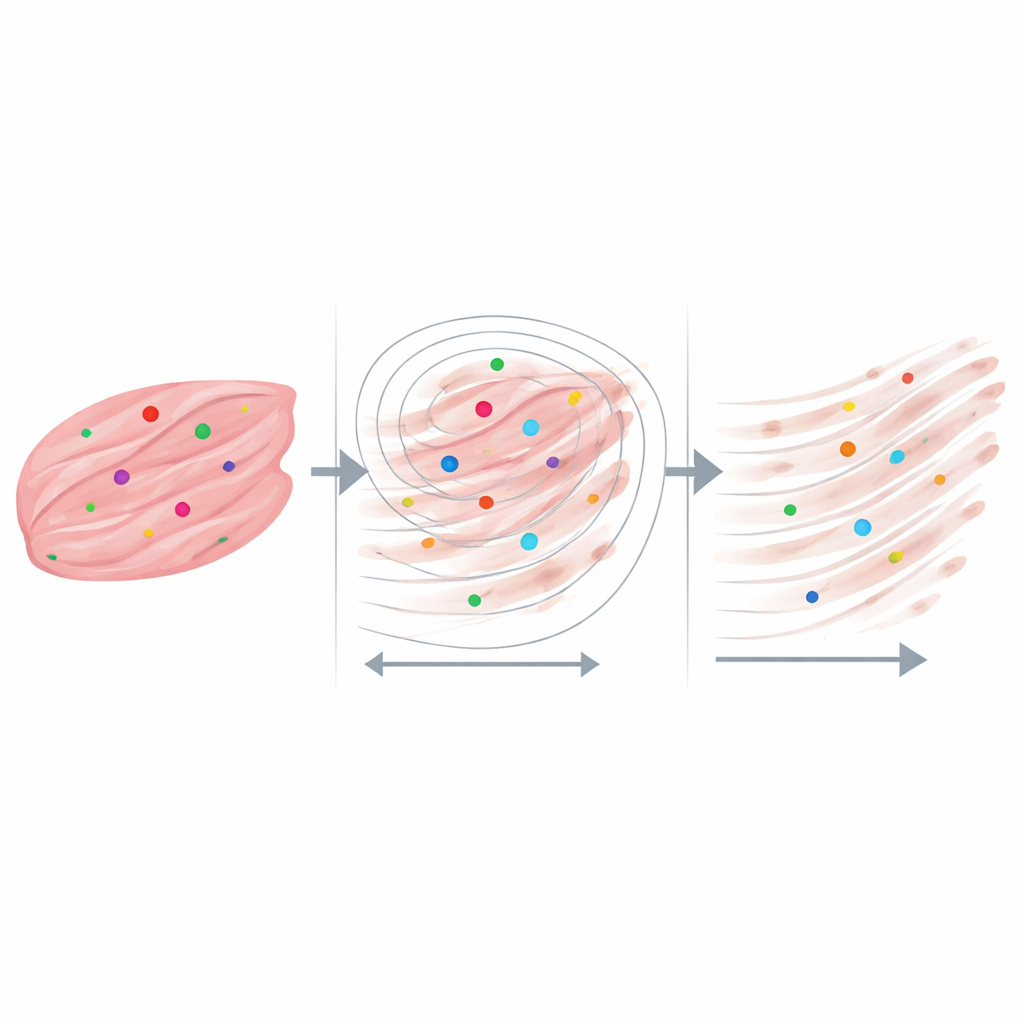
O que isso pode significar para doenças musculares e além
Essas descobertas sugerem que vínculos importantes entre mensagens gênicas e estrutura do tecido podem ficar ocultos quando se observam apenas médias amplas, mas tornam‑se visíveis quando examinados em nível celular. Neste estudo de prova de conceito, regiões enriquecidas em transcritos específicos de distrofina tenderam a ficar próximas de fibras de colágeno mais longas e densas, sugerindo que a atividade gênica local e a remodelação fibrótica podem influenciar uma à outra dentro de microambientes diminutos do músculo. Os autores enfatizam que o grupo de pacientes é pequeno e o trabalho ainda não é um teste clínico. Em vez disso, apresentam uma plataforma flexível que pode ser estendida a outros genes, tipos de tecido e métodos de imagem. Ao conectar onde os genes estão ativos e como a estrutura do tecido é construída, essa abordagem abre a porta para descobrir novos biomarcadores espaciais de fibrose, regeneração e respostas a terapias emergentes baseadas em RNA.
Citação: Scodellaro, R., Mietto, M., Ferlini, A. et al. Correlative multimodal imaging for microscale spatial mapping of collagen-gene activity interactions in human tissues. npj Imaging 4, 17 (2026). https://doi.org/10.1038/s44303-026-00149-8
Palavras-chave: imagem multimodal, distrofia muscular de Duchenne, fibrose por colágeno, expressão gênica espacial, biópsia de músculo esquelético