Clear Sky Science · pt
Uma estratégia de radiomarcação em etapa única para PET, SPECT e radionuclídeos terapêuticos usando nanopartículas como quelante universal
Por que partículas radioativas minúsculas importam
O cuidado moderno do câncer depende cada vez mais de ver e tratar tumores com fármacos radioativos que os iluminam em exames e, em alguns casos, os destroem internamente. Ainda assim, construir cada novo medicamento radioativo é um processo demorado e delicado, porque a maioria dos projetos precisa ser feita sob medida para um metal radioativo específico. Este estudo explora uma abordagem bem diferente: usar um único tipo de nanopartícula à base de ferro como um “encaixe universal” capaz de acomodar muitos isótopos médicos distintos para imagem e terapia, potencialmente acelerando a criação e o ajuste fino desses fármacos.
De muitas chaves para uma única fechadura
Os fármacos radioativos atuais normalmente dependem de garras químicas chamadas quelantes, que prendem átomos metálicos e os ligam a anticorpos ou outros vetores de direcionamento. Cada metal radioativo tende a exigir seu próprio quelante e sua própria receita — condições como temperatura, acidez e tempo de reação mudam conforme o caso. Para alguns metais de importância médica, especialmente os usados em terapias potentes com partículas alfa, ainda não existe um quelante ideal. Os autores argumentam que essa abordagem metal‑a‑metal virou um gargalo: a lista de isótopos úteis continua a crescer, mas a química para manuseá‑los com segurança não consegue acompanhar.
Nanopartículas como um encaixe universal
Para enfrentar esse desafio, os pesquisadores recorreram a nanopartículas de óxido de ferro muito pequenas, um material já estudado como agente de contraste para ressonância magnética. Eles projetaram partículas com um núcleo de óxido de ferro de cerca de três nanômetros de diâmetro, envolvido por um revestimento de citrato que as mantém estáveis na corrente sanguínea. Durante uma única etapa de síntese assistida por micro‑ondas de 10 minutos, doparam o núcleo com um de dez metais radioativos diferentes, comumente usados em exames de PET, SPECT ou em radioterapia interna. Esse processo em uma única etapa produziu partículas de tamanho consistente com altos rendimentos e, crucialmente, excelente estabilidade em soro humano — mesmo para isótopos terapêuticos desafiadores como rádon‑223 e actínio‑225, cujos produtos de decaimento frequentemente escapam dos quelantes tradicionais.
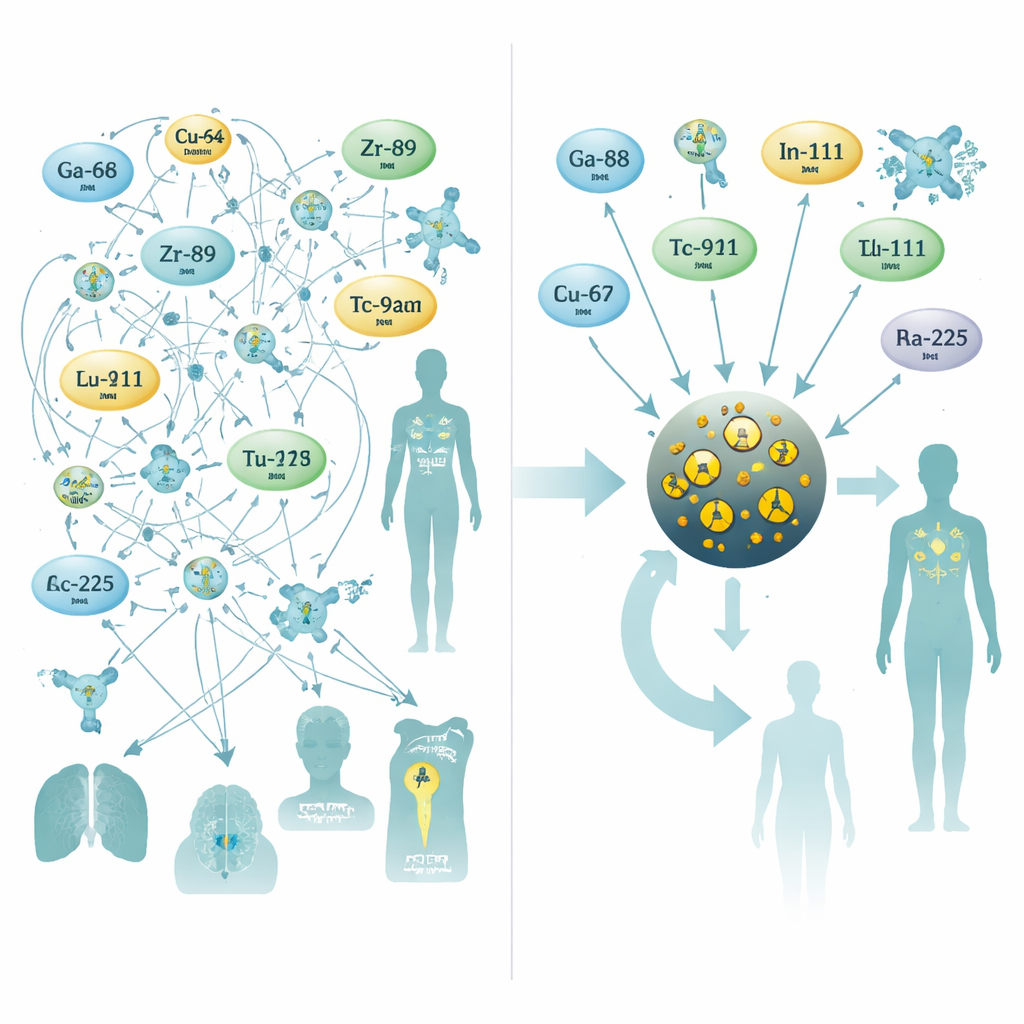
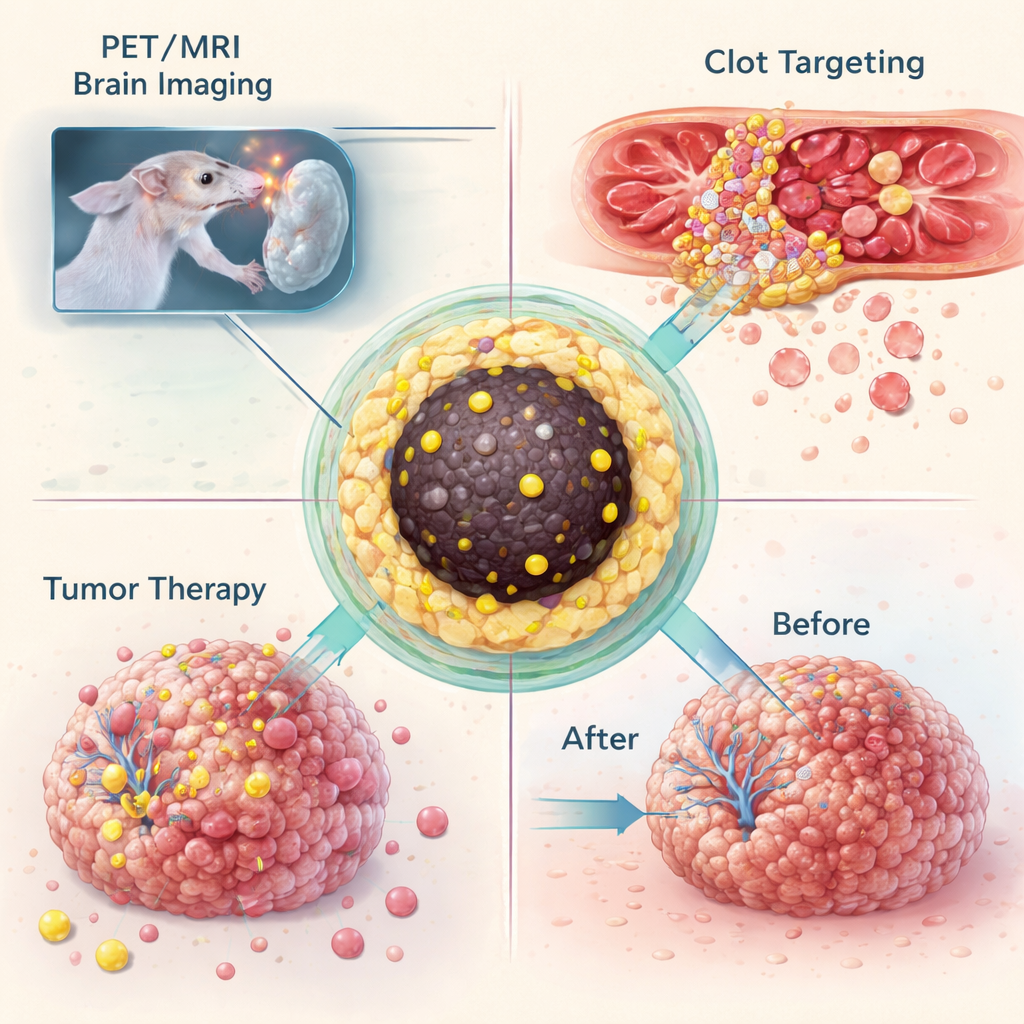
Imagem de coágulos e tumores cerebrais
Tendo demonstrado que podiam aprisionar muitos isótopos diferentes no mesmo desenho de nanopartícula, a equipe testou o que esses “nanotraçadores” conseguem fazer em animais vivos. Em um modelo murino de glioblastoma, um tumor cerebral letal, partículas marcadas com gálio‑68 foram injetadas na corrente sanguínea e imageadas com PET combinado à RM. As partículas se acumularam em tumores grandes o suficiente para comprometer a barreira hematoencefálica, permitindo que a mesma formulação proporcionasse tanto contraste brilhante em RM quanto um sinal sensível em PET. Em um experimento separado, as partículas foram modificadas quimicamente para que pudessem se ligar, por meio de uma reação click altamente seletiva, a um anticorpo que se direciona a plaquetas ativadas dentro de coágulos sanguíneos. Em camundongos com lesão na artéria carótida, essa estratégia de "pré‑alvo" em duas etapas produziu sinais PET claros no local do coágulo, enquanto os animais controle não exibiram esse ponto quente.
Do diagnóstico ao tratamento e eliminação mais segura
A mesma plataforma também foi usada para entregar tratamento. Quando nanopartículas carregadas com lutécio‑177 foram injetadas diretamente em tumores de glioblastoma em camundongos, as partículas permaneceram em grande parte confinadas à massa tumoral por pelo menos duas semanas. Nesse período, tumores não tratados cresceram para várias vezes seu tamanho inicial, enquanto os tumores tratados deixaram de crescer, sugerindo que a dose de radiação localizada foi suficiente para interromper a progressão. Reconhecendo que tratamentos repetidos poderiam sobrecarregar fígado e baço com ferro, a equipe ajustou as condições de síntese para produzir partículas ainda menores — em torno de quatro a cinco nanômetros — que são pequenas o suficiente para serem filtradas pelos rins. Essas partículas reduzidas ainda retiveram com segurança sua carga radioativa, mas foram rapidamente excretadas para a bexiga, reduzindo o acúmulo de longo prazo em órgãos importantes.
O que isso pode significar para o cuidado do câncer no futuro
Para não‑especialistas, a mensagem-chave é que os pesquisadores construíram uma plataforma única e flexível de nanopartículas que pode ser combinada com muitos metais radioativos diferentes sem precisar reinventar a química a cada vez. Em modelos animais, a mesma partícula básica pode ajudar a detectar tumores cerebrais, destacar coágulos sanguíneos, entregar radiação diretamente em tumores e até ser ajustada para sair do corpo pelos rins. Embora sejam necessários mais estudos antes que essa abordagem chegue a pacientes, ela oferece uma rota promissora para projetar famílias de agentes diagnósticos e terapêuticos que compartilham o mesmo comportamento no corpo, diferenciando‑se apenas pelo tipo de radiação que carregam. Essa consistência pode simplificar o desenvolvimento, melhorar os testes de segurança e, em última instância, tornar ferramentas avançadas de medicina nuclear mais amplamente disponíveis.
Citação: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
Palavras-chave: radioteranóstica, nanopartículas, imagem por PET, glioblastoma, radioterapia dirigida