Clear Sky Science · pt
Sinucleinopatia acelerada e localizada em um modelo híbrido de camundongo: implicações para estudos por tomografia por emissão de pósitrons
Por que esta pesquisa é importante
A doença de Parkinson é mais conhecida por tremores e problemas de movimento, mas, no interior do cérebro, ela começa com pequenas alterações difíceis de detectar. Médicos precisam com urgência de maneiras de identificar essas mudanças precocemente e testar novos fármacos rapidamente. Este estudo descreve um modelo refinado de camundongo que reproduz características-chave do dano cerebral semelhante ao da doença de Parkinson em apenas algumas semanas e em uma região cerebral muito específica, adaptado para uso com exames cerebrais avançados chamados de imagem por PET. 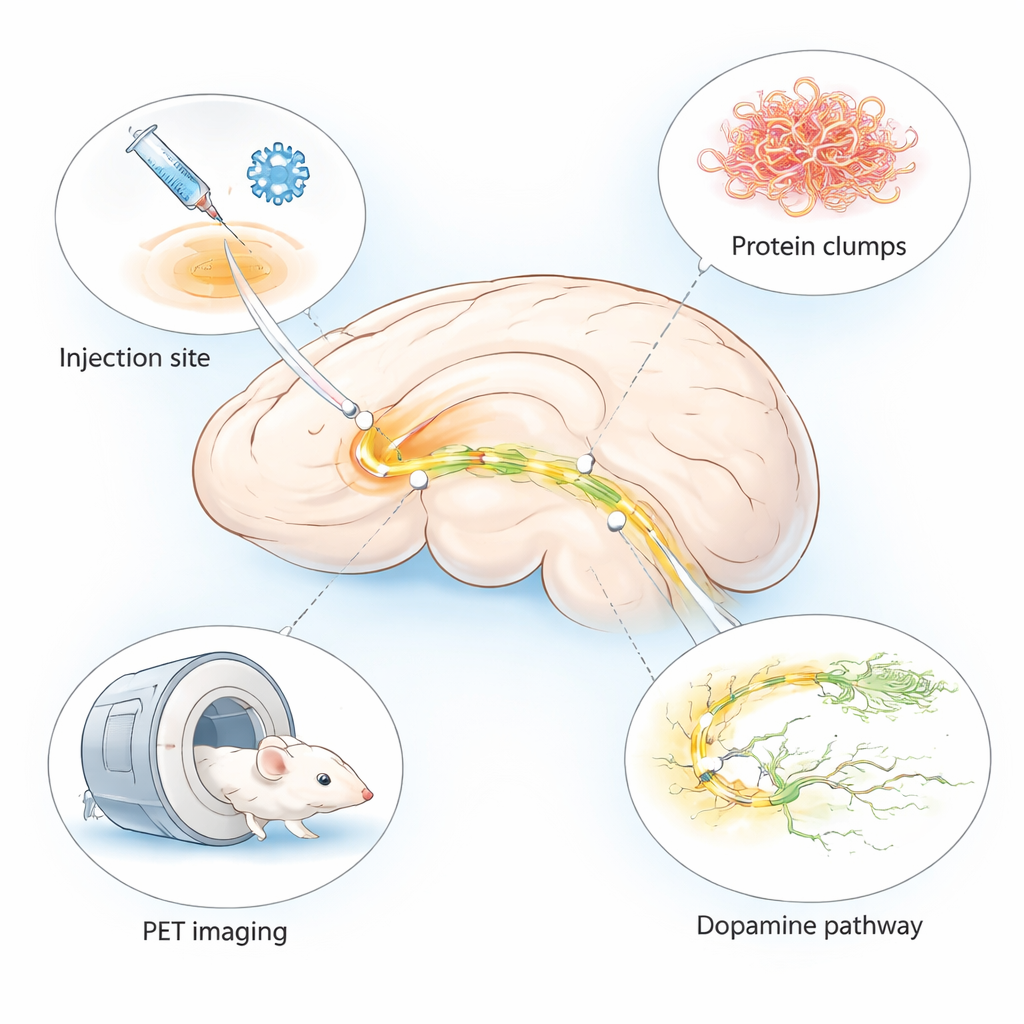
Construindo um modelo de doença mais rápido e focado
Muitos modelos animais existentes da doença de Parkinson levam meses para desenvolver sintomas ou deixam de mostrar toda a gama de alterações cerebrais observadas em pacientes. Os autores combinaram duas abordagens estabelecidas em um único modelo “híbrido”. Eles injetaram um vírus inofensivo que faz com que células cerebrais produzam alfa‑sinucleína humana — uma proteína que forma agregados na doença de Parkinson — juntamente com fibrilas pré‑formadas, que atuam como sementes que disparam a agregação adicional. Ambos foram administrados em uma pequena região relacionada ao movimento, chamada substância negra, de um lado do cérebro do camundongo. Esse desenho produz alterações intensas e localizadas semelhantes à doença no lado injetado, enquanto o outro lado permanece relativamente saudável para comparação.
Acompanhando agregados proteicos e morte de neurônios
Em apenas duas semanas após a injeção, os camundongos apresentaram níveis elevados de alfa‑sinucleína humana e de sua forma anormal fosforilada na área cerebral alvo. Ao microscópio, os pesquisadores observaram estruturas que lembram os corpos de Lewy e os neuritos de Lewy, marcas registradas da doença de Parkinson. Nas semanas seguintes, esses depósitos anormais aumentaram. Ao mesmo tempo, neurônios produtores do mensageiro químico dopamina — crucial para movimentos suaves — começaram a desaparecer. Marcadores dessas células caíram para aproximadamente 60% do nível observado no lado não tocado até a quinta semana, confirmando uma perda progressiva clara do sistema dopaminérgico.
Inflamação, sinapses em declínio e usinas de energia fatigadas
As células imunes do cérebro, chamadas microglia, também passaram para um estado altamente ativo e inflamatório ao redor da região danificada. Colorações para várias proteínas relacionadas à inflamação foram muito mais intensas próximas aos depósitos de alfa‑sinucleína do que no lado oposto do cérebro. Mais tarde no processo, a equipe detectou perda de sinapses — os pequenos pontos de contato onde os neurônios se comunicam — e sinais de que as mitocôndrias, as usinas de energia das células, não estavam funcionando corretamente. Juntos, esses achados mostram que o modelo não apenas gera agregados proteicos; ele também captura a reação em cadeia de inflamação, falha nas conexões e problemas energéticos que contribuem para a morte neuronal na doença de Parkinson. 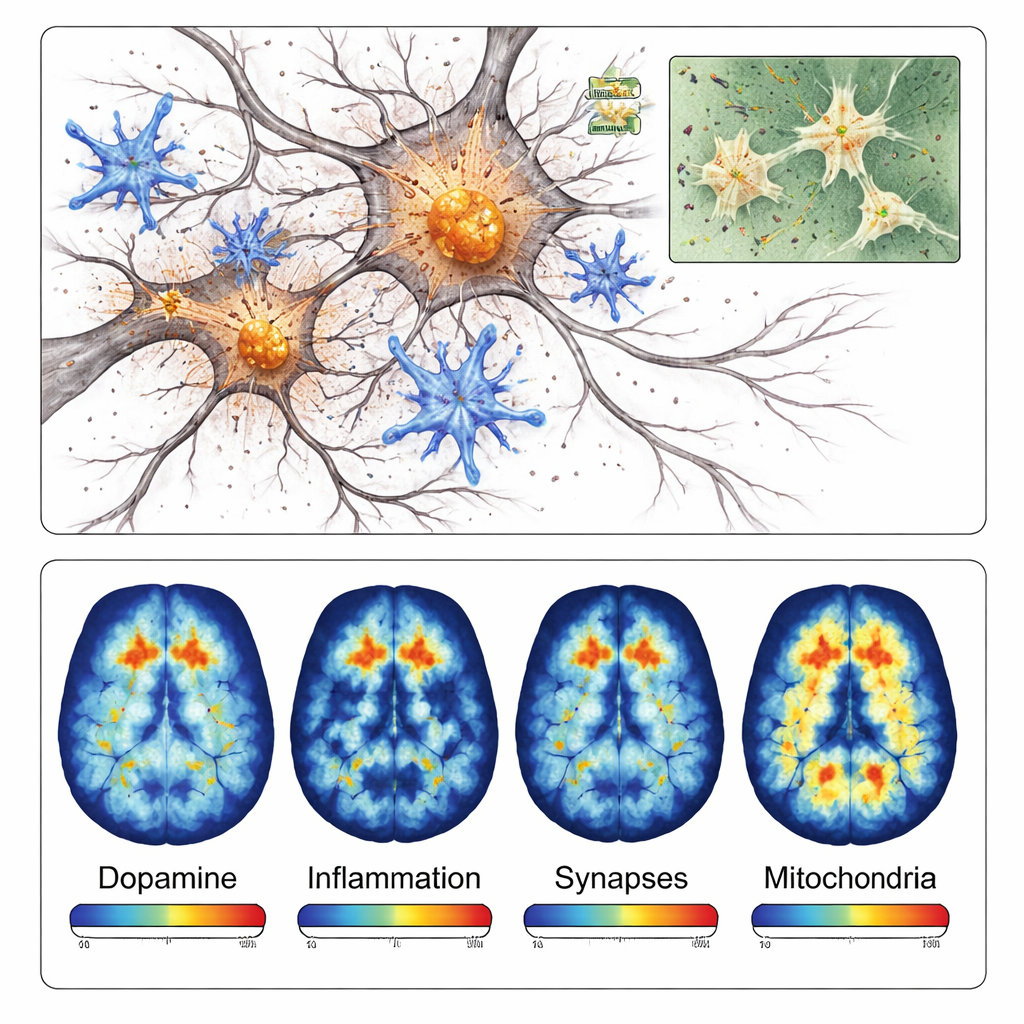
Colocando os scanners de PET para funcionar
Por ser localizado e se desenvolver rapidamente, este modelo é especialmente adequado à tomografia por emissão de pósitrons (PET), uma técnica de imageamento que pode medir moléculas específicas em cérebros vivos. Os pesquisadores testaram quatro radiotraçadores PET diferentes que se ligam a terminais nervosos dopaminérgicos, microglia inflamatória, proteínas sinápticas e enzimas mitocondriais. Em cada caso, as varreduras por PET mostraram sinais mais baixos ou mais altos no lado injetado de maneiras que correspondiam às observações microscópicas. Por exemplo, o radiotraçador direcionado às vias dopaminérgicas mostrou cerca de 40% menos sinal no lado lesionado, enquanto o radiotraçador de inflamação mostrou mais de 40% a mais de sinal na região afetada.
O que isso significa para pacientes e tratamentos futuros
Este novo modelo de camundongo reúne, em um curto período, muitas das alterações-chave que ocorrem ao longo de anos nos cérebros de pessoas com doença de Parkinson. Como o dano está confinado a uma área pequena e bem definida e pode ser acompanhado por PET, os pesquisadores podem testar com mais eficiência novos radiotraçadores de imagem e potenciais terapias. Embora nenhum camundongo possa reproduzir completamente a condição humana, essa abordagem oferece uma ferramenta prática e poderosa para preencher a lacuna entre o trabalho básico de laboratório e os estudos humanos, ajudando em última instância a refinar o diagnóstico e acelerar a busca por tratamentos melhores.
Citação: Xia, C.A., Tsai, HM., Diaz Garcia, S. et al. Accelerated and localized synucleinopathy in a hybrid mouse model: implications for positron emission tomography studies. npj Imaging 4, 7 (2026). https://doi.org/10.1038/s44303-026-00138-x
Palavras-chave: Doença de Parkinson, alfa-sinucleína, sinucleinopatia, imagem por PET, modelo de camundongo