Clear Sky Science · pt
Modelos de equações diferenciais ordinárias da dinâmica de replicação do SARS-CoV-2 e eficácias de antivirais
Por que os números importam para um vírus novo
Quando a COVID-19 surgiu, os médicos podiam observar o que o vírus fazia aos pacientes, mas não conseguiam prever com facilidade quem ficaria gravemente doente nem quando um medicamento deveria ser administrado para obter o melhor efeito. Este artigo de revisão examina como os pesquisadores transformaram medições virais vindas de pacientes, animais e culturas celulares em “filmes” matemáticos da infecção dentro do corpo. Esses modelos usam equações para acompanhar como o vírus cresce, como nossas células e o sistema imune reagem, e como antivirais e vacinas podem inclinar a balança a nosso favor.
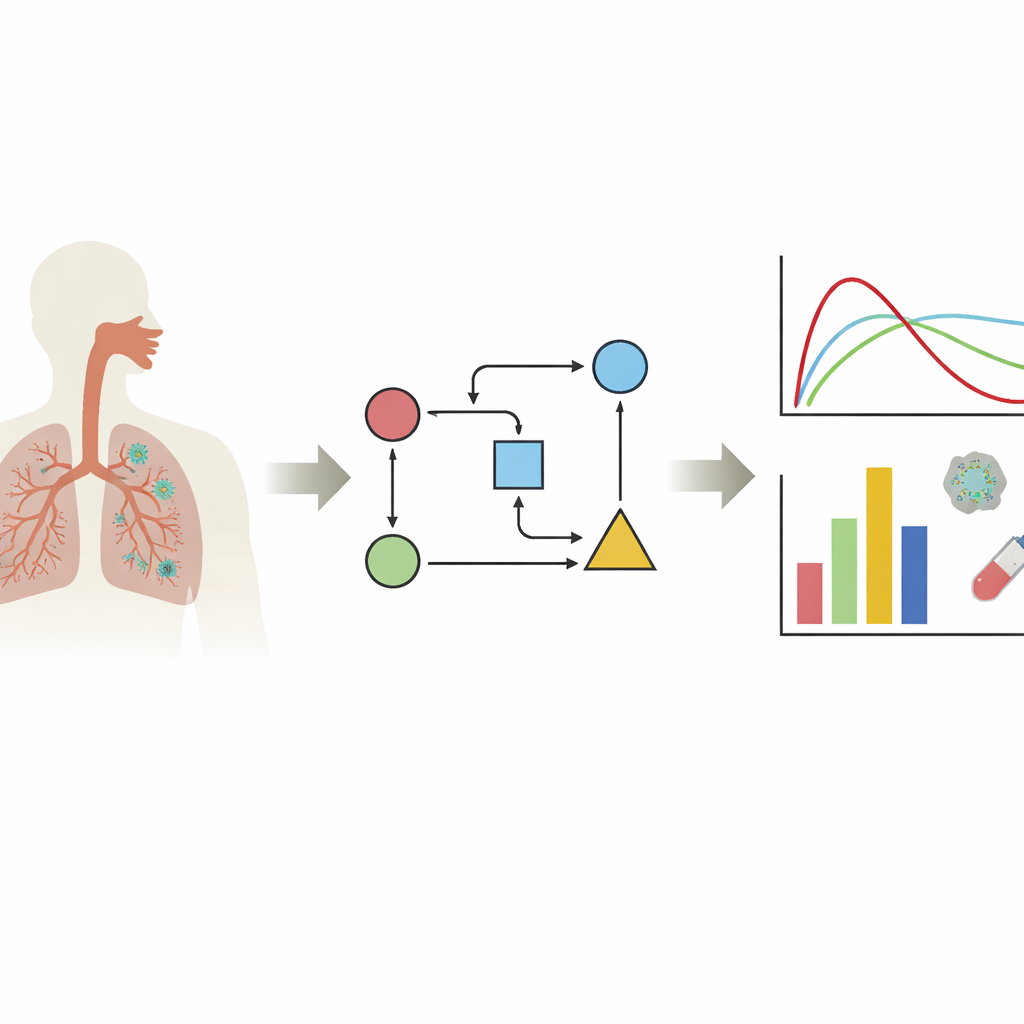
Acompanhando o vírus dentro do corpo
Os autores se concentram em uma família de modelos chamados modelos limitados por células-alvo. Em termos simples, esses modelos rastreiam três protagonistas principais: células saudáveis que podem ser infectadas, células já infectadas e partículas virais livres. Alimentando essas equações com dados reais sobre níveis virais, os pesquisadores podem estimar características ocultas da infecção: com que rapidez o vírus infecta células, quanto tempo uma célula infectada produz vírus e quão rápido o vírus é eliminado. A revisão mostra que a maior parte do trabalho se concentra nos tecidos que mais importam para a COVID-19 — o nariz e as vias aéreas superiores e inferiores — enquanto poucos modelos examinam outros órgãos. Uma mensagem-chave é que o comportamento viral pode parecer muito diferente dependendo do tecido, da variante viral e da linhagem celular estudada em laboratório, de modo que não existe uma curva de infecção “típica” única.
O que aprendemos sobre o sistema imune
Muitos modelos adicionam camadas que representam as defesas precoces do sistema imune e sua resposta mais lenta e direcionada. Estudos focados na primeira linha de defesa sugerem que uma atividade rápida e bem sincronizada de células imunes inatas e moléculas de sinalização pode atenuar a infecção, mas raramente a elimina por si só. Outros trabalhos destacam o papel crucial das células T e dos anticorpos em finalmente controlar o vírus. Os modelos também capturam um lado mais sombrio: se a resposta imune direcionada for tardia ou equivocada, as mesmas ferramentas que deveriam nos proteger podem alimentar “tempestades de citocinas” prejudiciais, nas quais sinais inflamatórios em excesso agridem tecidos saudáveis. Nestas simulações, o equilíbrio fino entre atividade imune benéfica e prejudicial frequentemente decide se a doença permanece branda ou se torna potencialmente fatal.
Quando medicamentos e vacinas funcionam melhor
Como as equações podem ser executadas repetidas vezes sob diferentes hipóteses, elas são ferramentas poderosas para testar estratégias de tratamento no computador antes de testá-las em pessoas. Em muitos estudos, os modelos concordam em um ponto central: antivirais funcionam melhor quando administrados muito cedo, antes que o vírus atinja seu pico e infecte a maior parte das células disponíveis. Tratamentos que impedem o vírus de copiar seu material genético mostram-se especialmente promissores, especialmente quando combinados com outros fármacos que atuam por mecanismos diferentes. O tratamento tardio, em contraste, tende a ter pouco impacto nas simulações, a menos que vários fármacos potentes sejam usados em conjunto. A vacinação é consistentemente prevista como mais eficaz do que os medicamentos isolados, principalmente por preparar o sistema imune para reconhecer o vírus rapidamente e manter níveis virais elevados por pouco tempo.
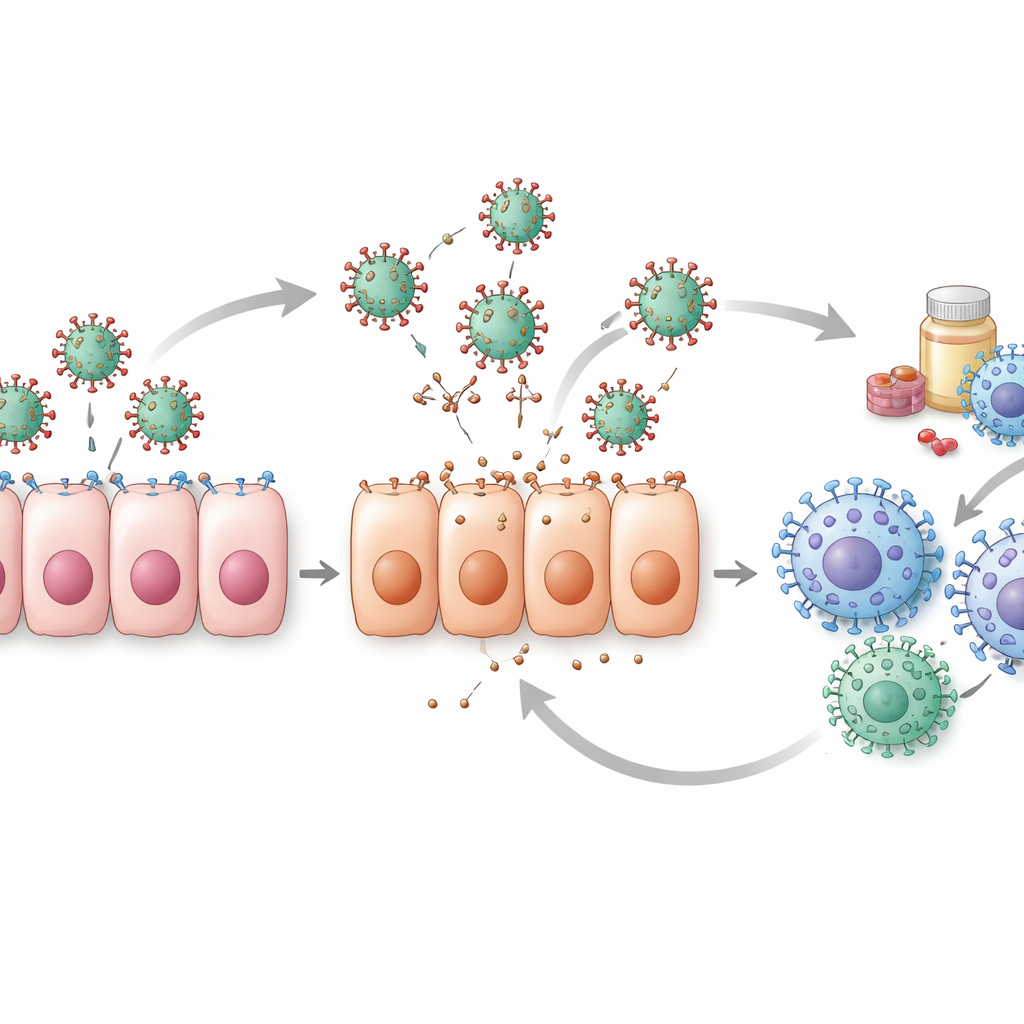
Desafios ocultos nos dados
A revisão também lança luz sobre as fraquezas por trás dos números. A maioria dos conjuntos de dados clínicos começa apenas depois que as pessoas já se sentem doentes, o que significa que os modelos muitas vezes perdem os primeiros dias cruciais da infecção, quando os níveis virais estão crescendo mais rapidamente. Sem essas medições iniciais, diferentes combinações de parâmetros do modelo podem explicar os mesmos dados, tornando difícil ter certeza de qual explicação é a correta. Apenas uma minoria dos estudos realiza verificações rigorosas para ver se suas estimativas de parâmetros são realmente únicas e confiáveis. Estudos em animais e experimentos em culturas celulares ajudam a preencher algumas lacunas, especialmente para pontos temporais iniciais, mas diferenças entre espécies e sistemas de laboratório limitam o quão diretamente esses resultados podem ser aplicados aos humanos.
O que isso significa daqui para frente
Para um não especialista, a conclusão é que modelos matemáticos cuidadosamente construídos melhoraram muito nossa compreensão de como o SARS-CoV-2 se comporta dentro do corpo e de como o timing, combinações de fármacos e vacinação prévia moldam os desfechos. Os modelos concordam amplamente que intervenção precoce e forte — especialmente via vacinação e antivirais administrados no momento certo — dá ao sistema imune a melhor chance de vencer, enquanto respostas tardias, tanto do organismo quanto do tratamento, estão associadas a doença mais grave. Ao mesmo tempo, os autores enfatizam que essas ferramentas só são tão boas quanto os dados que lhes são fornecidos. Para se preparar para variantes futuras ou novos vírus, eles pedem amostragens clínicas mais ricas e precoces e medições imunológicas mais amplas, de modo que os “números por trás da infecção” possam guiar decisões mais rápidas e precisas em surtos no mundo real.
Citação: Kapischke, T., Herrmann, S.T., Bertzbach, L.D. et al. Ordinary differential equation models of SARS-CoV-2 replication dynamics and antiviral drug efficacies. npj Viruses 4, 17 (2026). https://doi.org/10.1038/s44298-026-00183-8
Palavras-chave: dinâmica viral do SARS-CoV-2, modelagem intra-hospedeiro, momento da terapia antiviral, resposta imune, vacinação contra COVID-19