Clear Sky Science · pt
A proteína G solúvel do vírus sincicial respiratório promove a disseminação viral via priming do NLRP3 mediado por TLR2 e piroptose
Por que esse vírus pulmonar importa para todos
O vírus sincicial respiratório, ou VSR, é mais conhecido como uma ameaça de inverno para bebês, mas também leva muitos idosos e pessoas com sistema imunológico debilitado ao hospital. Mesmo com novas vacinas e anticorpos protetores, o VSR ainda reinfecta indivíduos repetidamente e pode causar danos pulmonares graves. Este estudo analisa uma proteína viral pouco conhecida, uma forma solúvel da proteína G do VSR, e revela como ela pode preparar discretamente as células pulmonares para uma inflamação explosiva e ajudar o vírus a se espalhar mais eficientemente pelas vias aéreas.
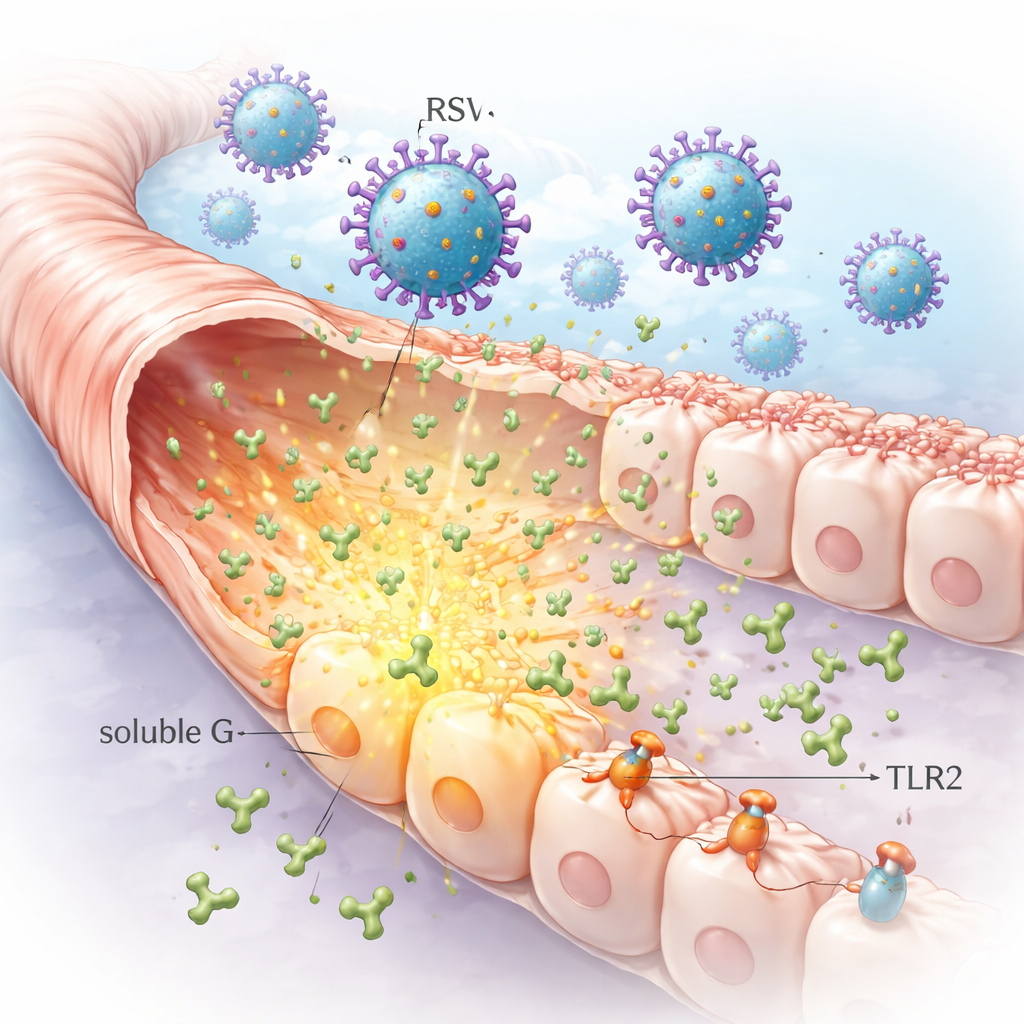
Uma proteína viral secretada que viaja à frente da infecção
O VSR carrega uma proteína de adesão chamada G em sua superfície que o ajuda a se ligar às células das vias aéreas. De forma incomum, células infectadas também liberam grandes quantidades de uma versão livre dessa proteína, conhecida como G solúvel. Os pesquisadores mostraram que células pulmonares infectadas em laboratório podem liberar níveis muito altos de G solúvel em seu entorno. Como essa forma pode difundir-se a partir do sítio original da infecção, ela pode alcançar células vizinhas que ainda não foram infectadas, preparando o terreno para alterações mais amplas no revestimento pulmonar do que o vírus sozinho causaria.
G solúvel como uma chave dupla para superfícies celulares
Combinando microscopia, testes bioquímicos de pull-down e tratamentos enzimáticos, a equipe mapeou como a G solúvel se liga às células. Eles descobriram que ela pode se anexar a cadeias açucaradas chamadas glicosaminoglicanos, assim como a um receptor conhecido do VSR chamado CX3CR1. Crucialmente, a G solúvel também se liga a uma molécula sensora de padrões em células imunes e das vias aéreas chamada TLR2. Um pequeno motivo na proteína G, conhecido como CX3C, mostrou-se importante para a ligação forte ao CX3CR1 e para o recrutamento robusto do TLR2. Isso significa que a G solúvel pode primeiro ser capturada de forma frouxa na superfície celular e então envolver receptores mais específicos que controlam como as células respondem a ameaças.
Preparando as células pulmonares para um tipo inflamatório de morte celular
O envolvimento do TLR2 pela G solúvel revelou-se longe de inofensivo. Em células imunes repórter e linhagens celulares humanas pulmonares, a G solúvel ativou a via de sinalização MyD88–NF-κB a jusante do TLR2, levando à liberação de mensageiros inflamatórios como IL-6 e IL-8. Ao mesmo tempo, aumentou a produção de componentes de um "sistema de alarme" molecular chamado inflamassoma NLRP3 e de enzimas que geram moléculas reativas como óxido nítrico e radicais de oxigênio. Por si só, essas mudanças causaram apenas danos leves. Mas quando células previamente primadas foram posteriormente infectadas com VSR, o segundo ataque desencadeou a montagem completa do inflamassoma, ativação da enzima caspase‑1, formação de poros na membrana celular e uma forma inflamável de morte celular conhecida como piroptose. Esse processo abriu buracos nas células, derramou conteúdos inflamatórios e coincidiu com maiores quantidades de vírus infeccioso sendo liberadas no fluido de cultura.
Como essa reação em cadeia pode agravar a doença pulmonar
O efeito pró-morte da G solúvel foi mais forte em células epiteliais das vias aéreas — as próprias células que o VSR prefere infectar — e dependia do inflamassoma NLRP3, pois um inibidor específico do NLRP3 resgatou em grande parte a viabilidade celular. Em contraste, certas células imunes ricas em TLR2, mas pobres no receptor CX3CR1, não sofreram morte lítica intensa nas mesmas condições. Esse padrão sugere que o VSR usa a G solúvel para enfraquecer e destruir seletivamente o revestimento protetor das vias aéreas enquanto preserva algumas células imunes que podem continuar a produzir sinais. O resultado é um ambiente pulmonar com mais inflamação, mais detritos celulares e mais oportunidades para novas partículas virais escaparem e infectarem células vizinhas.
O que isso significa para tratamentos futuros
Para um público não especializado, a mensagem principal é que o VSR não depende apenas de danos diretos causados pela invasão viral. Ao liberar grandes quantidades de proteína G solúvel, ele pode "amolecer" células próximas via TLR2, tornando-as mais propensas a morrer de forma inflamatória e a liberar vírus. Este trabalho identifica vários passos nessa cadeia — a própria G solúvel, seu motivo CX3C, o TLR2 e o inflamassoma NLRP3 — como potenciais alvos terapêuticos. Em princípio, terapias que bloqueiem a interação entre a G solúvel e o TLR2, ou que atenuem a atividade do NLRP3, poderiam reduzir tanto a lesão pulmonar quanto a disseminação viral. Essas abordagens poderiam, no futuro, complementar vacinas e anticorpos já existentes contra o VSR, oferecendo melhor proteção para os pacientes mais jovens e vulneráveis.
Citação: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
Palavras-chave: vírus sincicial respiratório, proteína G solúvel, inflamassoma TLR2, piroptose, inflamação pulmonar