Clear Sky Science · pt
Avaliação STAR (stroma–tumor AI risk): associação da proporção tumor–estroma derivada por IA com sobrevida de pacientes oferece valor prognóstico adicional além do KELIM no câncer epitelial de ovário
Por que o “vizinhança” ao redor de um tumor importa
Quando pensamos em câncer, geralmente imaginamos uma massa de células fora de controle. Mas os tumores vivem em um bairro movimentado de tecido de suporte, vasos sanguíneos e células imunes chamado estroma. Este estudo faz uma pergunta simples, porém poderosa: podemos usar o equilíbrio entre células tumorais e esse tecido circundante, medido por inteligência artificial (IA) em lâminas de microscópio rotineiras, para prever quais pacientes com câncer de ovário provavelmente terão desfechos melhores ou piores — antes mesmo do início do tratamento?
Uma nova forma de ler lâminas de biópsia padrão
Mulheres com câncer epitelial de ovário normalmente têm tecido removido em cirurgia ou biópsia. Essas amostras são coradas e examinadas ao microscópio em todos os hospitais. Os pesquisadores focaram em uma característica chamada proporção tumor–estroma (TSP): quanto da imagem é composto por tecido de suporte em comparação com células cancerosas. Em trabalhos anteriores, patologistas estimavam essa proporção a olho e descobriram que tumores ricos em estroma frequentemente se comportavam de forma mais agressiva e resistiam à quimioterapia padrão à base de platina. No estudo atual, a equipe usou um sistema de aprendizado profundo para medir automaticamente a TSP em lâminas digitalizadas, com o objetivo de transformar uma tarefa manual e um tanto subjetiva em uma leitura rápida e reprodutível disponível já no momento do diagnóstico.
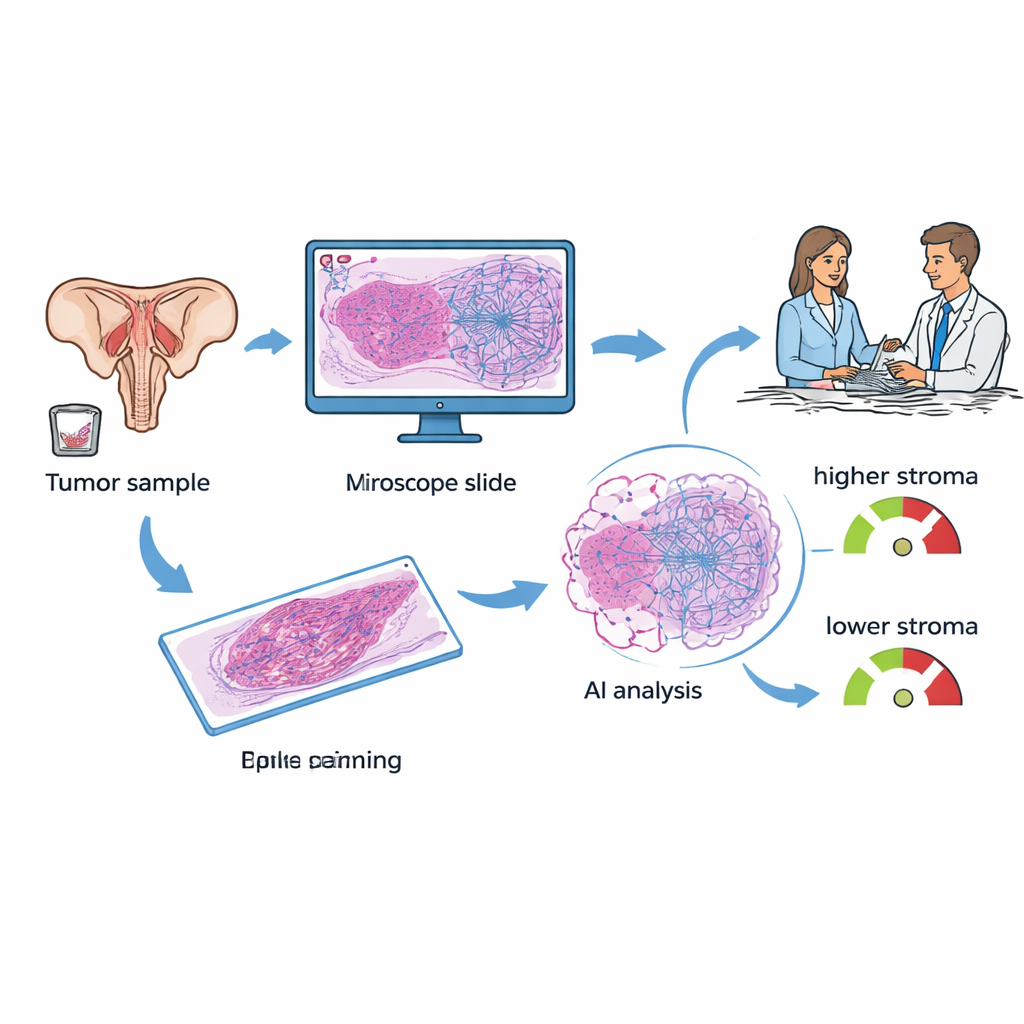
Comparando a análise de tecido por IA com um escore baseado em sangue
Hoje, uma ferramenta amplamente discutida para câncer de ovário é o KELIM, um escore baseado em quão rapidamente um marcador sanguíneo chamado CA-125 cai durante os primeiros 100 dias de quimioterapia. O KELIM é barato e útil, mas só pode ser calculado após várias semanas de tratamento, e nem todas as pacientes têm exames sanguíneos precoces suficientes para gerar o escore. Os investigadoras reuniram dados de 89 mulheres tratadas em um único centro de câncer que tinham tanto lâminas de tecido quanto pelo menos três medidas de CA‑125. Eles calcularam o KELIM para cada paciente, um patologista rotulou as regiões tumorais nas lâminas e então o modelo de IA estimou a TSP, classificando cada caso como “baixo estroma” (menos de 50% de estroma) ou “alto estroma” (50% ou mais).
IA iguala especialistas e sinaliza tumores de maior risco
O julgamento da IA correspondeu de perto ao dos patologistas experientes: em 94% dos casos, a classificação automatizada da TSP concordou com a manual, um nível de concordância considerado excelente. Quando a equipe analisou os desfechos das pacientes, verificaram que mulheres cujos tumores foram classificados como alto estroma pela IA apresentaram sobrevida global significativamente pior do que aquelas com tumores baixo estroma. Em termos estatísticos, TSP alta quase dobrou o risco de morte durante o seguimento, e esse efeito persistiu mesmo após ajustar pelo escore KELIM. Em contraste, neste grupo de pacientes do mundo real, o KELIM esteve relacionado à resistência tumoral aos fármacos à base de platina, mas não se mostrou claramente associado ao tempo de sobrevida das pacientes.
O que isso pode significar para decisões de tratamento
Como a TSP pode ser medida a partir de lâminas rotineiras obtidas no momento do diagnóstico, a TSP baseada em IA oferece uma maneira de avaliar o risco antes do início da quimioterapia, potencialmente meses antes do KELIM. Um resultado de TSP alto pode alertar os clínicos de que um tumor provavelmente é mais agressivo e mais difícil de tratar, indicando monitoramento mais próximo, consideração precoce de terapias adicionais ou estratégias cirúrgicas diferentes. O método também é relativamente de baixo custo: depende de imagens patológicas já existentes e de um modelo de software, em vez de novos testes laboratoriais. Os autores argumentam que a TSP automatizada poderia funcionar ao lado de outros marcadores, como testes genéticos e tendências do CA‑125, para refinar o prognóstico sem acrescentar um ônus substancial para pacientes ou equipes de patologia.
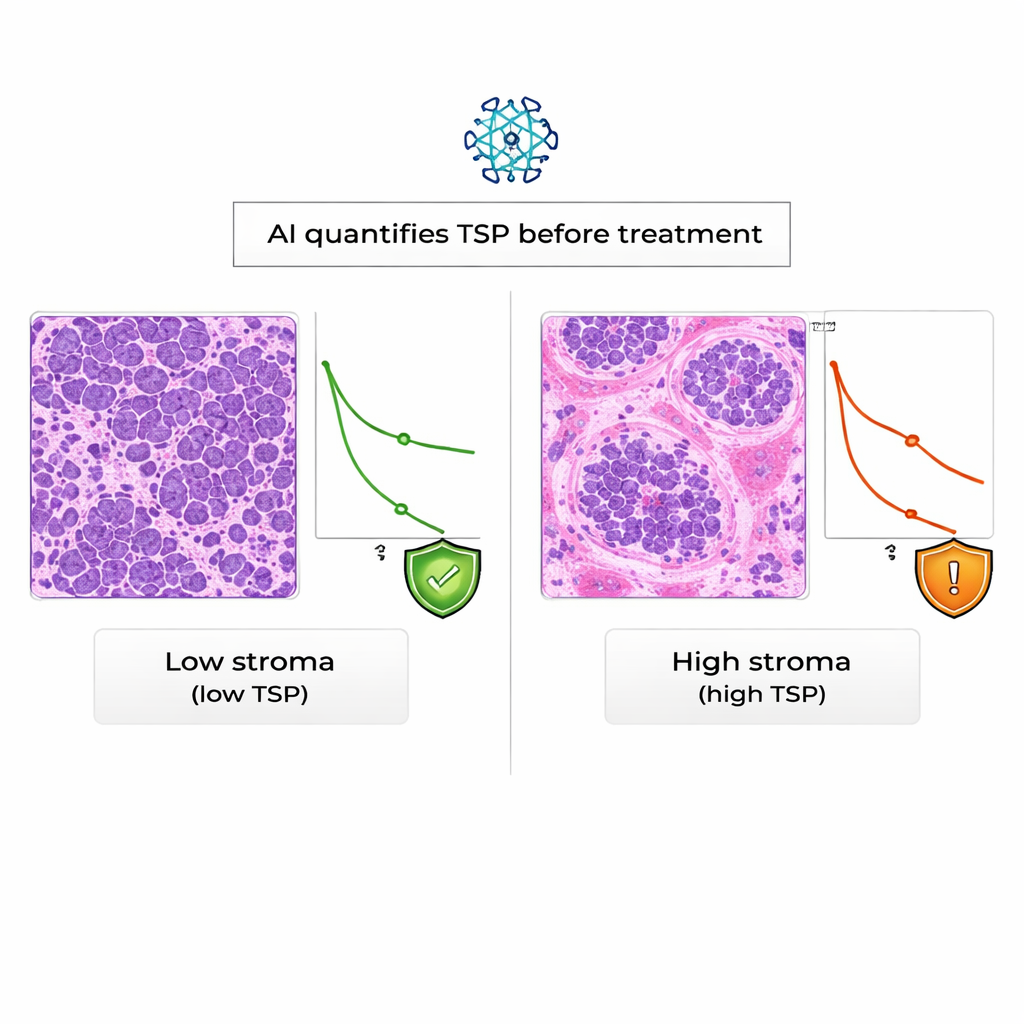
Olhando adiante: orientação mais inteligente e antecipada para pacientes
Para o público leigo, a mensagem principal é que nem todos os cânceres de ovário são iguais, e o tecido de suporte ao redor do tumor carrega pistas importantes sobre como a doença vai se comportar. Este estudo mostra que a IA pode ler essas pistas com confiabilidade em lâminas de biópsia padrão e que tumores com muito estroma tendem a estar associados a pior sobrevida, independentemente de escores baseados em sangue existentes. Embora sejam necessários estudos maiores e mais diversos antes que essa abordagem faça parte da prática rotineira, a TSP derivada por IA mostra-se promissora como um sinal de alerta precoce que pode ajudar médicos a personalizar planos de tratamento e oferecer às pacientes expectativas mais claras desde o início.
Citação: Aggarwal, A., Madill, M., Jana, M. et al. STAR (stroma-tumor AI risk) assessment: association of AI-derived tumor-stroma proportion with patient survival provides added prognostic value beyond KELIM in epithelial ovarian cancer. BJC Rep 4, 4 (2026). https://doi.org/10.1038/s44276-026-00205-1
Palavras-chave: câncer de ovário, inteligência artificial, microambiente tumoral, biomarcador prognóstico, patologia digital