Clear Sky Science · pt
Levantamento genômico revela o surgimento de uma linhagem dominante multirresistente em populações de Proteus mirabilis
Por que esse germe hospitalar importa para você
Para muitas pessoas, infecções do trato urinário são um incômodo doloroso ocasional. Mas em hospitais e casas de repouso, algumas infecções são provocadas por bactérias resistentes que aderem a cateteres, suportam múltiplos antibióticos e se espalham silenciosamente entre pessoas e animais. Este estudo acompanha um desses culpados, Proteus mirabilis, ao redor do globo, usando seu DNA como diário de viagem para revelar como uma única linhagem difícil de tratar ascendeu discretamente à dominância ao longo do último século.
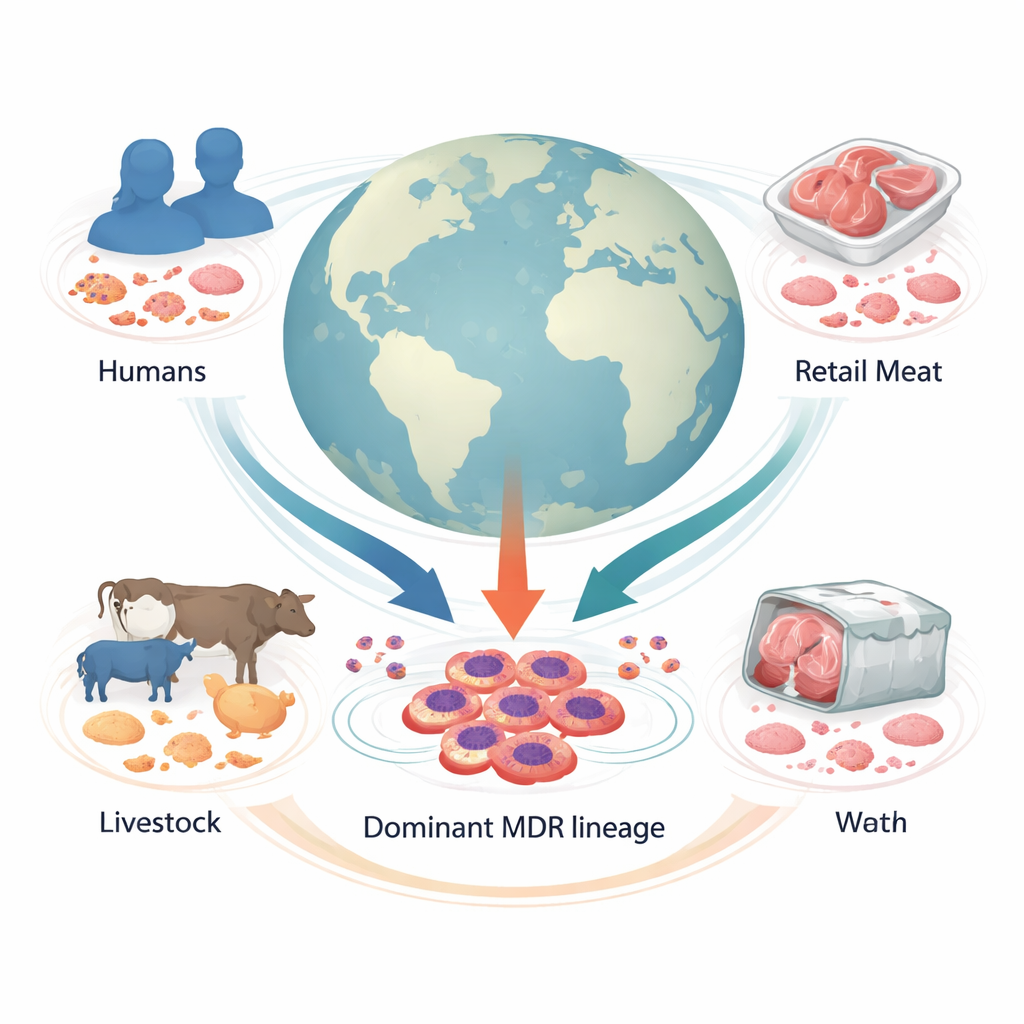
Uma visão global de uma ameaça oculta
Os pesquisadores montaram genomas de 1.142 amostras de Proteus mirabilis coletadas em 34 países, provenientes de humanos, animais de produção, carne à venda e outros ambientes. Ao comparar genomas completos, eles classificaram as bactérias em 178 famílias genéticas. Uma se destacou: o “Cluster-1”, uma linhagem majoritária que representou uma em cada cinco amostras e incluiu cepas de hospitais em vários continentes. A maioria dessas cepas veio de humanos, mas uma parcela substancial também foi isolada em animais de fazenda e em carne, indicando que essa linhagem circula entre espécies e ao longo da cadeia alimentar.
Uma linhagem equipada com muitos escudos contra medicamentos
Quando a equipe vasculhou os genomas em busca de genes de resistência a antibióticos, o Cluster-1 apresentou uma carga notavelmente maior. Em média, seus membros abrigavam quase 18 genes de resistência cada, muito mais do que outras linhagens. Entre eles há genes que anulam alguns dos nossos antibióticos mais potentes, como os carbapenêmicos, frequentemente reservados como recurso final. Muitos desses genes de resistência estão inseridos em uma grande “ilha” de DNA chamada PmGRI1, que pode saltar entre bactérias. Algumas versões dessa ilha carregam mais de 20 genes de resistência ao mesmo tempo, transformando efetivamente o Proteus em uma farmácia ambulante de defesas e deixando os médicos com poucas opções de tratamento.
Traços pegajosos que ajudam as bactérias a se manter
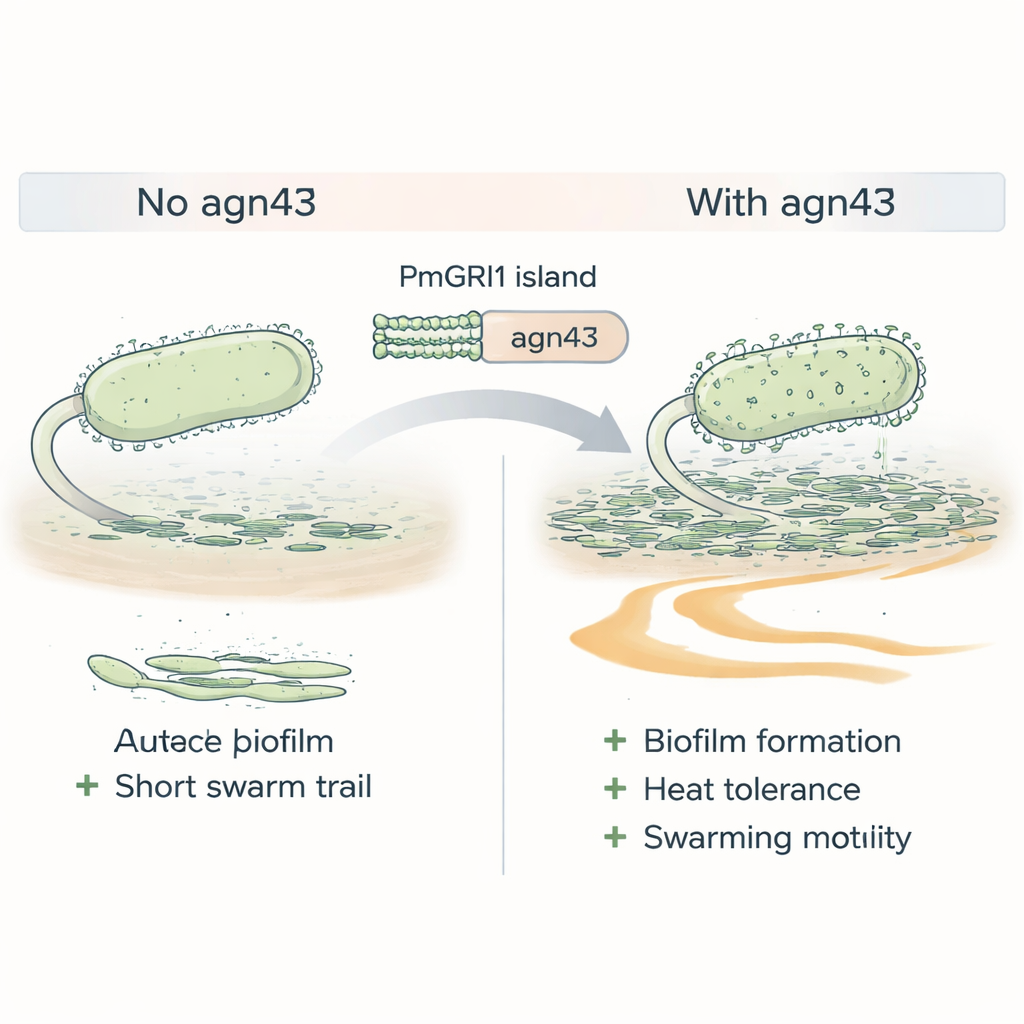
A resistência por si só não garante sucesso; as bactérias também precisam sobreviver no corpo e no ambiente hospitalar. As cepas do Cluster-1 eram enriquecidas em genes associados à adesão às células e à formação de biofilmes — comunidades viscosas que protegem as bactérias de medicamentos e do sistema imune. Um gene de destaque na ilha PmGRI1, chamado agn43, produz uma proteína de superfície que age como um velcro molecular, ajudando as células a se agregarem. Quando os cientistas deletaram agn43 em uma cepa do Cluster-1, o mutante formou biofilmes mais fracos, tolerou menos o estresse por calor e apresentou menor capacidade de invasão em superfícies, características que normalmente ajudam o Proteus a colonizar cateteres urinários e a se espalhar pelo trato urinário.
Como e onde essa super-linhagem se espalhou
Ao combinar diferenças genéticas com as datas de isolamento, os pesquisadores reconstruíram uma linha do tempo para o Cluster-1. Estimaram que seu ancestral comum mais recente apareceu por volta de 1910, décadas antes do uso generalizado de antibióticos modernos. A linhagem depois se dividiu em dois ramos de importância clínica: um observado principalmente na China que carrega um gene que inativa carbapenêmicos chamado blaKPC-2, e outro visto sobretudo nos Estados Unidos que carrega um gene relacionado, blaIMP-27. A partir do final dos anos 1980, o Cluster-1 expandiu-se rapidamente e foi repetidamente detectado movendo-se entre países e entre humanos, animais de produção e carne, sublinhando seu potencial epidêmico.
O que isso significa para pacientes e saúde pública
Para um leigo, a mensagem é que uma família particular de Proteus mirabilis evoluiu para um germe hospitalar altamente bem-sucedido ao combinar duas vantagens: uma armadura espessa de genes de resistência a antibióticos e uma “pegajosidade” extra que o ajuda a formar filmes protetores e a persistir em cateteres e tecidos. Essa combinação torna as infecções mais difíceis de tratar e mais fáceis de disseminar. O trabalho ressalta a necessidade de vigilância genética rigorosa dessa linhagem tanto em hospitais quanto na agricultura, controle de infecções mais estrito em torno do uso de cateteres e uso cuidadoso de antibióticos para desacelerar a ascensão e a circulação global de cepas multirresistentes.
Citação: Zhang, T., Wei, H., Ju, Z. et al. Genomic survey uncovers the emergence of a multidrug-resistant dominant lineage in Proteus mirabilis populations. npj Antimicrob Resist 4, 17 (2026). https://doi.org/10.1038/s44259-026-00189-5
Palavras-chave: resistência a antibióticos, infecção do trato urinário, infecções hospitalares, genômica bacteriana, biofilme