Clear Sky Science · pt
Resposta global à exposição a antibióticos revela papel crítico do metabolismo de nucleotídeos na tolerância de alto nível a β-lactâmicos
Por que algumas bactérias resistem aos nossos melhores antibióticos
Antibióticos deveriam eliminar bactérias nocivas, mas muitas infecções persistem teimosamente ou reaparecem após o tratamento. Este artigo explora uma razão pouco reconhecida para isso: algumas bactérias conseguem se abrigar e sobreviver temporariamente mesmo a doses muito altas de fármacos potentes como a penicilina. Ao revelar como esses microrganismos reprogramam sua química interna para resistir ao ataque, os pesquisadores indicam novas maneiras de restaurar a eficácia dos antibióticos existentes.
Um truque furtivo de sobrevivência dentro das infecções
Quando expostas a antibióticos β-lactâmicos, como a penicilina, muitas bactérias Gram-negativas perigosas não morrem simplesmente. Em vez disso, podem perder sua parede celular rígida e se transformar em corpos frágeis e arredondados chamados esferoplastos. Nessa forma, deixam de se multiplicar, mas permanecem vivas e metabolicamente ativas. Depois que o fármaco some, reconstruem a parede, retomam a forma normal de bastonete e podem reativar a infecção. Como essa “tolerância” é um passo em direção à resistência completa aos antibióticos e à falha do tratamento, entender como os esferoplastos sobrevivem é crucial para a medicina futura.
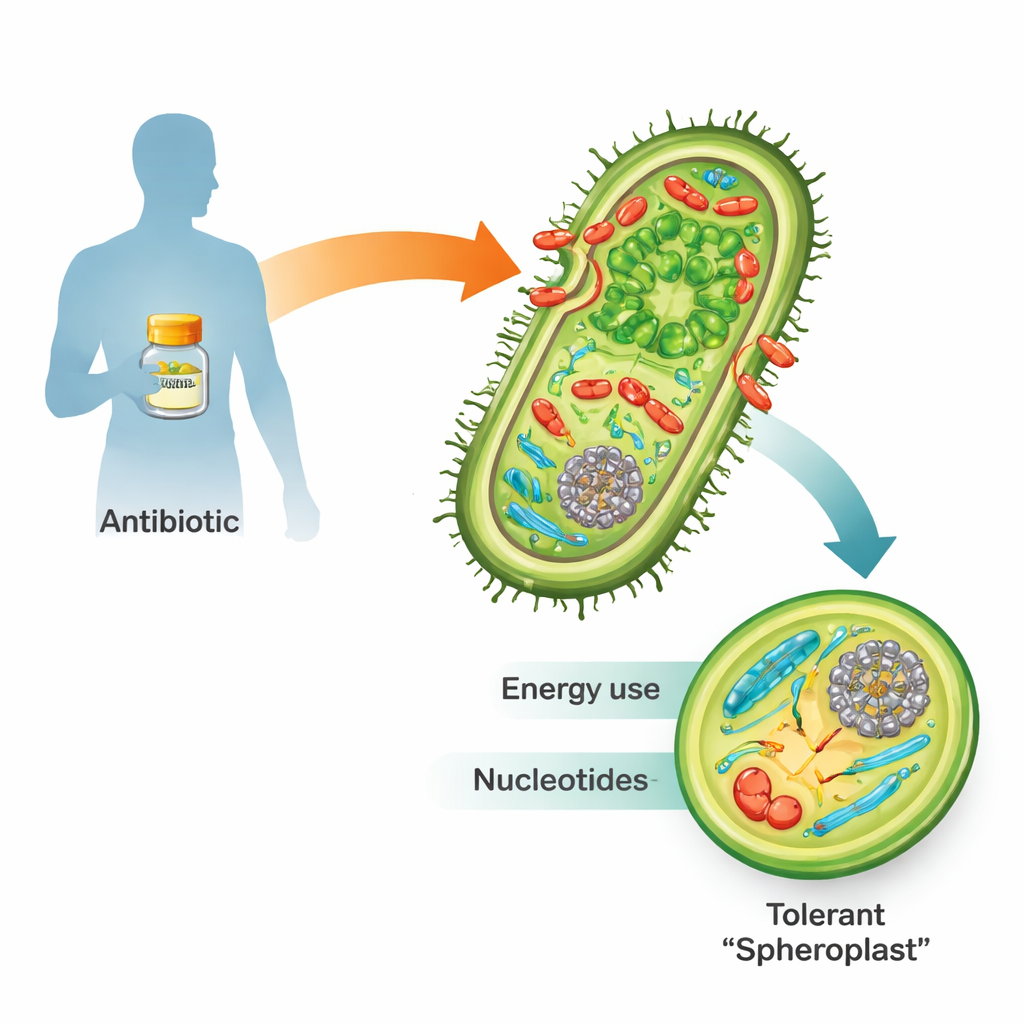
Escutando a transmissão de emergência da célula
A equipe usou Vibrio cholerae, a bactéria que causa a cólera, como modelo porque é excepcionalmente tolerante a β-lactâmicos e fácil de manipular geneticamente. Eles submeteram as bactérias a dez vezes a dose letal mínima de penicilina e acompanharam a resposta ao longo do tempo com duas ferramentas poderosas. A transcriptômica rastreou quais genes foram ativados ou desativados, enquanto a metabolômica mediu centenas de pequenas moléculas que alimentam e constroem a célula. Juntas, essas técnicas “multi-ômicas” criaram um mapa temporal de como uma célula tolerante reconfigura seu funcionamento interno durante um ataque medicamentoso.
Redirecionamento metabólico e um ponto fraco oculto
Os dados revelaram mudanças amplas em vias centrais. Genes para a construção da parede celular foram fortemente ativados, consistente com a tentativa da célula de reparar danos e se preparar para a recuperação. Sistemas de resposta ao choque térmico e ao estresse também se intensificaram, provavelmente para lidar com proteínas mal dobradas e oxidadas geradas pelo estresse induzido pelo antibiótico. Ao mesmo tempo, o metabolismo central do carbono mudou: certos passos do ciclo do TCA (o principal gerador de energia da célula) foram impulsionados, enquanto intermediários-chave da glicólise, como glicose-6-fosfato e frutose-6-fosfato, foram dramaticamente reduzidos. Esses intermediários normalmente alimentam tanto a produção de energia quanto a síntese da parede celular, sugerindo que um ciclo “fútil” contínuo de material da parede estava drenando recursos.
Nucleotídeos sob pressão
A mudança mais marcante envolveu nucleotídeos, os blocos de construção do DNA, RNA e de muitas moléculas transportadoras de energia. Os níveis de muitos nucleotídeos e de seus precursores despencaram em células tratadas com penicilina, mesmo quando os genes para sintetizá-los do zero foram fortemente ativados. Ao mesmo tempo, genes envolvidos na “reciclagem” de nucleotídeos foram reprimidos, como se a célula tentasse conservar o que ainda restava. Esses padrões sugerem que os esferoplastos estão sob forte estresse de nucleotídeos. Quando os pesquisadores interferiram deliberadamente em vias que fornecem precursores de nucleotídeos — como a via das pentoses-fosfato — ou bloquearam a produção de nucleotídeos com outro fármaco, o trimetoprim, a combinação com β-lactâmicos matou muito mais bactérias do que cada fármaco sozinho. Essa forte sinergia foi observada não apenas em Vibrio cholerae, mas também em cepas clínicas altamente tolerantes de Klebsiella pneumoniae e Escherichia coli.
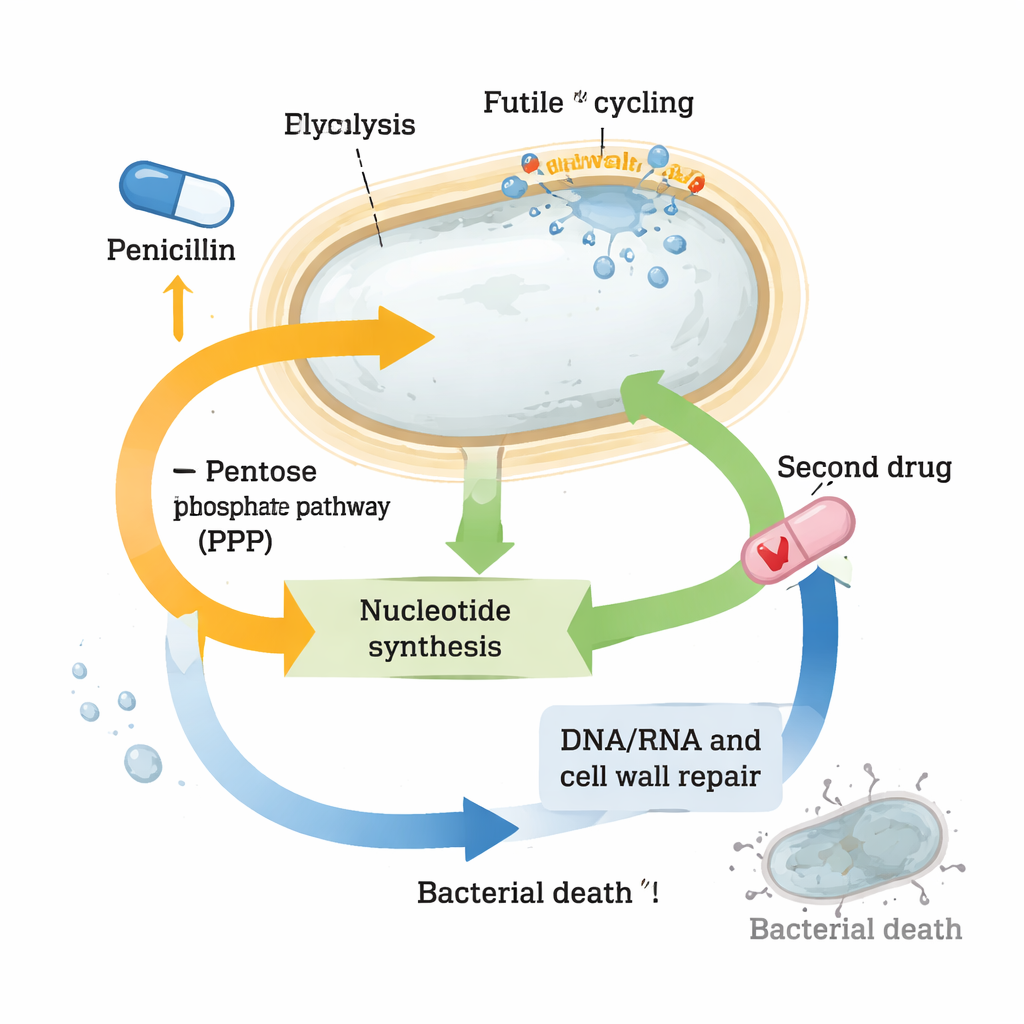
Transformando a química da sobrevivência em vantagem terapêutica
Apesar da grande remodelação de seu metabolismo, os esferoplastos tolerantes conseguem manter sua moeda energética, o ATP, relativamente estável e evitar danos catastróficos, o que os ajuda a resistir a exposições longas a antibióticos. Mas o trabalho mostra que, ao fazer isso, esgotam seus pools de nucleotídeos até o limite. Esse equilíbrio precário cria uma vulnerabilidade: empurrar um pouco mais o metabolismo de nucleotídeos com um segundo fármaco colapsa suas defesas e restaura a capacidade letal dos antibióticos. Para leitores leigos, a conclusão é que algumas bactérias sobrevivem aos antibióticos não porque os fármacos deixem de atingir seus alvos, mas porque as células reprogramam rapidamente sua química para suportar o golpe. Ao encontrar e explorar os elos fracos dessa reconfiguração de sobrevivência — aqui, o metabolismo de nucleotídeos — os pesquisadores podem transformar antibióticos antigos em terapias combinadas poderosas que superem até patógenos altamente tolerantes.
Citação: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
Palavras-chave: tolerância a antibióticos, antibióticos β-lactâmicos, metabolismo de nucleotídeos, persistência bacteriana, combinações de fármacos