Clear Sky Science · pt
Atenuação da ativação epicárdica e da abundância de miofibroblastos via o eixo Fbln2–Nupr1b estimula a regeneração cardíaca em zebrafish
Por que alguns corações conseguem se curar
Quando uma pessoa sofre um ataque cardíaco, o músculo danificado costuma ser reparado com uma cicatriz rígida que nunca cicatriza por completo. Os zebrafish, pequenos peixes listrados de aquário, fazem algo notável: eles regeneram o tecido cardíaco e, com o tempo, removem grande parte da cicatriz. Este estudo aborda uma pergunta aparentemente simples, mas com grandes implicações médicas: como um coração em cura sabe quando construir tecido cicatricial e quando removê-lo para que novo músculo possa crescer? Ao decifrar esse equilíbrio nos zebrafish, o trabalho aponta para estratégias que um dia podem ajudar corações humanos lesionados a se reparar em vez de falhar.
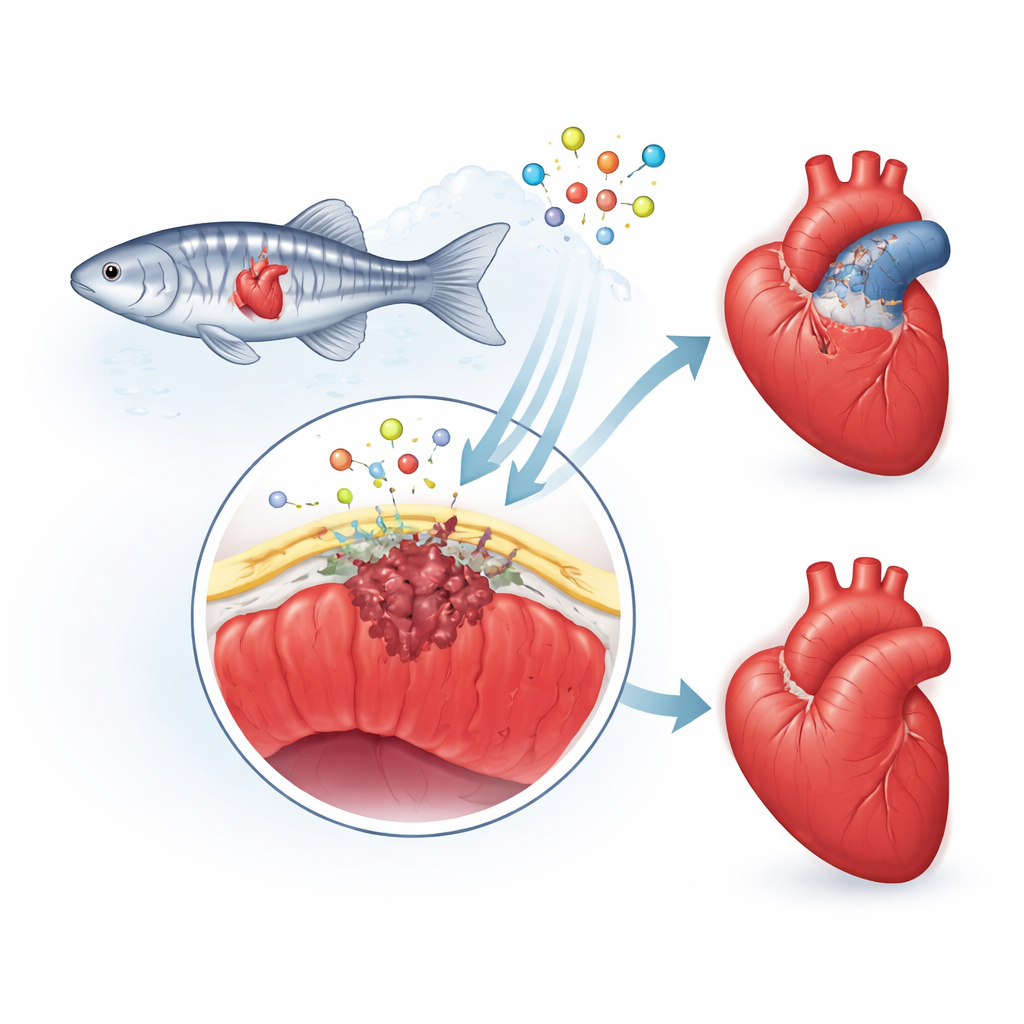
A camada protetora externa do coração
Os pesquisadores concentram-se no epicárdio, uma fina “camada” que cobre o coração. Após a lesão, essa camada desperta, suas células mudam de identidade e algumas migram para a área danificada. Lá, tornam-se células de suporte e formadoras de cicatriz, e liberam sinais químicos que orientam o crescimento de novos vasos sanguíneos e do músculo cardíaco. Em humanos, essa resposta de reparo tende a exceder o necessário, deixando uma cicatriz espessa e permanente. Nos zebrafish, porém, a cicatriz é temporária e é gradualmente desmontada à medida que o músculo saudável retorna. A equipe levantou a hipótese de que uma proteína chamada fibulina-2 (Fbln2), presente no arcabouço em torno do coração, ajuda a definir o ritmo e a intensidade dessa resposta epicárdica.
Um dimmer molecular na formação de cicatrizes
Usando edição genética em zebrafish, os cientistas criaram dois tipos de animais com níveis diferentes de Fbln2: uma linhagem com Fbln2 reduzida e outra com a proteína completamente removida. Eles lesionaram os corações dos peixes com uma sonda de congelamento, imitando um infarto, e acompanharam a cicatrização ao longo de semanas a meses. Quando os níveis de Fbln2 foram reduzidos, a divisão celular precoce no músculo cardíaco e no endotélio dos vasos diminuiu, mas a cicatriz fibrosa que se formou foi menor e mais facilmente remodelada. Em três meses, esses corações haviam regenerado bem e retinham pouco colágeno, o principal componente da cicatriz. Em contraste, peixes que careciam completamente de Fbln2 mostraram um bloqueio mais acentuado de uma via chave de crescimento e cicatrização, envolvendo uma família de sinais conhecida como TGFβ, e apresentaram muito menos células formadoras de cicatriz logo sob o epicárdio. Suas cicatrizes iniciais também foram menores—porém, mais tarde, esses corações não conseguiram remover o colágeno e terminaram com cicatrizes grandes e duradouras e regeneração pobre.
Observando de perto as mudanças de estado epicárdico
Para ver como as células epicárdicas se comportavam em resolução de célula única, a equipe usou sequenciamento de RNA de célula única logo após a lesão. Identificaram vários “estados” celulares epicárdicos, incluindo células em repouso, células recém-ativadas, células estressadas que se adaptam a baixo oxigênio e células que estavam ativamente se dividindo. Em peixes com Fbln2 normal, as células epicárdicas progrediam de forma contínua do estado de repouso para ativado e depois para estados mais maduros. Em peixes com Fbln2 reduzida ou ausente, essa progressão estagnou: as células permaneceram em estágios iniciais e os grupos ativados mais maduros estiveram sub-representados, especialmente nos animais com perda completa. Vários genes que normalmente se ativam durante a ativação epicárdica e em resposta à sinalização TGFβ foram reduzidos, apontando a Fbln2 como um regulador dessa via que decide com que intensidade o epicárdio se compromete a formar e remodelar tecido cicatricial.
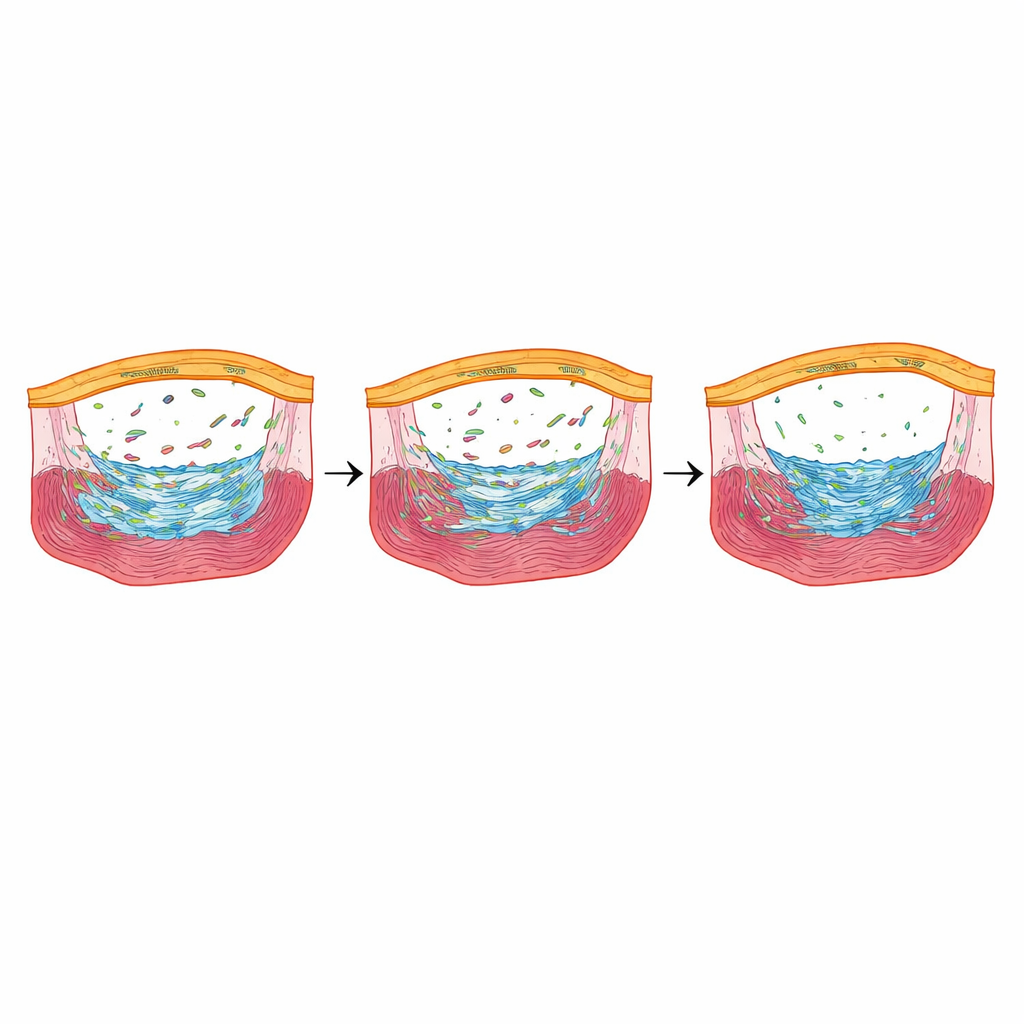
Um respondedoor ao estresse que ajusta o reparo
Entre os genes mais fortemente reduzidos quando a Fbln2 foi diminuída, um sobressaiu: nupr1b, um regulador sensível ao estresse ativo em células epicárdicas durante as fases iniciais da cura. Quando os pesquisadores deletaram nupr1b, os zebrafish apresentaram menos células epicárdicas formadoras de cicatriz e menor divisão de cardiomiócitos, além de manter grandes depósitos de colágeno meses após a lesão—muito semelhante aos peixes que careciam totalmente de Fbln2. Surpreendentemente, quando eles reativaram temporariamente nupr1b apenas nas células epicárdicas de peixes com Fbln2 reduzida, o número de células formadoras de cicatriz e a proliferação dos cardiomiócitos retornaram, e a cicatrização tardia aumentou. Bloquear quimicamente os receptores de TGFβ reduziu os níveis de nupr1b, posicionando nupr1b a jusante de um eixo de sinalização Fbln2–TGFβ.
O que isso significa para curar o coração humano
Em conjunto, essas descobertas revelam um “eixo epicárdico Fbln2–Nupr1b” que ajuda os corações de zebrafish a caminhar na corda bamba entre fibrose insuficiente e excessiva. Reduzir ligeiramente esse eixo modera o estouro inicial de cicatrização e favorece a remoção eficiente da cicatriz, enquanto desligá-lo completamente prejudica a regeneração e deixa uma cicatriz rígida para trás. Para a medicina humana, a lição é que o objetivo não é bloquear a cicatrização por completo, mas regulá-la—mantendo estrutura suficiente para prevenir ruptura e garantindo que o tecido cicatricial seja temporário e possa ser substituído por músculo saudável. Entender e, eventualmente, aproveitar esse sistema de controle dos zebrafish pode orientar terapias futuras que incentivem o coração humano lesionado rumo à regeneração verdadeira em vez da cicatrização crônica.
Citação: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
Palavras-chave: regeneração cardíaca, fibrose, zebrafish, epicárdio, sinalização TGF-beta