Clear Sky Science · pt
Avaliação integrativa genômica e bibliográfica da cardiomiopatia arritmogênica relacionada à desmogleína 2 com validação em coorte italiana
Por que esse gene do coração importa para famílias
Muitos problemas cardíacos súbitos em jovens e em pessoas aparentemente saudáveis não são aleatórios — eles estão escritos, ao menos em parte, no DNA. Este artigo explora uma proteína “cola” cardíaca chave chamada desmogleína‑2 e mostra como pequenas alterações em seu gene podem enfraquecer o músculo cardíaco, perturbar seu ritmo elétrico e aumentar o risco de eventos perigosos. Ao combinar grandes bancos de dados genéticos com um grupo de pacientes italiano cuidadosamente acompanhado, os pesquisadores oferecem respostas mais claras para famílias que se perguntam o que realmente significa um resultado de teste para esse gene.
A cola mecânica do coração
As células do músculo cardíaco precisam permanecer firmemente unidas enquanto batem milhões de vezes ao longo da vida. A desmogleína‑2 faz parte de uma estrutura microscópica em forma de rebite que prende células vizinhas para que elas possam puxar em conjunto. Os autores explicam como essa proteína atravessa do lado externo da célula, onde se prende a um parceiro correspondente na célula adjacente, até o interior, onde se conecta a uma estrutura de suporte. Como a desmogleína‑2 é o único membro de sua família presente nas células cardíacas, qualquer dano sério a ela não pode ser compensado por um substituto, deixando o coração especialmente vulnerável.
Separando alterações genéticas relevantes do ruído de fundo
O sequenciamento moderno encontra milhares de diferenças no gene da desmogleína‑2 na população, mas a maioria não causa doença. A equipe revisou sistematicamente 115 estudos publicados e recorreu a dois grandes bancos de dados públicos que juntos listavam mais de 5.000 variantes. Usando regras amplamente aceitas em genética médica, reclassificaram cada alteração quanto à probabilidade de ser prejudicial. Descobriram que as variantes verdadeiramente danosas se agrupam em regiões específicas da proteína — especialmente nos segmentos externos que precisam de cálcio para formar uma ponte rígida entre as células, em um trecho curto que deve ser clivado para a maturação da proteína, e na região interna que se prende a outra proteína cardíaca crucial. Muitas outras alterações permaneceram “incertas”, mas um subconjunto mostrou fortes indícios de importância e foi sinalizado para acompanhamento mais detalhado.
O que a coorte italiana revela
Para ver como esses padrões genéticos se manifestam em pessoas reais, os pesquisadores estudaram 95 indivíduos na Itália que carregavam variantes da desmogleína‑2 e foram avaliados em detalhes com exames de imagem, testes de ritmo cardíaco e acompanhamento de longo prazo. Cerca de metade cumpria critérios rigorosos para cardiomiopatia arritmogênica, uma condição na qual partes do músculo cardíaco são gradualmente substituídas por cicatriz e gordura, preparando o terreno para arritmias perigosas. Entre os parentes que carregavam uma variante, apenas cerca de quatro em cada dez apresentaram sinais de doença, ressaltando que um teste genético positivo não garante a doença, mas sinaliza a necessidade de monitoramento cuidadoso. Aqueles com doença manifesta tiveram uma carga notável de eventos arrítmicos graves, enquanto transplantes e óbitos foram menos frequentes, porém presentes.
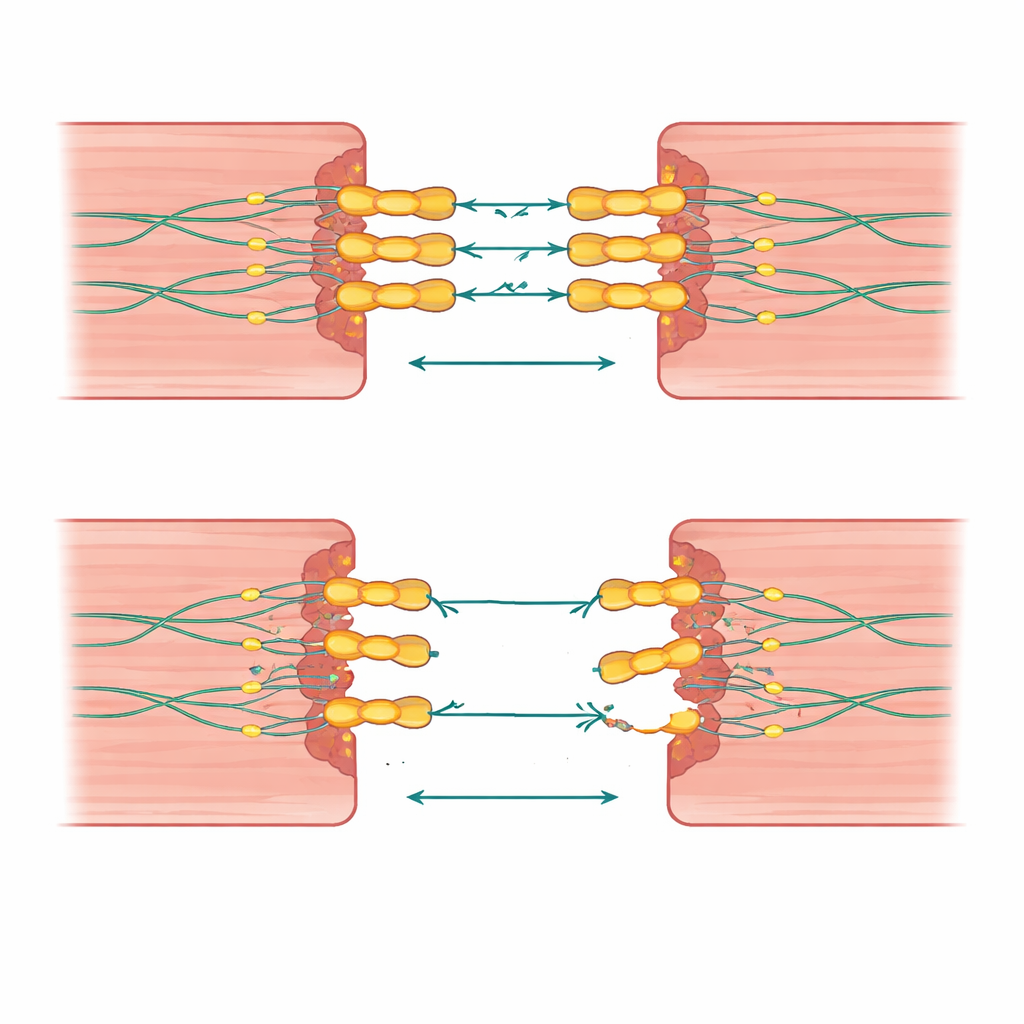
Quando um único impacto não é suficiente
Uma percepção marcante deste trabalho é que o número e a combinação de alterações genéticas importam. Pessoas que herdaram duas cópias defeituosas da desmogleína‑2, ou uma variante de desmogleína‑2 mais uma alteração em um gene relacionado à “cola” cardíaca, tendiam a adoecer mais jovens e a apresentar dano mais difuso em ambos os lados do coração. Algumas famílias carregavam grandes deleções ou duplicações que removiam ou dobravam não só a desmogleína‑2, mas também genes vizinhos, ligando novamente essas alterações a doença agressiva e a aglomerados de mortes súbitas. Em contraste, muitos parentes com apenas uma alteração apresentaram sintomas leves ou nenhum, sugerindo que genes de fundo e fatores da vida, como exercício, podem inclinar a balança entre risco silencioso e doença evidente.
Da forma da proteína ao risco do paciente
Para conectar o código do DNA aos efeitos físicos, a equipe usou modelos proteicos 3D avançados para ver como substituições específicas poderiam afrouxar o andaime da desmogleína‑2. Alterações que distorciam laços de ligação ao cálcio ou quebravam pontos de fixação chave foram previstas como capazes de desestabilizar a proteína e enfraquecer a adesão célula a célula. Essas pistas estruturais foram incorporadas ao sistema de classificação, ajudando a mover algumas variantes limítrofes para categorias mais prováveis de serem danosas ou mais prováveis de serem benignas. Essa ponte entre modelagem molecular e dados clínicos leva o teste genético além da leitura simples do código rumo a uma compreensão mais funcional.
O que isso significa para pacientes e famílias
Para famílias afetadas pela cardiomiopatia arritmogênica, este estudo oferece tanto cautela quanto orientação. Mostra que nem toda variante da desmogleína‑2 é uma sentença de doença cardíaca severa, mas que certos padrões — especialmente múltiplos impactos ou alterações em regiões críticas da proteína — estão ligados a problemas mais precoces e mais graves. Os autores argumentam que pessoas portadoras dessas variantes não devem ser descartadas como “saudáveis até prova em contrário”, mas sim acompanhadas ao longo da vida com exames de ritmo e imagem personalizados. A abordagem integrativa deles — que mistura genética de grandes bases de dados, estudos familiares detalhados e estrutura proteica — aponta o caminho para estimativas de risco mais precisas e aconselhamento mais confiante quando uma alteração em desmogleína‑2 aparece em um teste genético.
Citação: Pinci, S., Celeghin, R., Martini, M. et al. Integrative genomic and literature assessment of desmoglein 2-related arrhythmogenic cardiomyopathy with Italian cohort validation. Commun Med 6, 145 (2026). https://doi.org/10.1038/s43856-026-01416-w
Palavras-chave: cardiomiopatia arritmogênica, desmogleína-2, doença cardíaca hereditária, risco genético, morte súbita cardíaca