Clear Sky Science · pt
Bloqueio seletivo da ativação latente de TGF-β1 suprime fibrose tecidual com boa segurança
Por que a cicatrização oculta importa
Muitas doenças crônicas danificam silenciosamente nossos órgãos ao depositar tecido cicatricial rígido, um processo chamado fibrose. Essa cicatrização pode gradualmente comprometer a função normal do fígado, rins, pulmões e até ao redor de tumores, onde também pode reduzir os efeitos das imunoterapias modernas contra o câncer. A proteína TGF-β1 está no centro desse processo de formação de cicatriz, mas bloqueá-la em todo o corpo mostrou-se perigoso. Este estudo descreve um novo anticorpo, chamado SOF10, projetado para bloquear apenas a ativação prejudicial de TGF-β1 enquanto preserva suas funções essenciais, mostrando benefícios promissores em modelos animais de doença hepática, insuficiência renal e câncer.
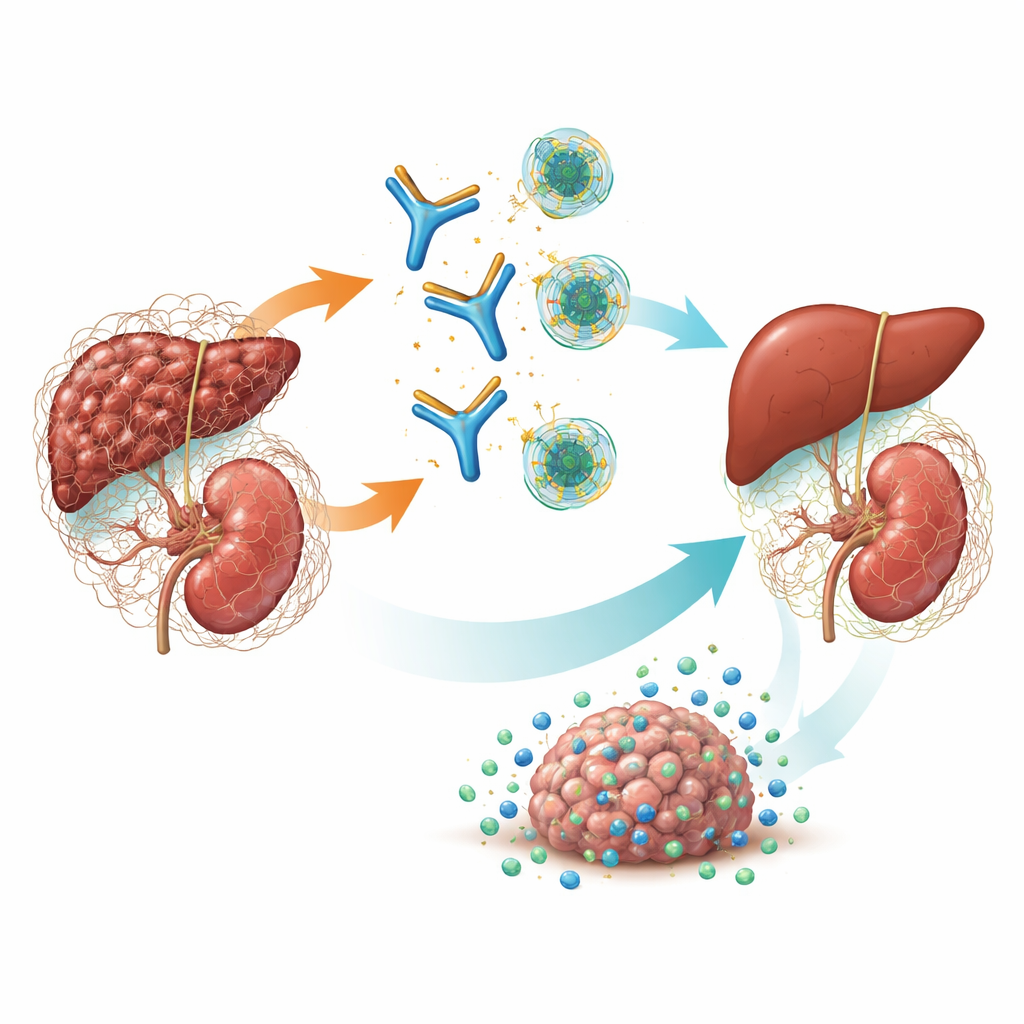
Um interruptor mestre para cicatrização e câncer
TGF-β é uma molécula de sinalização poderosa que ajuda a controlar como as células crescem, cicatrizam e interagem com o sistema imune. Em doenças crônicas, uma forma—TGF-β1—conduz os fibroblastos a construir tecido conjuntivo em excesso, levando ao enrijecimento e falência dos órgãos. Ela também molda uma cápsula fibrosa e imunossupressora ao redor de tumores que impede que células imunes e medicamentos alcancem as células cancerosas. Drogas anteriores tentaram desligar as três formas de TGF-β ao mesmo tempo, mas esse “bloqueio pan” causou efeitos colaterais graves, como danos nas válvulas cardíacas, hemorragias e tumores cutâneos. Estudos genéticos e modelos prévios sugeriram que TGF-β1 é a principal responsável pela fibrose renal e por muitos tumores sólidos, levantando a possibilidade de que direcionar cuidadosamente apenas essa isoforma possa ser eficaz e mais seguro.
Trancando o TGF-β1 em sua forma inativa
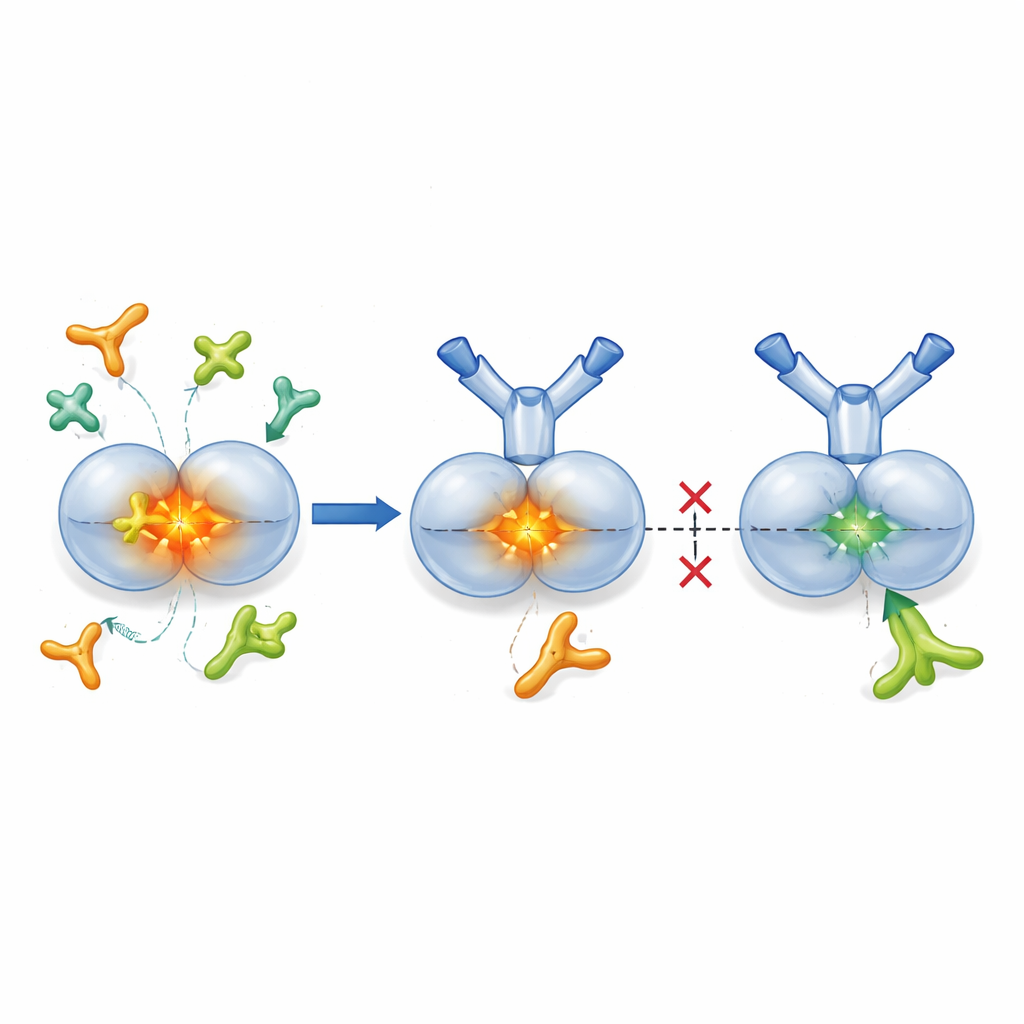
TGF-β1 é normalmente produzido em um pacote “latente”, em que o núcleo ativo é envolto por uma proteína parceira que o mantém inativo até ser necessário. Enzimas chamadas proteases e certas proteínas de superfície celular conhecidas como integrinas podem abrir esse pacote, liberando TGF-β1 ativo no tecido próximo. Os pesquisadores desenvolveram o SOF10, um anticorpo humanizado que se liga apenas à forma latente de TGF-β1, não ao hormônio ativo nem a outras isoformas. Estudos estruturais por cristalografia de raios X mostraram que o SOF10 se encaixa na interface entre duas metades do complexo latente, estabilizando-o como uma braçadeira. Em testes de laboratório, isso impediu que proteases e uma integrina (αvβ8) liberassem TGF-β1 ativo, ao mesmo tempo em que deixou outra integrina (αvβ6)—importante para manter o equilíbrio imune em tecidos saudáveis—em grande parte intocada. Na prática, o SOF10 silenciosamente bloqueia as rotas de ativação prejudiciais enquanto preserva uma via homeostática chave.
Protegendo fígado e rins de danos lentos
Para verificar se essa braçadeira seletiva sobre TGF-β1 poderia realmente limitar a formação de cicatrizes, a equipe testou o SOF10 em vários modelos de camundongos. Em um modelo dietético rápido de doença hepática gordurosa que progride para fibrose hepática, o tratamento com SOF10 reduziu a expressão hepática de genes responsivos a TGF-β e de genes de síntese de colágeno, além de diminuir os níveis de hidroxiprolina, um marcador químico de acúmulo de tecido cicatricial. Em dois modelos renais diferentes—um modelo cirúrgico de obstrução que promove fibrose intersticial e um modelo genético da síndrome de Alport que desenvolve tanto cicatrização glomerular quanto insuficiência renal—o SOF10 reduziu a atividade de genes fibróticos, diminuiu o conteúdo de colágeno e reduziu visivelmente as áreas cicatrizadas ao microscópio. No modelo crônico de Alport, exames sanguíneos mostraram melhora da função renal, e esses benefícios foram equivalentes aos observados com um anticorpo bloqueador amplo de TGF-β, porém sem bloquear outras isoformas de TGF-β.
Libertando o sistema imune dentro dos tumores
Como o tecido fibrótico ao redor de tumores pode atuar tanto como uma barreira física quanto como um freio imune, os pesquisadores investigaram se o SOF10 poderia melhorar as respostas aos medicamentos inibidores de checkpoint. Em modelos murinos de câncer de mama e cólon que normalmente respondem mal à terapia anti–PD-L1, a adição de SOF10 retardou significativamente o crescimento tumoral, enquanto SOF10 ou anti–PD-L1 isoladamente tiveram pouco efeito. Tumores de animais tratados com a combinação continham mais células T CD8 assassinas e mais das enzimas tóxicas que elas usam para destruir células cancerosas. Fibroblastos retirados desses tumores mostraram menor atividade em vias de síntese de colágeno e matriz, mas maior atividade em vias de interferon e apresentação de antígeno, uma mudança para uma estroma mais favorável ao sistema imune. Essas alterações refletiram de forma próxima o que foi observado com bloqueio amplo de TGF-β, sugerindo que direcionar apenas o TGF-β1 latente pode reprogramar o ambiente tumoral de maneira semelhante.
Sinais de segurança em animais
Como tentativas anteriores de bloquear TGF-β de forma ampla enfrentaram problemas de segurança, a equipe realizou estudos de toxicidade de 13 semanas em camundongos e macacos cynomolgus, administrando doses repetidas e altas de SOF10. O fármaco comportou-se como um anticorpo típico na corrente sanguínea e, em uma ampla faixa de doses, não houve sinais de dano em órgãos principais, contagem de células sanguíneas ou função cardíaca e pulmonar. As doses mais altas testadas—até 200 mg/kg a cada duas semanas em camundongos e 100 mg/kg em macacos—foram designadas como níveis sem efeitos nocivos observados. Esse perfil de segurança sustenta a ideia de que poupar TGF-β2, TGF-β3 e a ativação mediada por αvβ6 reduz os riscos vistos com abordagens anteriores, menos seletivas.
O que isso pode significar para pacientes
Em conjunto, os achados sugerem que trancar o TGF-β1 em sua casca inativa—em vez de eliminar toda a sinalização de TGF-β—pode reduzir a cicatrização em múltiplos órgãos, melhorar a função renal e tornar tumores resistentes mais vulneráveis à imunoterapia, tudo isso com segurança encorajadora em testes animais. Embora ensaios em humanos sejam necessários para confirmar esses benefícios e monitorar efeitos a longo prazo, o SOF10 e estratégias semelhantes podem abrir uma nova via para tratar doenças fibróticas crônicas e certos cânceres, reduzindo a cicatrização prejudicial ao mesmo tempo em que preservam os papéis de cura e equilíbrio imunológico que nossos tecidos ainda requerem.
Citação: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
Palavras-chave: fibrose, TGF-beta1, anticorpo monoclonal, doença renal e hepática, imunoterapia contra o câncer