Clear Sky Science · pt
Caracterização genômica e subagrupamento do complexo clonal Escherichia coli 38 revelam marcadores genéticos associados ao hospedeiro
Por que isso importa para o dia a dia
Infecções resistentes a antibióticos deixaram de ser um problema distante restrito a hospitais — elas afetam cada vez mais a alimentação, os animais, as viagens e a vida comunitária. Este estudo foca em um grupo específico de bactérias Escherichia coli, chamado complexo clonal 38 (CC38), que pode causar infecções graves na corrente sanguínea e no trato urinário e frequentemente resiste aos nossos antibióticos mais importantes. Ao rastrear de onde essas bactérias vêm e como se movem entre humanos, animais e o ambiente, os pesquisadores revelam pistas que podem ajudar as autoridades de saúde a interromper cepas perigosas antes que se espalhem amplamente.
Um olhar mais atento sobre uma família bacteriana problemática
Nem todas as E. coli são nocivas, mas algumas linhagens são reincidentes em doenças graves. O CC38 emergiu recentemente como um desses grupos problemáticos, ficando em segundo lugar, atrás de uma linhagem de alto risco bem conhecida (ST131), em infecções sanguíneas na Dinamarca. A equipe examinou 242 CC38 resistentes de pacientes dinamarqueses, 83 provenientes de alimentos e animais de criação, e mais de 2.300 genomas relacionados coletados mundialmente. Eles usaram sequenciamento do genoma completo — essencialmente lendo o DNA de cada bactéria — para mapear como diferentes ramos dessa família estão relacionados, quais genes de resistência carregam e em quais hospedeiros tendem a viver.
Seguindo a trilha de hospitais a fazendas e alimentos
Quando os pesquisadores compararam E. coli CC38 de pacientes dinamarqueses com amostras de aves, animais de criação e alimentos, encontraram dois grupos principais na Dinamarca. Um grupo era composto majoritariamente por infecções humanas, enquanto o outro continha bactérias de aves, outros animais de criação e produtos alimentícios. Importante: não houve correspondências de DNA quase idênticas entre isolados humanos e animais, sugerindo que não ocorreram surtos alimentares claros na Dinamarca durante o período do estudo. Contudo, modelos estatísticos que analisam segmentos de DNA acessório indicaram que alguns subgrupos associados a humanos provavelmente têm origem em aves, apontando para episódios passados ou derramamentos indiretos de galinhas para pessoas.
Uma árvore genealógica global com dois grandes ramos
Ampliando para um conjunto de dados mundial com 2.638 genomas, a equipe construiu uma “árvore genealógica” global para o CC38. Dois ramos principais se destacaram. Um estava fortemente associado a aves e apresentava níveis moderados de resistência a medicamentos, além de muitos traços ligados a doença grave. O outro era dominado por subgrupos associados a humanos que diferiam em resistência, potencial de causar doenças e hospedeiros preferenciais. Alguns subgrupos eram claramente centrados em humanos e altamente resistentes, enquanto outros mostraram padrões mistos, aparecendo em humanos, aves, vida selvagem, água e animais de companhia. Esse mosaico reflete a capacidade do CC38 de se adaptar a diferentes ambientes e espécies hospedeiras, complicando os esforços de controle.
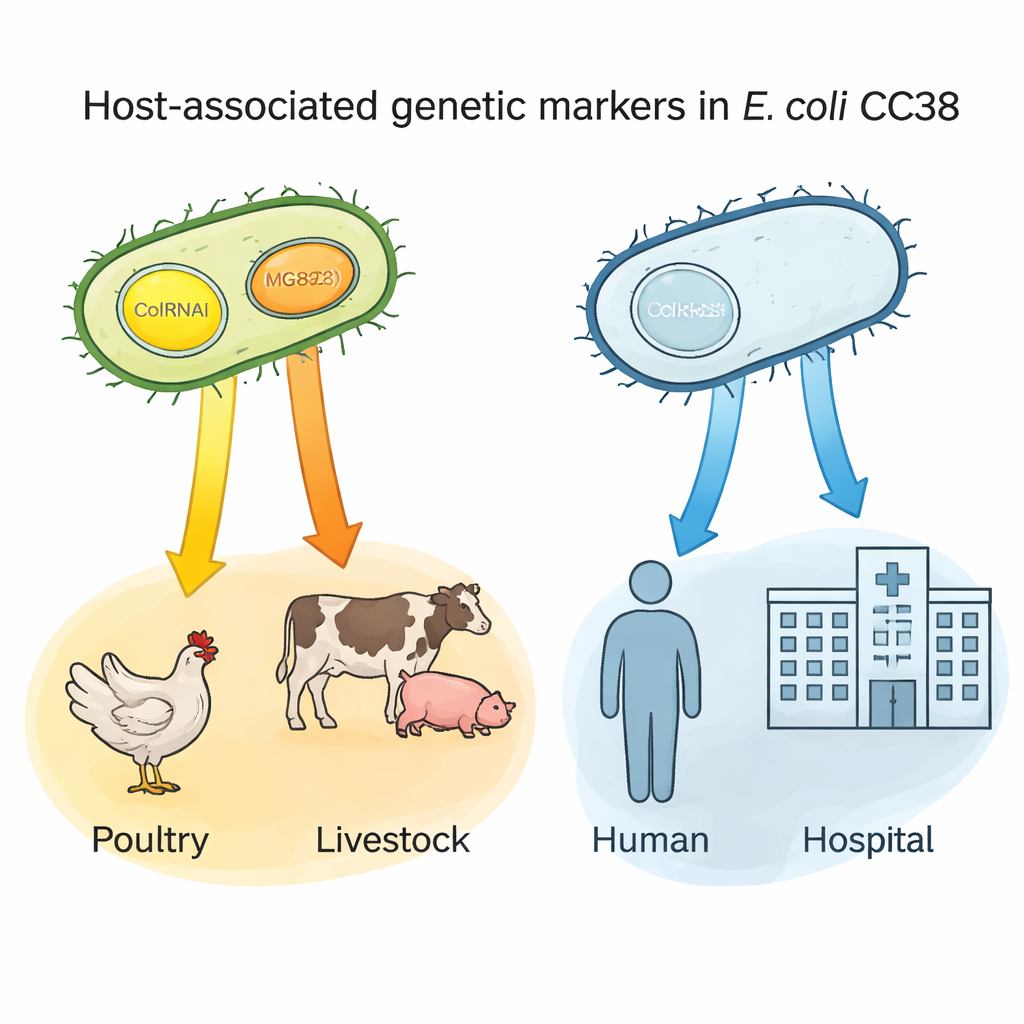
Pequenos círculos de DNA como “etiquetas” de hospedeiro
Uma descoberta chave envolveu dois pequenos pedaços de DNA — plasmídeos chamados ColRNAI e Col(MG828) — que podem se mover entre bactérias. Esses plasmídeos eram comuns em CC38 de aves e outros animais de criação, mas raros nos subgrupos centrados em humanos. Usando análise estatística, os autores mostraram que portar qualquer um desses plasmídeos previa fortemente uma origem em aves; portar ambos juntos era especialmente característico de linhagens ligadas a animais de criação e a certas fontes alimentares. Como esses plasmídeos frequentemente também carregam traços de resistência, eles podem atuar como “etiquetas” genéticas que sinalizam bactérias provavelmente originárias de reservatórios animais e ajudar a rastrear como cepas resistentes entram na cadeia alimentar e alcançam pessoas.
O que isso significa para proteger a saúde
Para um público não especialista, a mensagem principal é que E. coli nocivas e resistentes a medicamentos não ficam confinadas a hospitais ou pacientes: elas formam populações interconectadas que abrangem humanos, aves, animais de criação, vida selvagem, alimentos e o ambiente. Este estudo mostra que, dentro de uma linhagem importante, o CC38, alguns ramos estão fortemente ligados a animais e outros a humanos, e que elementos genéticos móveis específicos podem ajudar a revelar de onde provavelmente veio uma cepa. Usar esses marcadores genéticos na vigilância de rotina pode fornecer aviso prévio quando bactérias resistentes associadas a animais começarem a aparecer em pessoas. Isso, por sua vez, apoia uma abordagem “One Health” — tratando a saúde humana, animal e ambiental como partes de um mesmo sistema — para desenhar estratégias mais inteligentes e direcionadas de prevenção de infecções e de desaceleração da disseminação da resistência a antibióticos.
Citação: Roer, L., Rasmussen, A., Hansen, F. et al. Genomic characterization and sub-clustering of Escherichia coli clonal complex 38 reveal host associated genetic markers. Commun Med 6, 126 (2026). https://doi.org/10.1038/s43856-026-01402-2
Palavras-chave: resistência antimicrobiana, Escherichia coli, transmissão zoonótica, aves e animais de criação, vigilância genômica