Clear Sky Science · pt
Predição do desfecho a partir do perfil proteico espacial de carcinomas de mama triple-negativos
Por que a disposição das células cancerosas importa
Quando os médicos examinam um câncer de mama agressivo ao microscópio, veem uma paisagem densa de células tumorais, células imunes e tecido de sustentação. Mas até recentemente, a maioria dos testes se concentrou em quanto de uma determinada molécula está presente, e não em onde ela se localiza. Este estudo mostra que o arranjo físico de proteínas e células dentro de carcinomas de mama triple-negativos pode prever o prognóstico dos pacientes e apresenta uma nova maneira de ler esses padrões espaciais diretamente a partir de imagens de alta resolução.
Ver o tecido tumoral em muitas cores
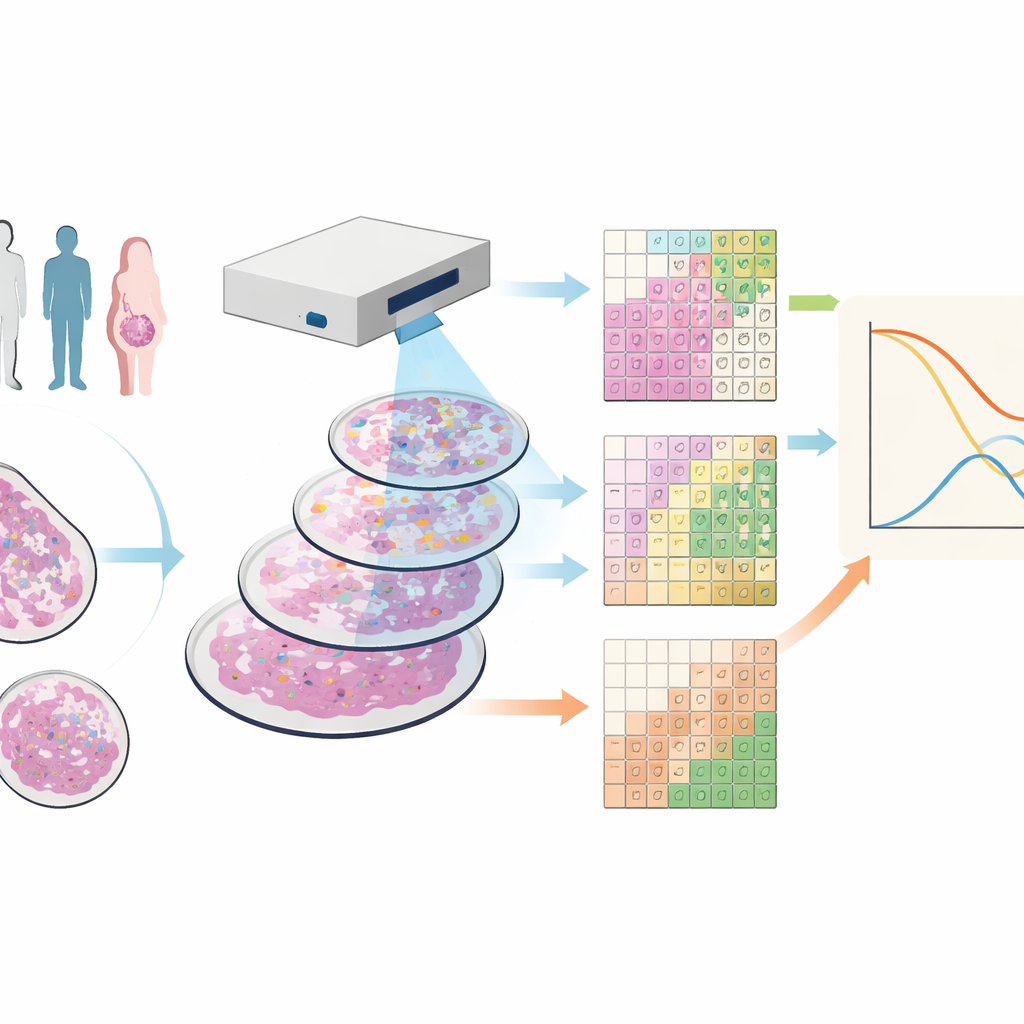
Os pesquisadores trabalharam com amostras de tecido de 88 pessoas com câncer de mama triple-negativo, uma forma da doença que carece de alvos farmacológicos comuns e frequentemente tem prognóstico ruim. Eles usaram uma técnica chamada citometria de massa por imagem, que marca cada amostra com dezenas de anticorpos ligados a metais. Em um scanner especializado, isso gera imagens em que cada ponto do tecido tem uma assinatura detalhada de muitas proteínas diferentes, revelando ao mesmo tempo células tumorais, vários tipos de células imunes, vasos sanguíneos e fibras estruturais.
Dividir a imagem em blocos em vez de células
A maioria das ferramentas atuais tenta traçar limites ao redor de cada célula e então classificá-las por tipo, um processo que pode ser sujeito a erro e demorado, especialmente em cortes finos de tecido onde células aparecem parcialmente. A equipe criou em vez disso o SparTile, um método que dispensa o contorno individual das células. O SparTile fragmenta cada imagem em muitos quadrados pequenos e sobrepostos, ou tiles, e usa técnicas matemáticas para aprender padrões recorrentes de combinações de proteínas dentro desses tiles. Primeiro agrupa os tiles em regiões amplas — tumor, tecido de suporte (estroma) ou zonas ricas em células imunes — e depois subdivide cada região em “microambientes” mais específicos, cada qual com sua própria mistura de proteínas e tipos celulares vizinhos.
Bairros ocultos ligados ao desfecho do paciente
Com esses microambientes mapeados, os cientistas mediram quanto de cada padrão aparecia na amostra de cada paciente e compararam isso com a sobrevida a longo prazo. Surgiram várias associações marcantes. Um microambiente centrado no tumor, rico na proteína chamada MX1 e em marcadores de células imunes mieloides, associou-se a um risco de morte muito maior. Outro padrão tumoral marcado por vimentina — sinal de que as células tumorais mudaram para um estado mais móvel e invasivo — também se correlacionou fortemente com sobrevida ruim. Em contraste, áreas dominadas por certos linfócitos T ligaram-se a desfechos melhores, enquanto regiões ricas em células B mostraram efeitos mais fracos, possivelmente porque eram raras nos pequenos núcleos de tecido analisados.
Distância entre células tumorais e imunes como sinal de alerta
Além da presença de determinados bairros, as relações espaciais entre eles também importaram. A equipe avaliou quão próximas regiões tumorais e regiões mieloides-ricas ficavam umas das outras calculando uma medida estatística de quanto os sinais proteicos se sobrepunham no espaço. Pacientes cujos tumores tinham áreas ricas em mieloides imersas entre células tumorais tenderam a evoluir pior do que aqueles em que as duas populações estavam mais separadas. Essa medida de “distância” permaneceu um preditor robusto de risco mesmo após ajustar por fatores clínicos padrão, e sua importância se manteve quando testada em dois conjuntos de imagens de câncer de mama independentes de outros grupos de pesquisa.
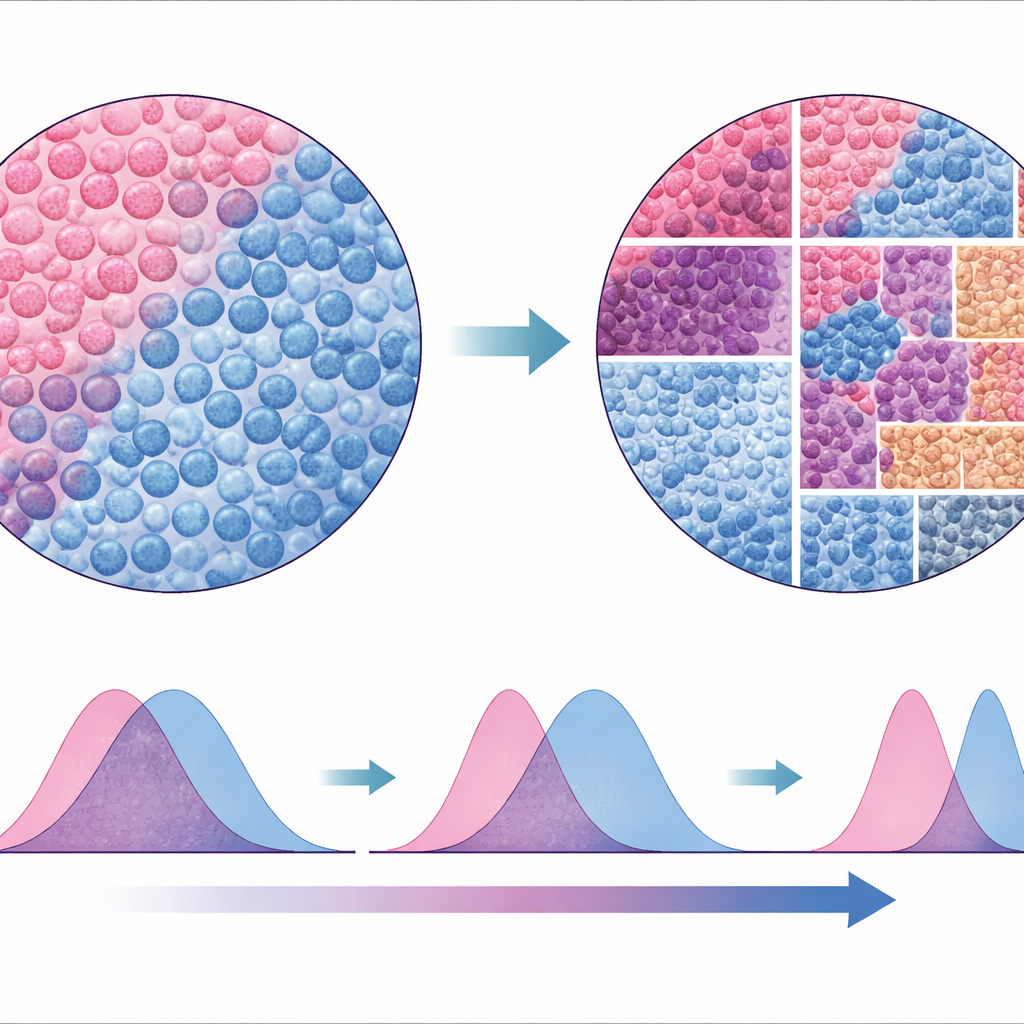
Uma nova forma de ler a paisagem tumoral
Para testar a robustez de sua abordagem, os autores compararam o SparTile com métodos tradicionais que dependem da segmentação e classificação de células individuais e da então construção de vizinhanças ao redor delas. Embora as análises baseadas em células tenham recuperado alguns dos mesmos padrões, foram menos consistentes entre conjuntos de dados e menos confiáveis para sinalizar certos microambientes de risco, como aqueles envolvendo MX1 e células mieloides. Como o SparTile trabalha diretamente sobre as imagens brutas de proteínas, ele evita muitas das suposições e armadilhas técnicas das abordagens célula a célula, mas ainda pode ser combinado com elas posteriormente quando tipos celulares detalhados forem necessários para planejar experimentos ou terapias.
O que isso significa para pacientes e cuidados futuros
Este trabalho mostra que não só os ingredientes, mas também a disposição de um tumor importam para prever a evolução de um paciente com câncer de mama triple-negativo. Ao converter imagens complexas com múltiplas proteínas em padrões espaciais interpretáveis e medidas de distância simples, o SparTile oferece uma forma de identificar pacientes de alto risco a partir de pequenas amostras de tecido e de revelar arranjos biológicos que podem ser alvos de tratamentos futuros. Embora sejam necessárias mais validações antes que possa orientar a prática clínica rotineira, a abordagem aponta para um futuro em que o “mapa” de um tumor se torne tão importante quanto sua lista de componentes moleculares.
Citação: Foroughi pour, A., Wu, TC., Noorbakhsh, J. et al. Prediction of outcome from spatial Protein profiling of triple-negative breast cancers. Commun Med 6, 133 (2026). https://doi.org/10.1038/s43856-026-01400-4
Palavras-chave: câncer de mama triple-negativo, microambiente tumoral, proteômica espacial, citometria de massa por imagem, biomarcadores prognósticos