Clear Sky Science · pt
IdentifiHR prevê deficiência de recombinação homóloga em carcinoma seroso de alto grau usando expressão gênica
Por que esta pesquisa importa para pacientes com câncer de ovário
Para pessoas com carcinoma seroso de alto grau, uma das formas mais letais de câncer de ovário, as escolhas de tratamento podem ser uma questão de vida ou morte. Cerca de metade desses tumores apresenta uma fraqueza na forma de reparar DNA danificado, o que os torna especialmente sensíveis a determinados fármacos chamados inibidores de PARP. O desafio é determinar, para cada paciente, se o tumor tem essa vulnerabilidade. Este estudo apresenta o IdentifiHR, uma nova ferramenta que interpreta padrões de atividade gênica, em vez de se basear apenas em mutações de DNA, para prever quais tumores têm reparo de DNA defeituoso e poderiam se beneficiar mais desses tratamentos direcionados.
De cicatrizes no DNA a padrões de atividade gênica
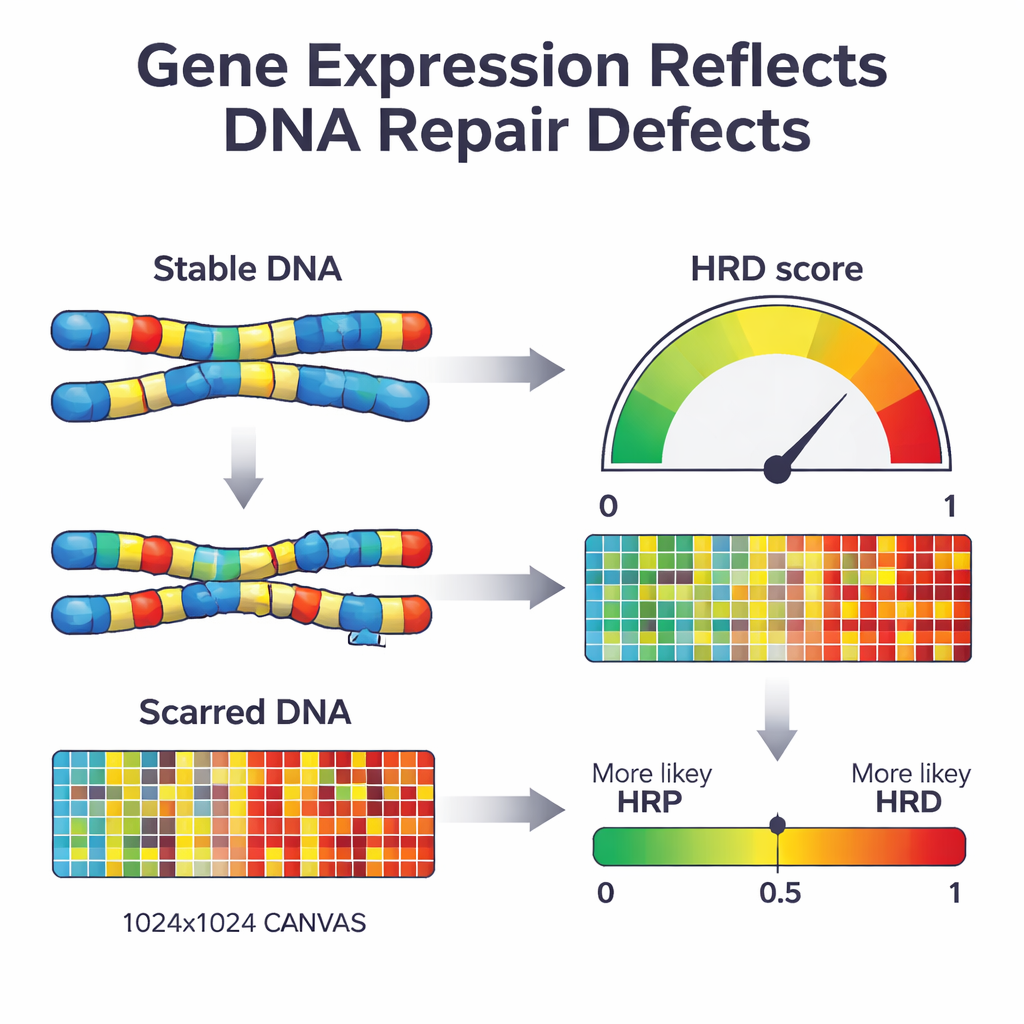
Quando uma célula perde uma via importante de reparo chamada recombinação homóloga, ela começa a consertar o DNA usando métodos mais propensos a erros. Com o tempo isso deixa um padrão característico de “cicatrizes” pelo genoma — regiões ausentes, cópias extras e segmentos cromossômicos quebrados. Testes clínicos existentes procuram essas cicatrizes diretamente no DNA ou por mutações específicas em genes-chave como BRCA1 e BRCA2. Embora poderosos, esses testes exigem sequenciamento extenso do DNA e nem sempre capturam o estado atual de reparo do tumor. Os autores perguntaram se uma camada diferente da biologia — o padrão de genes ligados ou desligados no tumor — poderia funcionar como uma leitura em tempo real desse dano e ser usada para classificar tumores como deficientes ou proficientes em reparo.
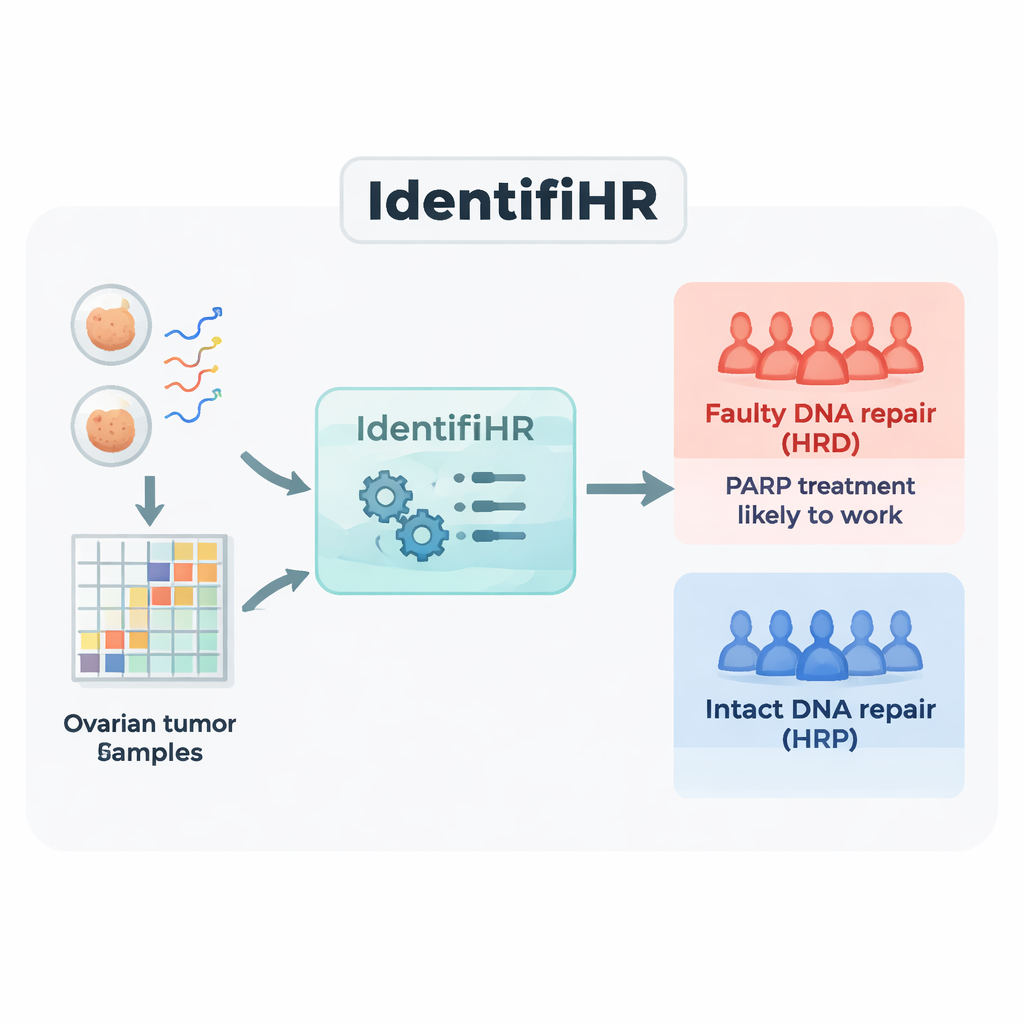
Construindo um preditor baseado em genes, IdentifiHR
A equipe começou com dados de RNA-seq de 361 tumores ovarianos em um grande recurso público, The Cancer Genome Atlas. O sequenciamento de RNA mede quais genes estão ativos, e em que grau, em cada amostra. Eles dividiram os tumores em um grupo de treinamento e um de teste, rotulando cada caso como deficiente em reparo (HRD) ou proficiente em reparo (HRP) usando o padrão atual baseado em DNA que combina várias medidas de cicatrizes genômicas. Nos tumores de treinamento, identificaram 2.604 genes cuja atividade diferia consistentemente entre cânceres HRD e HRP. Muitos desses genes estavam em regiões do genoma já conhecidas por serem repetidamente ganhas ou perdidas em tumores com defeito de reparo, mostrando que o sinal de expressão gênica ecoava o dano subjacente no DNA.
Uma assinatura de 209 genes que acompanha o status de reparo
Em seguida, os pesquisadores usaram uma abordagem de aprendizado de máquina conhecida como regressão logística penalizada para comprimir essa lista de 2.604 genes até o conjunto mais informativo. O modelo resultante, que nomearam IdentifiHR, baseia-se na atividade de apenas 209 genes para estimar a probabilidade de um tumor ser deficiente em reparo. Curiosamente, apenas um desses genes é um gene clássico de reparo de DNA; a maioria são genes comuns cuja atividade é alterada devido a mudanças mais amplas na estrutura cromossômica. O IdentifiHR não fornece apenas um rótulo sim/não — ele produz um escore de probabilidade que varia de forma contínua com o escore de dano baseado em DNA subjacente, refletindo a ideia de que a deficiência de reparo existe em um espectro, e não como um estado estritamente ligado/desligado.
Testando a ferramenta em múltiplas coortes de pacientes
Os autores testaram rigorosamente o IdentifiHR em três conjuntos de dados independentes que nunca haviam sido usados no treinamento. No subconjunto retido de The Cancer Genome Atlas, o modelo distinguiu corretamente tumores HRD de HRP em cerca de 85% dos casos. Teve desempenho similar — cerca de 86% de acurácia — em um estudo australiano separado que incluiu não apenas tumores primários, mas também amostras coletadas em autópsia, de líquido abdominal (ascite) e de trompas de Falópio normais, o provável local onde muitos desses cânceres começam. Em todas as amostras de trompa de Falópio normal, o IdentifiHR previu corretamente reparo de DNA intacto. A ferramenta também funcionou em dados de célula única “pseudoagregados”, onde milhares de células cancerosas individuais foram combinadas computacionalmente para imitar uma amostra de bulk, alcançando novamente cerca de 84% de acurácia. Nessas avaliações, o IdentifiHR igualou ou superou o desempenho de vários métodos existentes baseados em genes originalmente desenvolvidos para outros cânceres ou para prever escores de dano relacionados.
Como isso pode mudar pesquisa e atendimento
Porque o IdentifiHR roda a partir de dados de RNA, que costumam ser mais baratos e fáceis de coletar que perfis completos do genoma, ele oferece uma maneira prática para pesquisadores — e, potencialmente, no futuro, clínicos — estimarem o status de reparo de DNA quando apenas dados de expressão gênica estão disponíveis. O modelo é distribuído como um pacote R de código aberto, de modo que qualquer grupo com dados de sequenciamento adequados pode aplicá-lo. Embora ainda não substitua os testes de DNA padrão-ouro, e sua capacidade de captar mudanças mais sutis, como restauração do reparo, precise de estudos adicionais, o IdentifiHR fornece uma nova e poderosa lente para identificar quais tumores ovarianos têm maior probabilidade de responder a inibidores de PARP e fármacos similares. Para os pacientes, esse trabalho aproxima o campo de decisões de tratamento mais precisas e guiadas pela biologia real do comportamento das células tumorais.
Citação: Weir, A.L., Lee, S.C., Li, M. et al. IdentifiHR predicts homologous recombination deficiency in high-grade serous ovarian carcinoma using gene expression. Commun Med 6, 119 (2026). https://doi.org/10.1038/s43856-026-01387-y
Palavras-chave: câncer de ovário, reparo de DNA, deficiência de recombinação homóloga, expressão gênica, aprendizado de máquina