Clear Sky Science · pt
Deficiência na recombinação homóloga em câncer de mama primário com receptor de estrógeno positivo e HER2 negativo
Por que isso importa para pacientes com câncer de mama
A maioria dos cânceres de mama pertence a um grande grupo chamado receptor de estrógeno positivo e HER2 negativo. Esses tumores costumam ser tratados com medicamentos que bloqueiam hormônios, às vezes combinados com quimioterapia. Ainda assim, muitos pacientes têm recidiva, e os médicos carecem de ferramentas precisas para decidir quem realmente precisa de tratamento intensivo ou poderia se beneficiar de novos medicamentos direcionados. Este estudo explora uma fraqueza específica em alguns tumores — chamada deficiência na recombinação homóloga, ou HRD — que torna as células cancerígenas deficientes no reparo de quebras no DNA, potencialmente abrindo caminho para um tratamento mais personalizado.
Uma fraqueza oculta em apenas alguns tumores
A recombinação homóloga é um dos principais sistemas da célula para consertar quebras perigosas no DNA. Quando esse sistema falha — frequentemente por defeitos em genes bem conhecidos como BRCA1, BRCA2, PALB2 ou RAD51C — as células acumulam mutações e podem ficar especialmente sensíveis a certos medicamentos, incluindo quimioterapias à base de platina e inibidores de PARP. A HRD é comum em uma forma agressiva de câncer de mama chamada triplo negativo, mas seu papel no grupo mais comum receptor de estrógeno positivo, HER2 negativo, tem sido incerto. Para esclarecer isso, os pesquisadores analisaram 502 desses tumores do estudo sueco SCAN‑B usando sequenciamento do genoma completo, juntamente com dados combinados sobre atividade gênica, metilação do DNA, tratamentos recebidos e desfechos de longo prazo.
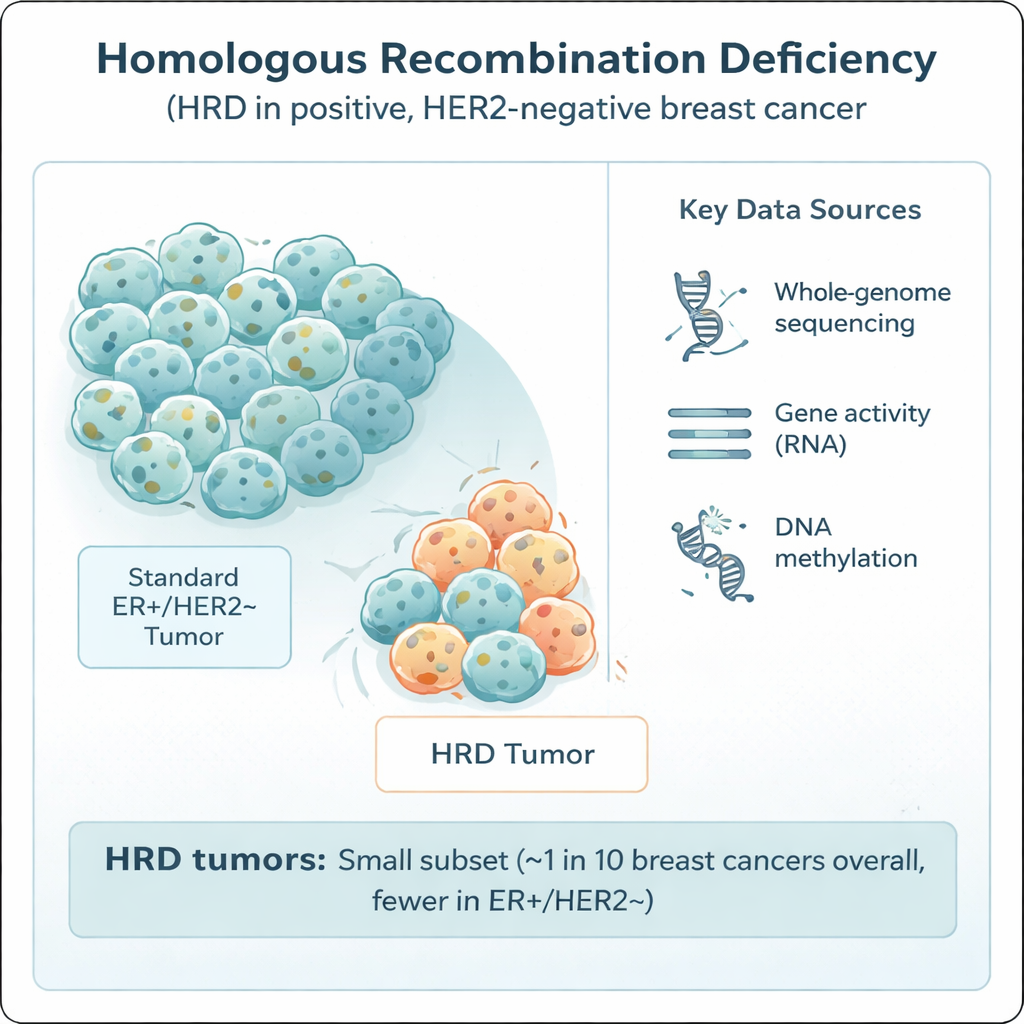
Como o estudo foi conduzido
Todos os tumores foram coletados no momento da cirurgia, antes de qualquer tratamento medicamentoso, fornecendo um retrato claro de sua biologia original. A equipe usou uma ferramenta sofisticada de reconhecimento de padrões, HRDetect, para ler as “assinaturas mutacionais” deixadas no DNA do câncer quando a recombinação homóloga está quebrada. Os tumores foram rotulados como HRD se ultrapassassem um limite rigoroso de probabilidade. Os cientistas também compararam diferentes formas de detectar HRD — desde outros escores baseados em DNA até um teste de expressão gênica baseado em RNA — para ver quão confiáveis e concordantes são os métodos. Além disso, examinaram características mais amplas, como carga total de mutações, padrões de ganhos e perdas cromossômicas, atividade de genes relacionados ao sistema imune e marcas químicas no DNA (metilação) que podem ligar ou desligar genes.
Quão comum é a HRD e o que a causa?
Os pesquisadores descobriram que apenas 8,4% dos tumores receptor de estrógeno positivo, HER2 negativo em seu grupo sequenciado apresentaram evidência forte de HRD — bem abaixo dos cerca de 60% observados na doença triplo negativa. Ao combinar esses dados com informações de registros nacionais e outros estudos, estimaram que cerca de 1 em 20 tumores desse subgrupo clínico, e aproximadamente 1 em 9 cânceres de mama no geral em populações da Europa Ocidental/Nórdica, são HRD. Nos tumores HRD, eles frequentemente conseguiram identificar uma causa provável: cerca de 70% apresentavam danos claros em BRCA1, BRCA2, RAD51C ou PALB2, por meio de mutações hereditárias, mutações ou deleções específicas do tumor, ou silenciamento epigenético de promotores gênicos. Notavelmente, cerca de um terço dos casos HRD se deveu à hipermetilação do promotor — um revestimento químico adicional que desativa genes de reparo de DNA sem alterar sua sequência. No entanto, aproximadamente 30% dos tumores HRD não apresentaram um único evento óbvio, sugerindo vias adicionais, ainda desconhecidas, para essa falha de reparo.
Como os tumores HRD se apresentam ao microscópio e na clínica
Os tumores HRD nesse grupo comum de câncer de mama tenderam a mostrar características de doença mais agressiva: frequentemente tinham taxas mais altas de divisão celular, níveis mais baixos de coloração dos receptores hormonais e genomas mais complexos e ricos em mutações do que tumores proficientes em recombinação homóloga. Eles apareceram em quase todos os principais subtipos moleculares, mas eram raros na classe mais indolente Luminal A e relativamente mais frequentes em um subconjunto menor do tipo basal‑like. Ainda assim, quando os pesquisadores analisaram a atividade gênica global e os padrões de metilação do DNA, os tumores HRD não se agrupavam em um único perfil facilmente reconhecível. Em vez disso, seus padrões de expressão foram diversos, e quaisquer diferenças dentro de subtipos específicos foram modestas. Alguns tumores HRD, especialmente nos grupos Luminal B e basal‑like, mostraram sinais mais altos de atividade imune e expressão aumentada de PD‑L1, sugerindo que podem ser mais visíveis ao sistema imune e potencialmente mais responsivos à imunoterapia.
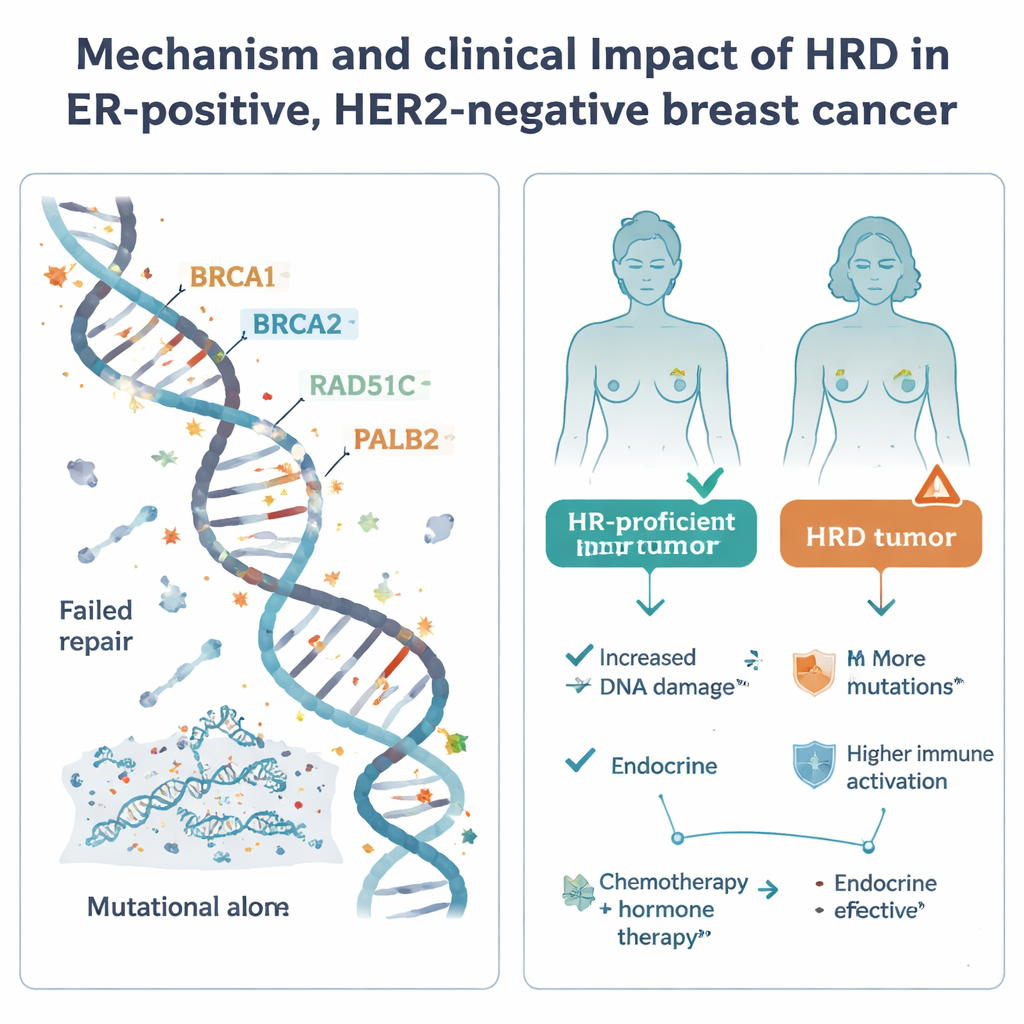
A HRD altera os desfechos dos pacientes?
O estudo examinou então como o status HRD se relacionou com desfechos do mundo real sob o cuidado padrão. Em pacientes tratadas apenas com terapia hormonal após a cirurgia, tumores HRD mostraram uma tendência a pior sobrevida livre de recidiva distante, embora o número de casos HRD fosse pequeno e o resultado não tenha alcançado significância estatística formal. Esse padrão, junto com as características moleculares agressivas, sugere que confiar apenas na terapia endócrina pode ser arriscado para pacientes cujos tumores são HRD. Em contraste, entre pacientes que receberam quimioterapia e terapia hormonal, o status HRD não se relacionou claramente com desfechos melhores ou piores; todos os grupos tiveram taxas de recidiva amplamente semelhantes, e a quimioterapia pode estar mitigando parte do risco adicional nos tumores HRD.
O que isso significa para escolhas de tratamento futuras
Para um leitor geral, a mensagem principal é que apenas uma minoria dos cânceres de mama receptor de estrógeno positivo, HER2 negativo, apresenta essa fraqueza específica no reparo do DNA, mas quando presente tende a indicar doença mais agressiva que pode não ser bem controlada apenas pela terapia hormonal. O trabalho apoia a ideia de que o sequenciamento do genoma completo pode identificar de forma confiável a HRD e esclarecer suas causas subjacentes, além de apenas testar mutações hereditárias em BRCA1 ou BRCA2. Embora o estudo ainda não prove que mudar o tratamento com base no status HRD melhora a sobrevida, ele fornece evidências iniciais de que pacientes com tumores HRD podem se beneficiar de quimioterapia e, em futuros ensaios, de inibidores de PARP ou imunoterapias. Em resumo, o teste de HRD poderia se tornar mais uma peça de uma caixa de ferramentas refinada para ajustar a intensidade do tratamento — e opções direcionadas novas — à biologia do câncer de mama de cada paciente.
Citação: Davies, H.R., Black, D., Kvist, A. et al. Homologous recombination deficiency in primary ER-positive and HER2-negative breast cancer. Commun Med 6, 118 (2026). https://doi.org/10.1038/s43856-026-01385-0
Palavras-chave: câncer de mama, reparo de DNA, genes BRCA, sequenciamento do genoma, terapia direcionada