Clear Sky Science · pt
Assinatura estrutural de proteínas plasmáticas classifica o estado da doença de Alzheimer
Por que um exame de sangue para perda de memória importa
A doença de Alzheimer costuma estar bem estabelecida muito antes de os problemas de memória ficarem evidentes, mas os testes atuais para detectá‑la precocemente podem ser invasivos, caros ou de difícil acesso. Este estudo explora uma ideia diferente: se pequenas alterações nas formas tridimensionais das proteínas circulantes no sangue podem revelar em que ponto alguém se encontra no trajeto do envelhecimento saudável para o esquecimento leve até a doença de Alzheimer plena. Se bem‑sucedido, um exame de sangue assim poderia simplificar a triagem, permitir tratamentos mais precoces e ajudar pesquisadores a acompanhar quem se beneficia de novas terapias.
Observando a forma da proteína, não apenas a quantidade
A maioria dos exames de sangue mede quanto de uma determinada molécula está presente. Aqui, os cientistas focaram na forma das proteínas. Dentro de nossas células, um sistema de controle de qualidade mantém as proteínas devidamente dobradas; quando esse sistema falha com a idade, proteínas mal dobradas podem se acumular e danificar células cerebrais. A equipe se perguntou se essa falha na “manutenção das proteínas” deixa uma impressão estrutural nas proteínas do sangue. De 520 voluntários que eram cognitivamente saudáveis, tinham comprometimento cognitivo leve (CCL) ou apresentavam doença de Alzheimer, coletaram sangue e usaram uma técnica química chamada perfilagem covalente de proteínas para marcar partes expostas das proteínas. Quanto mais exposta uma região, mais facilmente ela é marcada, gerando uma leitura numérica da forma da proteína que é em grande parte independente da quantidade total de proteína presente.
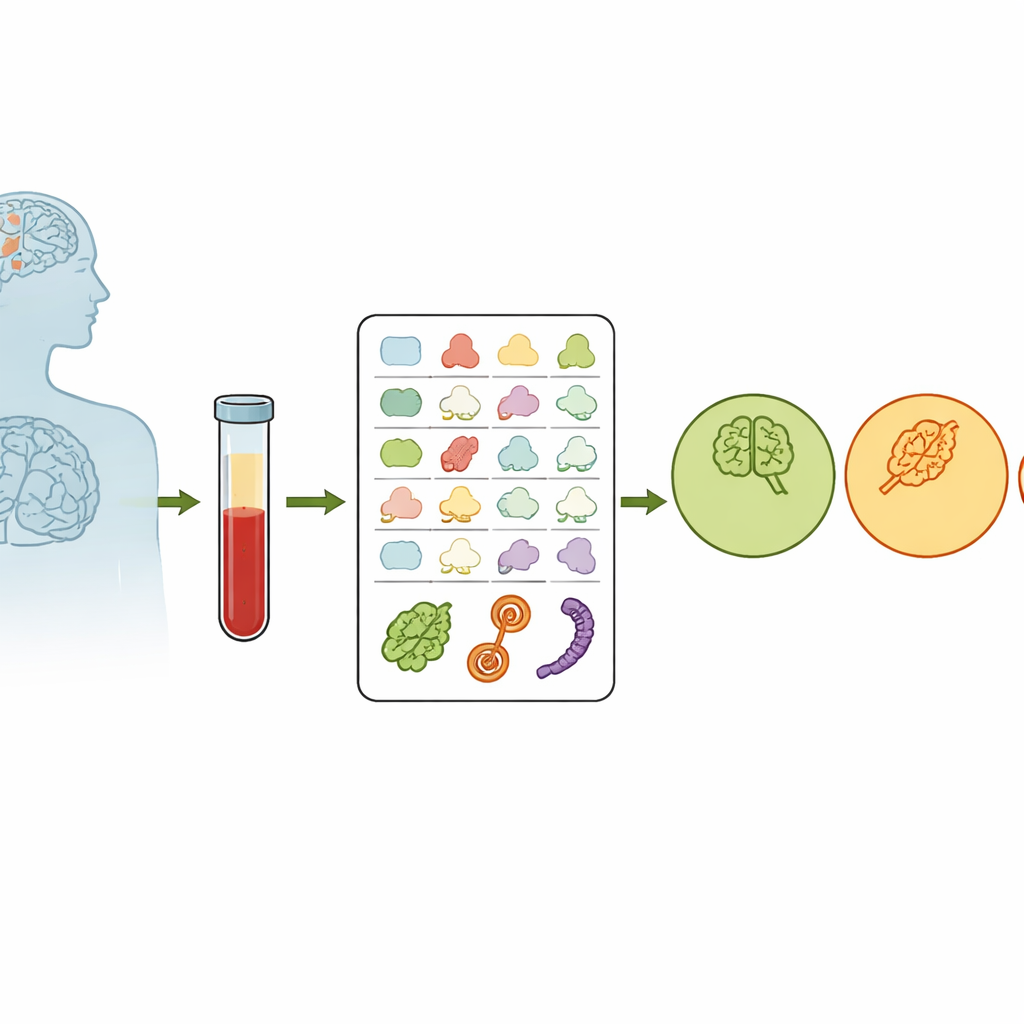
Encontrando impressões estruturais no sangue
Ao analisar quase 900 fragmentos protéicos marcados, os pesquisadores observaram uma tendência sutil, porém consistente: à medida que as pessoas progrediam de saudáveis para CCL e depois para Alzheimer, certas superfícies de proteínas ficaram menos expostas e mais variáveis entre indivíduos. Esse padrão é coerente com a ideia de que o controle do dobramento proteico piora conforme a doença avança. A equipe também examinou como um importante fator de risco genético para Alzheimer, a variante APOE ε4, influenciava a forma das proteínas. Eles constataram que pessoas portadoras de duas cópias de ε4 mostraram mudanças estruturais distintas em várias proteínas que interagem com a APOE, sugerindo que esse gene de risco altera não apenas quais proteínas estão presentes, mas também como elas são dobradas e organizadas.
Conectando proteínas do sangue ao humor e comportamento
O Alzheimer afeta muito mais que a memória; sintomas como agitação, depressão e alucinações são comuns e frequentemente diferem entre homens e mulheres. Os pesquisadores combinaram avaliações clínicas de 12 tipos de sintomas neuropsiquiátricos com suas medidas de forma protéica. Em ambos os sexos, sintomas piores tendiam a acompanhar proteínas ficando mais estruturalmente “fechadas”. Algumas proteínas, incluindo a clusterina e várias outras associadas ao acúmulo de amiloide, acompanharam a severidade dos sintomas de maneira similar em homens e mulheres, enquanto outras mostraram padrões específicos por sexo. Essas descobertas sugerem que a estrutura das proteínas no sangue pode refletir não só a presença da doença, mas também como ela se manifesta no comportamento e no humor.
Painel de três proteínas para classificar o estágio da doença
Para transformar essas medições complexas em algo clinicamente útil, a equipe alimentou os dados estruturais em 18 abordagens diferentes de aprendizado de máquina. O modelo com melhor desempenho, baseado em deep learning, apoiou‑se em apenas três fragmentos protéicos provenientes de C1QA, clusterina (também chamada CLUS) e apolipoproteína B (ApoB). Usando apenas as leituras estruturais desses três fragmentos, o modelo classificou corretamente indivíduos como saudáveis, com CCL ou com Alzheimer em cerca de 83% das vezes em um conjunto de teste independente. Ao responder a perguntas binárias mais simples — por exemplo, distinguir saudável de CCL, ou CCL de Alzheimer — o desempenho do painel foi ainda mais forte, com medidas de acurácia comparáveis ou superiores a muitas abordagens atuais baseadas em sangue que focam nas quantidades de proteínas em vez da estrutura.
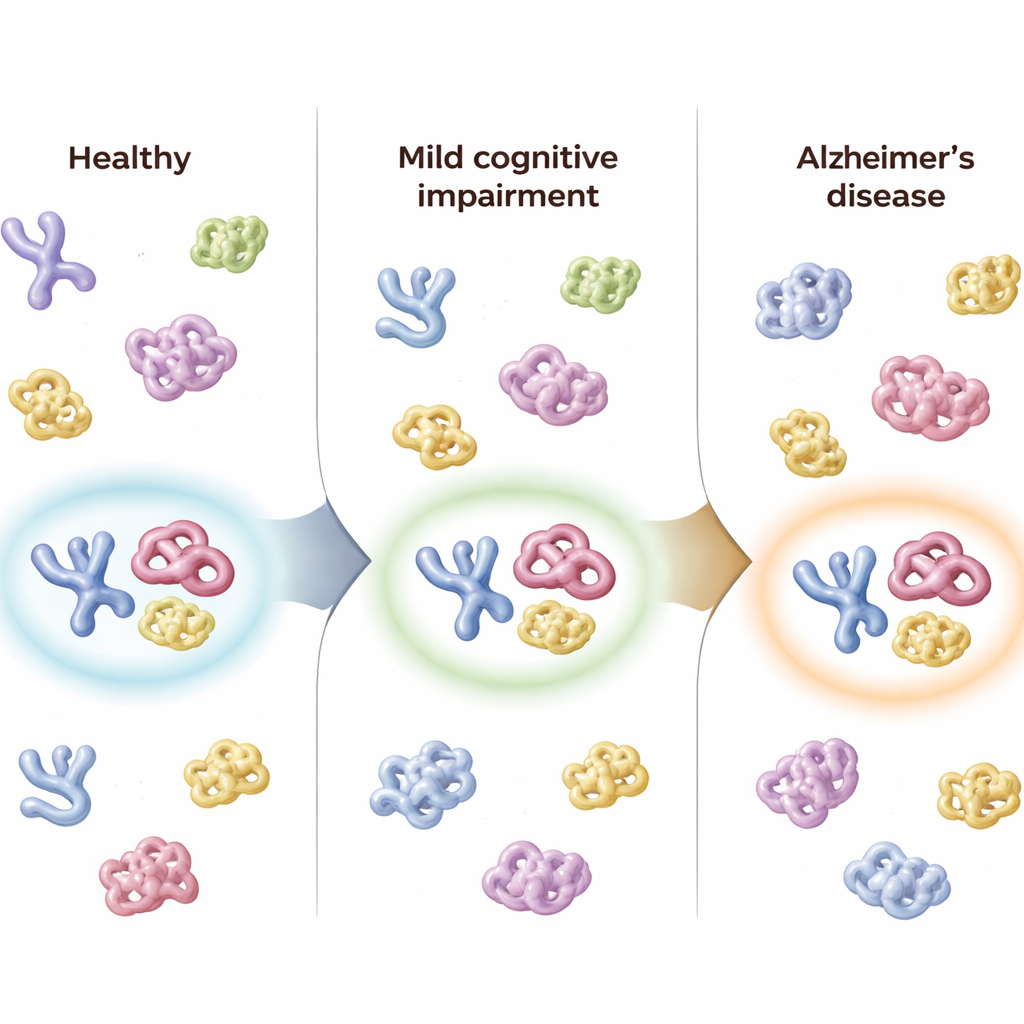
Acompanhando pessoas ao longo do tempo
Os pesquisadores também tiveram amostras de acompanhamento de 50 participantes coletadas até cerca de oito meses depois. Em pessoas cujo diagnóstico piorou — por exemplo, de saudável para CCL, ou de CCL para Alzheimer — a pontuação combinada do painel de três proteínas mudou na mesma direção, refletindo a progressão da doença. Em contraste, indivíduos cujo estado clínico permaneceu o mesmo apresentaram pouca alteração nas pontuações do painel. A pontuação geral de “confiança de Alzheimer” do painel acompanhou de perto testes cognitivos padrão, medidas de funcionamento diário, atrofia cerebral observada em ressonância magnética e marcadores estabelecidos no líquido cefalorraquidiano de amiloide e tau, sugerindo que o sinal estrutural detectado no sangue espelha alterações cerebrais subjacentes.
O que isso pode significar para pacientes
Em conjunto, o trabalho mostra que pequenas mudanças coordenadas nas formas de apenas algumas proteínas abundantes no sangue podem sinalizar de forma confiável se alguém é cognitivamente saudável, está levemente comprometido ou tem doença de Alzheimer. Como o teste usa sangue em vez de líquido cefalorraquidiano ou imagens cerebrais, ele poderia, em princípio, ser escalado para triagem de rotina ou para selecionar e monitorar participantes em ensaios clínicos. Os autores ressaltam que estudos maiores e de maior duração são necessários, e a química envolvida ainda é especializada. Ainda assim, os resultados apontam para a estrutura das proteínas — e não apenas seus níveis — como uma nova fonte promissora de informação para detectar e acompanhar a doença de Alzheimer de forma mais precoce e precisa.
Citação: Son, A., Kim, H., Diedrich, J.K. et al. Structural signature of plasma proteins classifies the status of Alzheimer’s disease. Nat Aging 6, 597–611 (2026). https://doi.org/10.1038/s43587-026-01078-2
Palavras-chave: Biomarcadores da doença de Alzheimer, exame de sangue para demência, alterações no dobramento de proteínas, diagnóstico por aprendizado de máquina, clusterina e C1QA