Clear Sky Science · pt
A resistência ao tratamento com quimioterapia à base de platina em câncer de pulmão e ovário é impulsionada por um secretoma senescente TGFβ alvo‑potencial
Quando o Tratamento do Câncer Volta-se Contra
A quimioterapia à base de platina é uma das principais ferramentas do tratamento moderno do câncer, especialmente para tumores de pulmão e ovário. Seu objetivo é danificar tanto o DNA tumoral que as células cancerosas não conseguem mais se dividir. Ainda assim, muitos pacientes veem seus tumores encolherem inicialmente, apenas para a doença retornar, mais resistente do que antes. Este estudo faz uma pergunta simples, porém inquietante: os próprios fármacos que salvam vidas podem também ajudar as células cancerosas sobreviventes a se recuperarem? A resposta, segundo os autores, reside em um grupo especial de células danificadas, semelhantes a células envelhecidas, e nas poderosas mensagens químicas que elas liberam.
A Dupla Vida das Células Tumorais Envelhecidas
A quimioterapia não trata todas as células tumorais da mesma forma. Algumas são mortas de imediato, mas outras entram em um estado chamado senescência celular — paradas permanentemente de se dividir, mas ainda muito vivas. Essas células senescentes aumentam de tamanho e passam a secretar um coquetel de proteínas e sinais conhecido como fenótipo secretório associado à senescência, ou SASP. Usando células humanas de câncer de pulmão e ovário em laboratório, bem como modelos em camundongos, os pesquisadores mostraram que drogas à base de platina como cisplatina e carboplatina geram células senescentes especialmente potentes. Quando células tumorais frescas foram expostas ao fluido extraído dessas culturas senescentes, cresceram mais rápido, migraram com mais facilidade e formaram aglomerados e esferas maiores e mais agressivos do que as células de controle.
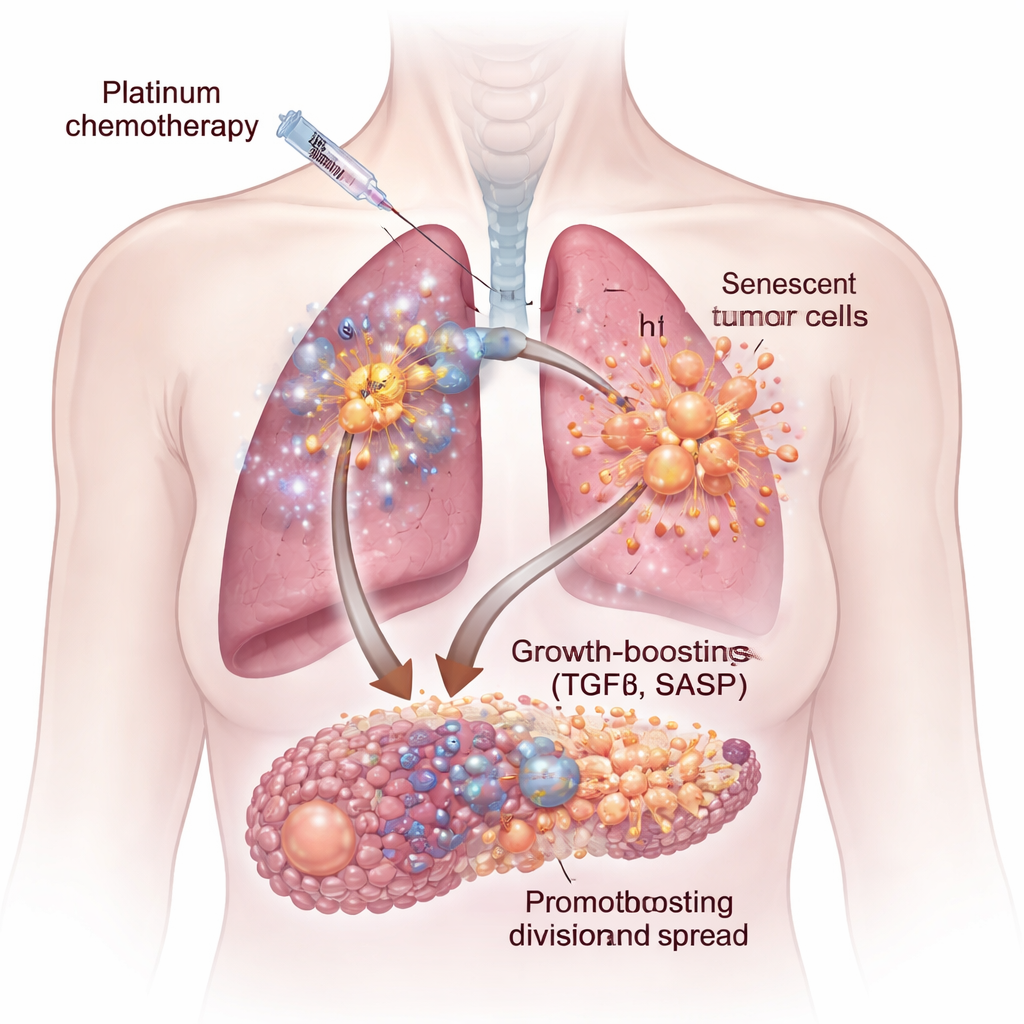
Um Sinal de Crescimento Oculto: TGFβ
Nem todas as quimioterapias desencadearam as mesmas secreções prejudiciais. Ao comparar drogas de platina com outros dois agentes comuns, docetaxel e palbociclib, apenas as células tratadas com platina produziram um SASP que aumentou fortemente o crescimento tumoral. Combinando estudos de expressão gênica, medidas de proteínas e um microarranjo de microambiente de alto rendimento, os autores identificaram um culpado central: a molécula sinalizadora transformador de crescimento beta, ou TGFβ. Células senescentes induzidas por cisplatina estavam enriquecidas em múltiplas formas de TGFβ e vias relacionadas. Adicionar TGFβ purificado a células cancerosas mimetizou o aumento de crescimento observado com o fluido das células senescentes, destacando essa família de citocinas como um motor central do secretoma pró‑tumoral.
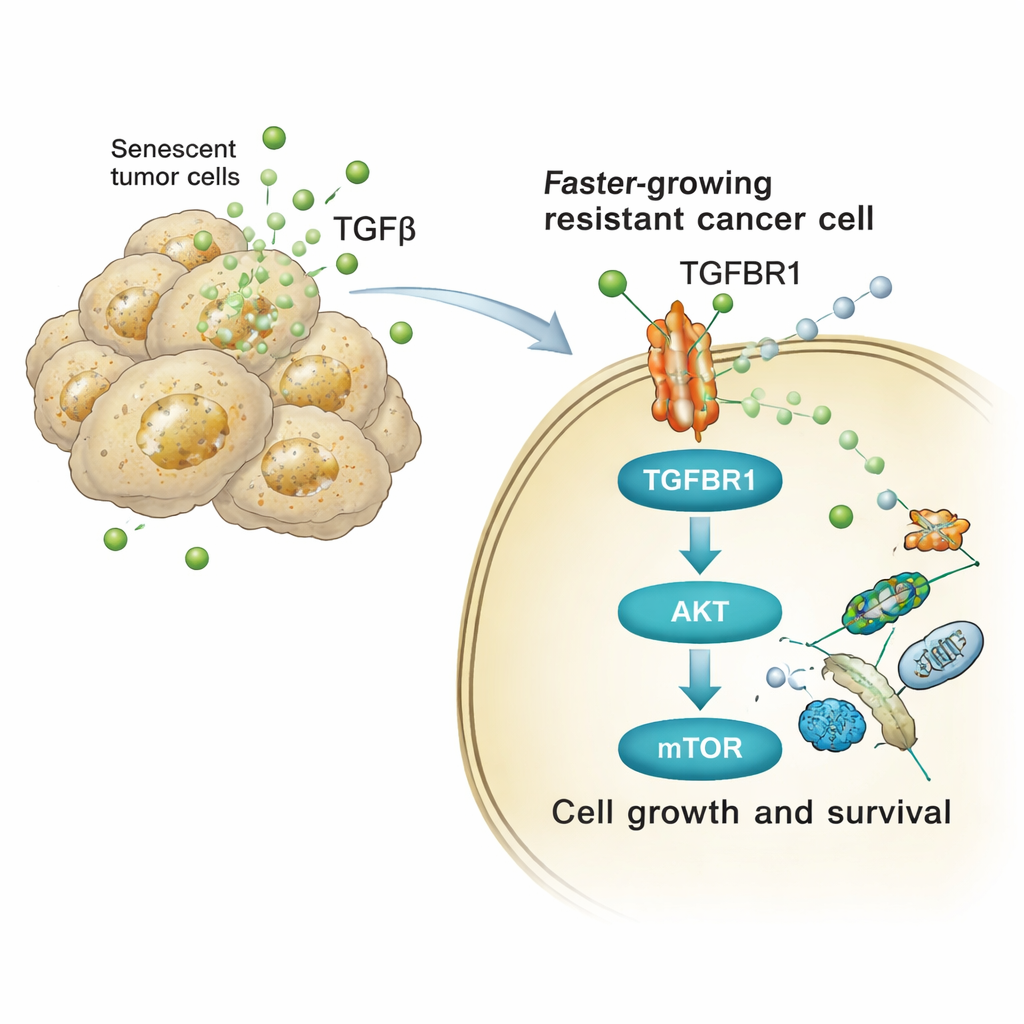
Como o Sinal Reprograma as Células Cancerosas
O estudo depois rastreou como esses sinais ricos em TGFβ mudam o comportamento das células tumorais vizinhas. Na superfície das células receptoras, o TGFβ se liga a um receptor chamado TGFBR1. Isso, por sua vez, ativa uma cadeia interna de proteínas — particularmente as vias AKT e mTOR — conhecidas por controlar crescimento celular, metabolismo e sobrevivência. Tanto em células humanas quanto em células de pulmão de camundongo, a exposição às secreções derivadas da cisplatina aumentou rapidamente as formas ativadas (fosforiladas) de AKT e de sua alvo a jusante p70S6K, e elevou a expressão de genes do ciclo celular. Bloquear TGFBR1 com um fármaco chamado galunisertibe, ou inibir diretamente o mTOR, suprimiu em grande parte esse surto de sinalização e reduziu a proliferação extra, a formação de colônias e o crescimento invasivo de esferas desencadeados pelo secretoma senescente.
Dos Camundongos aos Pacientes: Uma Vulnerabilidade Compartilhada
Esses mecanismos não ficaram confinados a placas de cultura. Em camundongos com tumores de pulmão, a mistura de células senescentes e não senescentes levou a tumores de crescimento mais rápido e a uma sobrevivência menor, enquanto eliminar células senescentes ou bloquear TGFBR1 contornou esse efeito. Quando tratamento padrão com cisplatina foi administrado a camundongos com câncer de pulmão geneticamente induzido, os tumores acumularam marcadores de senescência ao lado de alta atividade AKT/mTOR em células vizinhas ainda em divisão. Combinar cisplatina com inibição de TGFBR1 ou com fármacos senolíticos (que matam seletivamente células senescentes) reduziu a carga tumoral e prolongou a sobrevivência em comparação com a quimioterapia isolada. De modo crucial, análises de amostras humanas de câncer de pulmão e de carcinoma seroso de alto grau do ovário coletadas após terapia baseada em platina revelaram padrões semelhantes: aumento de marcadores de senescência e intensificação da sinalização AKT/mTOR no microambiente tumoral, especialmente em regiões ricas em células senescentes.
Transformando uma Fraqueza em Vantagem
Para o público em geral, a mensagem principal é que a quimioterapia com platina pode deixar para trás uma população de células “zumbi” danificadas mas perigosas. Essas células tumorais senescentes não se dividem mais, mas liberam sinais ricos em TGFβ que despertam as células cancerosas próximas, ajudando os tumores a reganhar terreno e a resistir a tratamentos subsequentes. A notícia encorajadora é que essa vulnerabilidade é tratável. Em modelos pré-clínicos de câncer de pulmão e ovário, adicionar fármacos que bloqueiam o receptor TGFβ TGFBR1 ou que eliminam seletivamente células senescentes tornou a quimioterapia à base de platina mais eficaz e melhorou a sobrevivência sem toxicidade evidente adicional. O trabalho aponta para futuros ensaios clínicos que combinem o tratamento padrão com platina e estratégias senolíticas ou anti‑TGFβ, com o objetivo de preservar os benefícios da quimioterapia enquanto desarmam seus efeitos colaterais ocultos impulsionados pela senescência.
Citação: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
Palavras-chave: resistência à quimioterapia, senescência celular, sinalização TGFβ, câncer de pulmão, câncer de ovário