Clear Sky Science · pt
Danos ao DNA em macrófagos impulsionam autoreatividade imune via apresentação de antígeno nuclear
Quando o desgaste celular vira o sistema imune contra nós
O envelhecimento traz um risco maior de doenças autoimunes, nas quais o sistema imune começa a atacar o próprio corpo que deveria proteger. Este estudo investiga um culpado surpreendente: danos diários ao DNA dentro de células imunes chamadas macrófagos. Ao rastrear como esse dano altera o que os macrófagos mostram a outras células imunes, os pesquisadores identificam um possível elo perdido entre o envelhecimento e o desenvolvimento de doenças como o lúpus.
Guardas do corpo que saem do script
Macrófagos são defensores de linha de frente que engolem micróbios e detritos e depois exibem fragmentos proteicos para células T, ajudando o sistema imune a decidir o que atacar. A equipe gerou camundongos cujos macrófagos eram defeituosos em uma proteína chave de reparo do DNA, ERCC1-XPF, de modo que essas células acumulavam danos persistentes ao DNA. À medida que esses animais envelheceram, desenvolveram características de autoimunidade: focos inflamatórios nos rins, depósitos de complexos imunes e proteínas do complemento, baços aumentados e altos níveis de anticorpos antinucleares semelhantes aos observados em animais naturalmente idosos. Perfis imunes detalhados mostraram expansão de plasmócitos, células T ativadas e células natural killer, todos sinais de um sistema imune cronicamente estimulado.
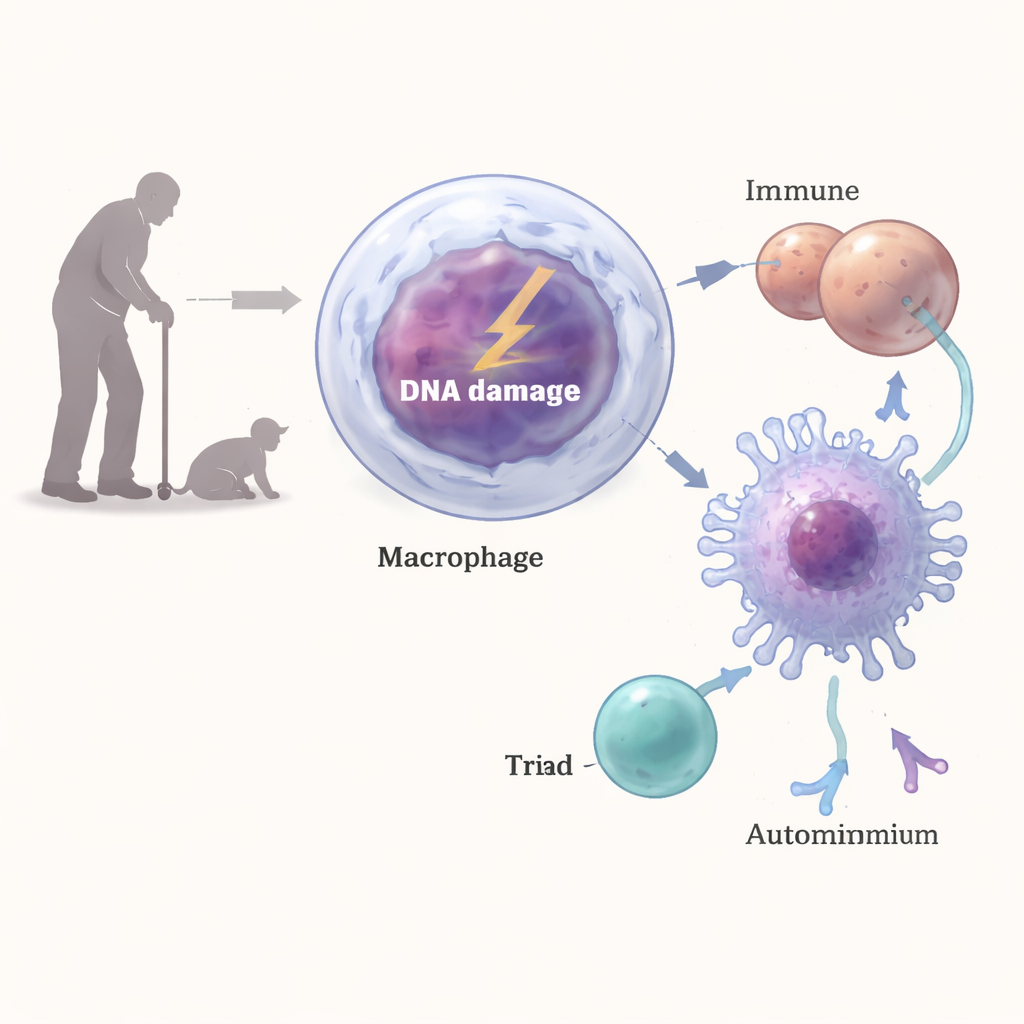
Do DNA quebrado às células T que miram o próprio corpo
Como danos ao DNA em macrófagos poderiam desencadear uma resposta tão forte, semelhante à autoimune? Os pesquisadores descobriram que quebras de DNA ativavam uma via clássica de resposta a danos nessas células, envolvendo enzimas como ATM, ATR e DNA‑PK. Essa sinalização aumentou os níveis de MHC classe II na superfície, as vitrines moleculares usadas para apresentar fragmentos proteicos às células T CD4. Quando macrófagos com dano no DNA foram misturados a células T, eles induziram ativação T mais intensa e produção de interferon‑gama do que macrófagos normais. Bloquear MHC‑II ou interferir na resposta a danos do DNA reverteu grande parte desse efeito, e em animais vivos, anticorpos que bloqueavam MHC‑II ou a depleção de células CD4 reduziram a inflamação renal e os níveis de autoanticorpos.
Proteínas próprias do núcleo colocadas em exibição
Para ver exatamente o que macrófagos danificados estavam mostrando às células T, a equipe isolou os peptídeos ligados ao MHC‑II e os analisou por espectrometria de massa. Em comparação com células normais ou estimuladas por lipopolissacarídeo, macrófagos com dano no DNA apresentaram um cardápio de peptídeos notavelmente diferente. Em vez de majoritariamente proteínas de membrana e extracelulares, suas moléculas de MHC‑II estavam enriquecidas em fragmentos derivados de proteínas nucleares e ribossomais, incluindo histonas e outros componentes intimamente associados ao DNA. Quando alguns desses peptídeos nucleares foram sintetizados e usados para restimular células imunes dos camundongos modificados, eles provocaram fortes respostas de células T, sugerindo que esses fragmentos próprios eram de fato imunogênicos.
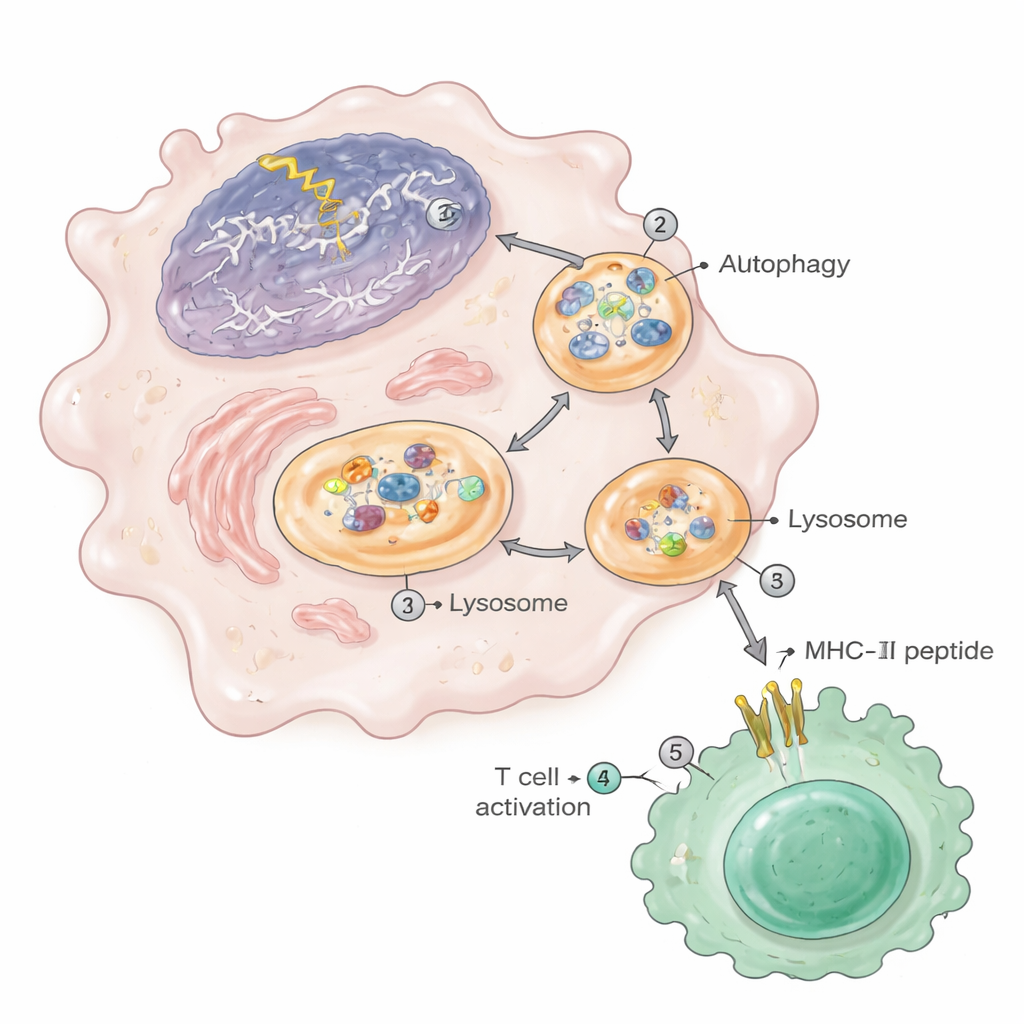
Autofagia: a via de limpeza que alimenta a autoimunidade
A jornada do material nuclear até a vitrine do MHC‑II dependia fortemente da autofagia, o sistema interno de reciclagem da célula. Sob dano ao DNA, a autofagia aumentou e levou fragmentos de cromatina — do próprio núcleo celular — a autossomos que então se fundiam com lisossomos, onde as proteínas são quebradas em peptídeos. Esses lisossomos em macrófagos danificados continham níveis elevados de proteínas nucleares e ribossomais. Quando os pesquisadores bloquearam a autofagia com fármacos ou removeram geneticamente um gene essencial da autofagia (Atg5) nas mesmas células mieloides, os animais apresentaram menos lesões renais, menos células T ativadas e plasmócitos, e uma redução dramática de peptídeos nucleares aparecendo no MHC‑II. Fragmentos de cromatina semelhantes e aumento da apresentação antigênica foram observados em macrófagos de camundongos propensos ao lúpus, em linhagens humanas de monócitos expostas a fármacos danificadores de DNA e em macrófagos de camundongos muito velhos.
Por que isso importa para envelhecimento e doenças autoimunes
Tomados em conjunto, os achados sugerem uma ideia simples, porém poderosa: à medida que envelhecemos, danos ao DNA se acumulam em macrófagos, que por sua vez usam a autofagia para limpar detritos nucleares. Ao fazê‑lo, eles inadvertidamente fragmentam material nuclear em peptídeos que são carregados no MHC‑II e exibidos às células T como se fossem estranhos. Com o tempo, essa exposição crônica a autoantígenos nucleares pode treinar o sistema imune a reagir contra o próprio corpo, promovendo a autoimunidade. Ao identificar essa via — do dano ao DNA à autofagia até a apresentação de antígenos nucleares — o estudo destaca novas estratégias para atenuar a autoimunidade relacionada à idade, como aumentar o reparo do DNA, ajustar a autofagia ou bloquear seletivamente a apresentação de peptídeos nucleares próprios sem desligar as defesas vitais do sistema imune.
Citação: Niotis, G., Arvanitaki, E.S., Theodorakis, E. et al. DNA damage in macrophages drives immune autoreactivity via nuclear antigen presentation. Nat Aging 6, 393–413 (2026). https://doi.org/10.1038/s43587-025-01053-3
Palavras-chave: envelhecimento e autoimunidade, danos ao DNA, macrófagos, autofagia, anticorpos antinucleares