Clear Sky Science · pt
Análises exploratórias dos desfechos clínicos do estudo de fase 1b do BIIB080 em doença de Alzheimer leve
Por que esta pesquisa importa para as famílias
A doença de Alzheimer corrói lentamente a memória, a independência e a identidade, e os medicamentos atuais oferecem apenas alívio modesto. A maioria dos novos tratamentos concentrou-se em limpar um culpado, a proteína amiloide, com impacto limitado sobre o outro marco-chave da doença: emaranhados de uma proteína chamada tau dentro das células cerebrais. Este estudo investigou se um fármaco experimental, BIIB080, que busca reduzir a produção de tau em sua fonte genética, poderia de forma segura desacelerar a perda de memória e o declínio nas atividades diárias em pessoas com Alzheimer inicial.
Uma nova forma de reduzir uma proteína problemática
Em vez de mirar a tau depois que os emaranhados já se formaram, o BIIB080 age um passo antes. É um oligonucleotídeo antisenso, uma curta cadeia de material genético sintético projetada para se ligar à mensagem que as células usam para produzir tau. Ao se prender a essa mensagem, o BIIB080 instrui as células a destruí‑la, reduzindo a quantidade total de tau que o cérebro produz, incluindo formas consideradas especialmente tóxicas. A esperança é que, com menos tau novo sendo fabricado, os emaranhados existentes possam encolher e se espalhar mais lentamente, aliviando os danos aos circuitos cerebrais que sustentam problemas de memória e cognição na doença de Alzheimer.
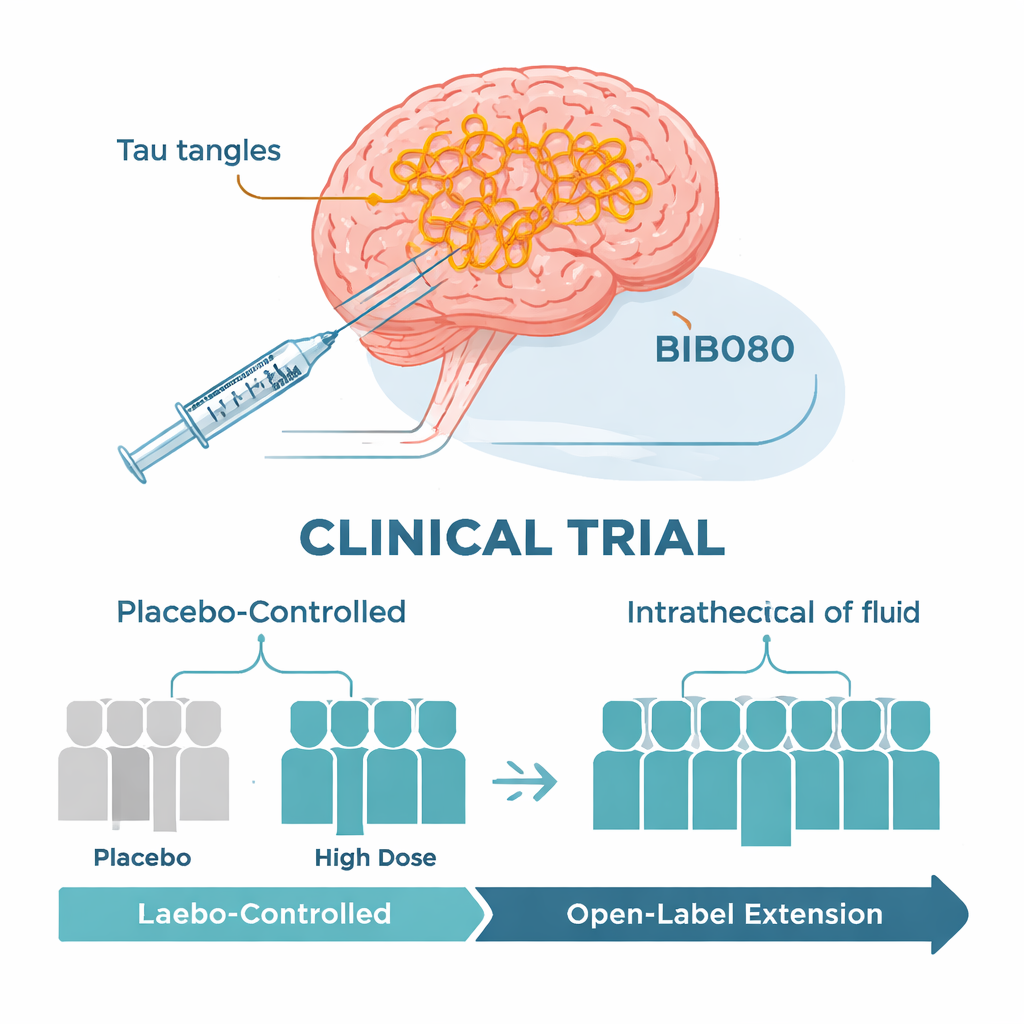
Como o ensaio inicial foi organizado
Os pesquisadores conduziram um ensaio clínico internacional de fase 1b, projetado principalmente para testar a segurança. Pouco mais de 100 pessoas de 50 a 74 anos com Alzheimer leve, confirmado por exames do líquido cefalorraquidiano, foram incluídas. Na primeira parte do estudo, os participantes foram randomizados para receber BIIB080 ou placebo por meio de injeções periódicas no líquido que envolve a medula espinhal durante três meses, e depois acompanhados por vários meses adicionais. Diferentes grupos receberam doses progressivamente mais altas. Em seguida houve uma extensão de longo prazo, na qual todos receberam o que a equipe considerou a dose alta de BIIB080 por quase um ano. Como não havia grupo placebo nessa segunda fase, os cientistas compararam os pacientes tratados com pacientes bem pareados provenientes de outros grandes estudos de Alzheimer.
Sinais de declínio mais lento no pensamento e na vida diária
Embora o estudo fosse pequeno e não projetado para provar eficácia, vários padrões surgiram. Pessoas que receberam as doses mais altas de BIIB080 apresentaram, em média, piora menor em testes padrão de cognição (como o Mini Exame do Estado Mental), memória e capacidade de realizar tarefas cotidianas do que aquelas que receberam placebo nos primeiros meses. Na extensão de longo prazo, 16 participantes que permaneceram em doses altas durante todo o período foram comparados com “controles externos” cuidadosamente pareados de outro ensaio focado em tau e de um grande banco de dados de pesquisa sobre Alzheimer. Em várias medidas — avaliação global da demência, escores cognitivos e questionários funcionais — o grupo BIIB080 tende a declinar mais lentamente do que esses grupos de comparação ao longo de cerca de dois anos desde o início do tratamento.
Mudanças no interior do cérebro que correspondem às tendências clínicas
Relatos anteriores do mesmo ensaio já haviam mostrado que o BIIB080 reduziu fortemente os níveis de tau no líquido cefalorraquidiano e, de forma marcante, diminuiu a quantidade de emaranhados de tau observada em exames cerebrais especializados em muitas regiões. As descobertas clínicas exploratórias deste estudo se alinham com essas mudanças biológicas: onde os emaranhados de tau caíram, a cognição e a função diária pareceram deteriorar‑se mais lentamente. Em modelos animais que produzem tau em excesso, drogas antisenso semelhantes não apenas reduziram os depósitos de tau, mas também diminuíram convulsões, perda de neurônios e problemas comportamentais. Juntos, esses fios de evidência sugerem que reduzir a produção de tau em sua fonte pode realmente modificar o curso do Alzheimer, e não apenas mascarar sintomas.
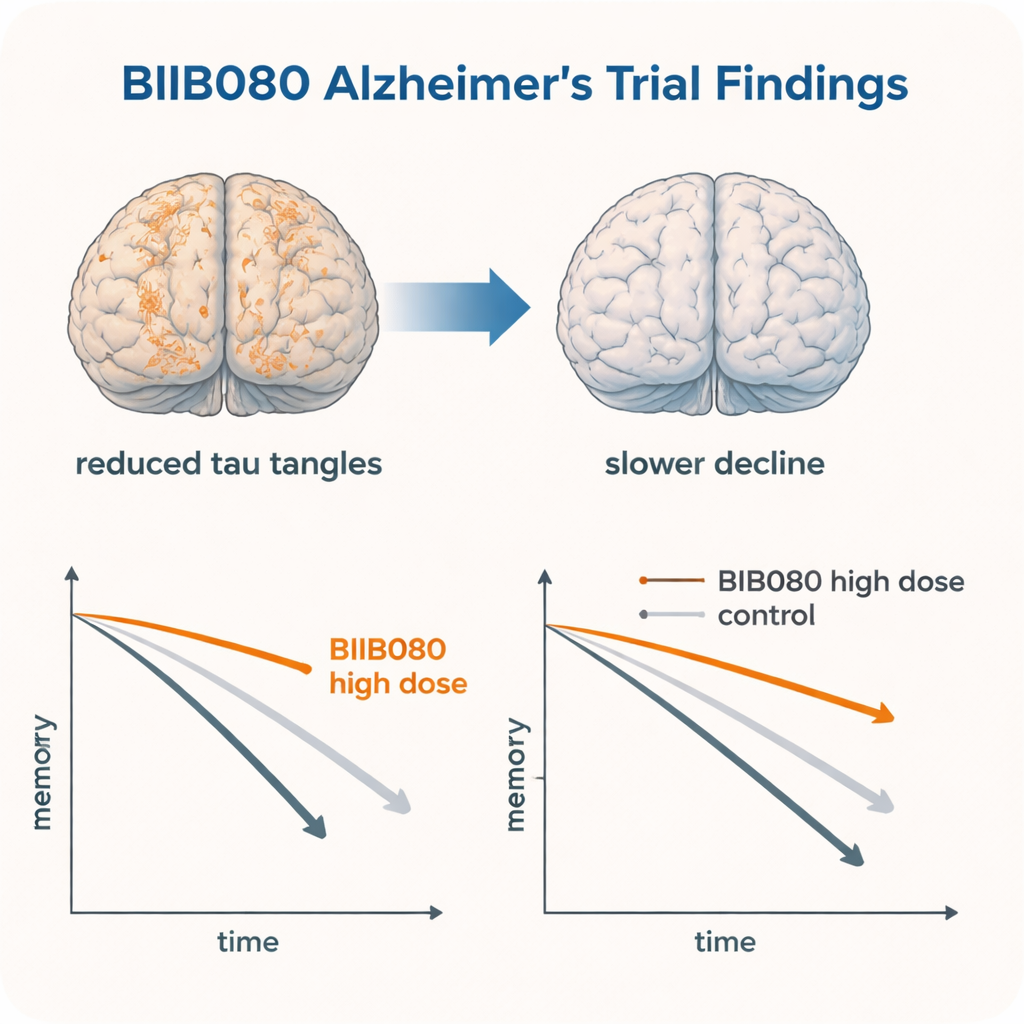
Segurança, ressalvas e próximos passos
A maioria dos efeitos adversos do BIIB080 neste ensaio foi leve a moderada e relacionada às próprias injeções espinhais, como dor de cabeça, dor nas costas ou tontura temporária. Alguns participantes desenvolveram problemas mais sérios, incluindo piora dos sintomas de demência, e interromperam o tratamento, portanto monitoramento cuidadoso continua essencial. É importante ressaltar que o estudo foi pequeno, utilizou vários grupos de dose com características iniciais desiguais e baseou‑se em comparação com dados externos depois que todos estavam na droga ativa. Os autores, por isso, enfatizam que as tendências encorajadoras ainda podem ser devidas ao acaso ou a vieses sutis.
O que isso pode significar para tratamentos futuros
Para pessoas que enfrentam a doença de Alzheimer, essas descobertas ainda não oferecem uma nova terapia aprovada, mas apontam para um caminho promissor. O BIIB080 parece reduzir de forma segura os emaranhados de tau no cérebro humano e está associado a declínio clínico mais lento neste estudo inicial, especialmente em doses mais altas. Como o ensaio foi exploratório, estudos maiores e mais rigorosos são necessários para confirmar se a droga realmente retarda a perda de memória e preserva a independência. Testes desse tipo já estão em andamento em um ensaio de fase 2 chamado CELIA, que acompanhará mais pacientes por mais tempo. Se os resultados futuros se confirmarem, terapias que diminuem a produção de tau poderão se juntar ou complementar os medicamentos que atacam a amiloide, oferecendo uma abordagem mais abrangente para alterar o curso do Alzheimer.
Citação: Shulman, M., Wu, S., Ziogas, N. et al. Exploratory analyses of clinical outcomes from the BIIB080 phase 1b study in mild Alzheimer’s disease. Nat Aging 6, 445–453 (2026). https://doi.org/10.1038/s43587-025-01031-9
Palavras-chave: Doença de Alzheimer, proteína tau, terapia antisenso, ensaio clínico, neurodegeneração