Clear Sky Science · pt
Senotoxinas miram a senescência via especificidade de ligação a lipídios, desequilíbrio iônico e remodelagem do lipidoma
Por que matar células “zumbis” pode afiar o tratamento do câncer
À medida que envelhecemos — ou somos submetidos a tratamentos agressivos como a quimioterapia — algumas células param de se dividir, mas se recusam a morrer. Essas células “zumbis”, conhecidas como células senescentes, podem liberar moléculas inflamatórias que danificam os tecidos e podem ajudar os tumores a retornar. Este estudo explora uma maneira surpreendente de eliminar seletivamente essas células problemáticas usando uma proteína derivada de veneno, potencialmente tornando os tratamentos contra o câncer mais eficazes e mais seguros.
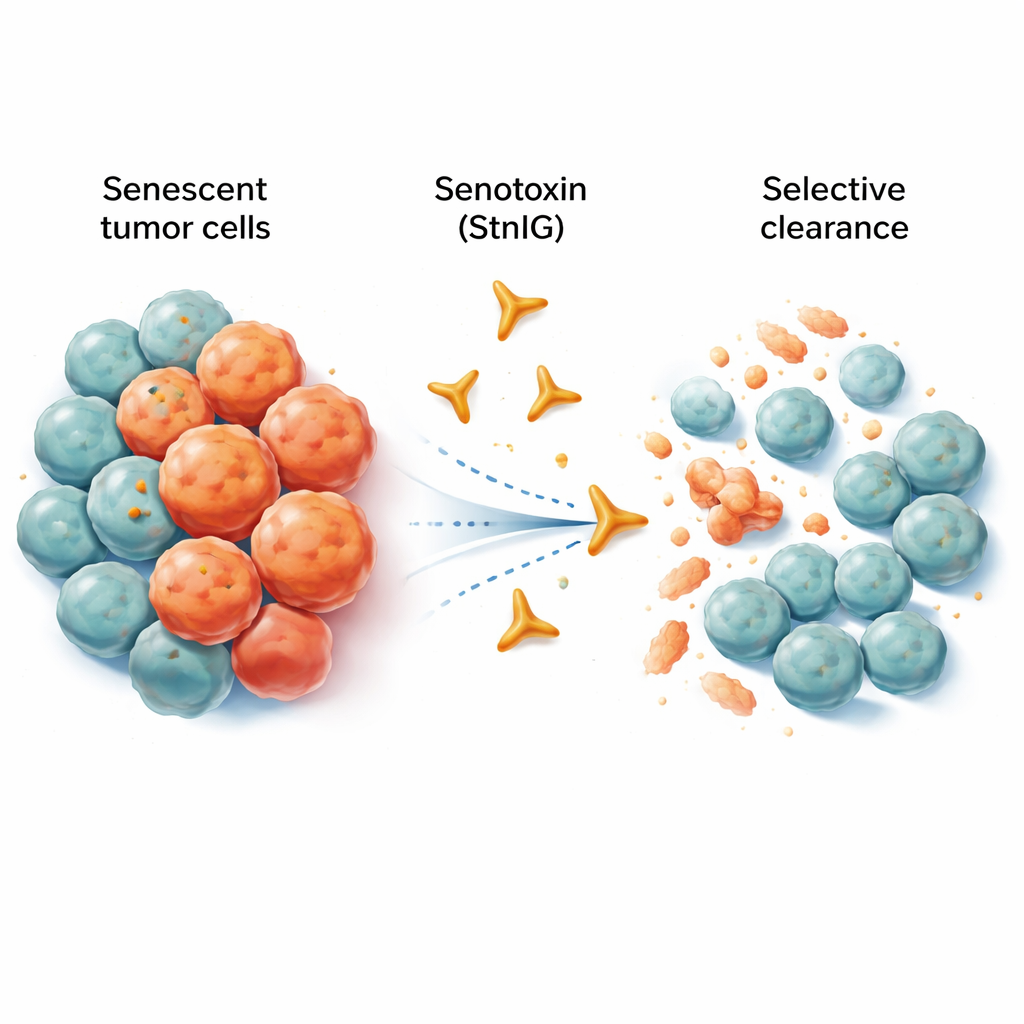
Células velhas que não desistem
As células senescentes são como trabalhadores aposentados que continuam ocupando suas mesas e atrapalhando o escritório. Elas não se multiplicam mais, mas liberam um coquetel de sinais inflamatórios que pode enfraquecer os tecidos vizinhos, promover o envelhecimento e até apoiar o crescimento e a disseminação de tumores. A quimioterapia, embora mate muitas células cancerosas, frequentemente deixa um rastro de células senescentes dentro e ao redor do tumor. Essas células remanescentes podem alimentar inflamação crônica, efeitos colaterais e, eventualmente, recaída. Medicamentos experimentais existentes chamados senolíticos visam remover células senescentes, mas muitos deles atingem também células saudáveis, funcionam apenas em faixas de dose muito estreitas ou são de difícil absorção pelo organismo.
Transformando veneno de anêmona-do-mar em uma ferramenta de precisão
Os pesquisadores voltaram-se para os especialistas naturais em matar células: os venenos animais. Eles se concentraram em uma proteína formadora de poros chamada sticholysin I (StnI), encontrada em uma anêmona-do-mar caribenha. Essa proteína pode perfurar pequenas aberturas nas membranas celulares. A equipe descobriu que a StnI, e uma versão refinada que eles engenheiraram chamada StnIG, são notavelmente melhores em matar células cancerosas senescentes do que suas vizinhas não senescentes. Em vários tipos de células humanas de câncer (melanoma, fígado, pulmão e tumores de origem nervosa) induzidas à senescência por drogas quimioterápicas, StnI e especialmente StnIG eliminaram as células envelhecidas em doses muito menores do que as necessárias para afetar células em crescimento ativo. StnIG mostrou-se mais seletiva do que um senolítico experimental líder, o navitoclax, sugerindo que toxinas cuidadosamente ajustadas podem superar as abordagens atuais.
Como membranas celulares alteradas se tornam um calcanhar de Aquiles
As células senescentes não mudam apenas internamente; sua membrana externa — a camada lipídica que envolve cada célula — também é remodelada. Em células saudáveis, certos lipídios ficam majoritariamente no lado interno da membrana, escondidos do mundo exterior. Em células senescentes, esse equilíbrio se rompe e esses lipídios se tornam expostos. Usando análise química detalhada e simulações computacionais, a equipe mostrou que StnIG reconhece e se liga a esse panorama lipídico alterado. Sua estrutura é especialmente eficaz em se acomodar a lipídios específicos que as células senescentes expõem na superfície. Uma vez ligada, StnIG forma poros que permitem que átomos carregados, ou íons, fluam para dentro e para fora de maneira altamente desequilibrada.
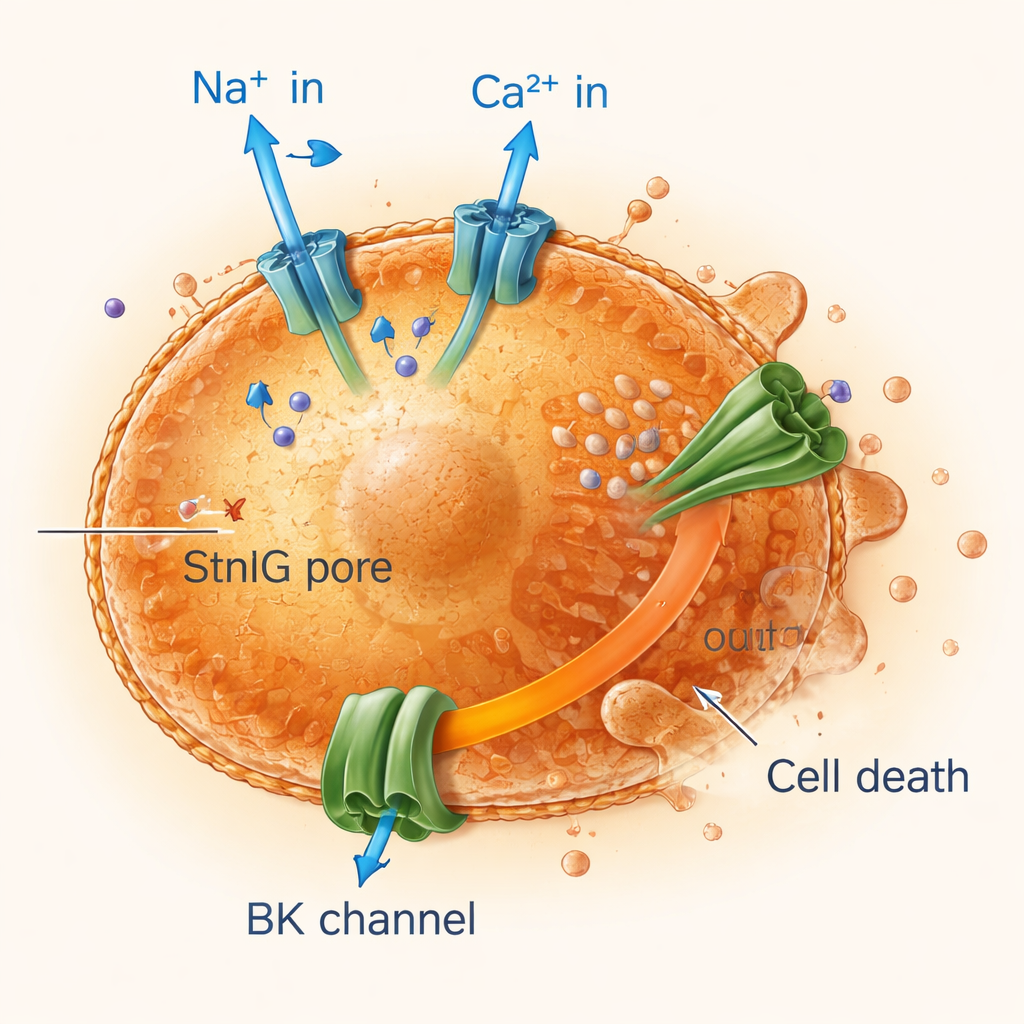
Curto-circuitando células envelhecidas com desequilíbrio iônico
Ao monitorar eletricidade e movimento iônico através das membranas celulares, os pesquisadores descobriram que os poros formados por StnIG permitem que íons de sódio e cálcio entrem às pressas nas células senescentes enquanto o potássio vaza continuamente para fora. O aumento de cálcio ativa grandes canais de potássio, amplificando a perda de potássio, que é crucial para manter o volume e a sobrevivência celular. Células senescentes, já menos flexíveis e mais frágeis do que as saudáveis, não conseguem lidar com essa perturbação iônica sustentada. Suas mitocôndrias — as usinas de energia da célula — perdem sua carga elétrica, a produção de energia despenca e as células passam por formas programadas de morte, incluindo apoptose e uma morte inflamatória explosiva chamada piroptose. Bloquear a entrada de cálcio ou os canais de potássio protegeu as células senescentes, confirmando que esse distúrbio iônico é central para a ação da toxina.
Do cultivo celular a animais vivos
A equipe então testou se essa estratégia funciona em organismos vivos. Em embriões de zebrafish carregando células humanas de melanoma senescentes, baixas doses de StnIG reduziram o número dessas células tão efetivamente quanto o navitoclax, sem toxicidade óbvia. Em modelos de camundongos com melanoma e câncer de fígado, a quimioterapia com um fármaco que bloqueia o ciclo celular (palbociclib) retardou o crescimento do tumor ao conduzir muitas células cancerosas à senescência. Quando os pesquisadores adicionaram StnIG de forma intermitente, os tumores encolheram ou entraram em remissão mais eficazmente do que apenas com quimioterapia, e de maneira comparável à combinação quimioterapia–navitoclax. Importante, os camundongos tratados com StnIG mostraram efeitos colaterais limitados e sem danos evidentes em órgãos principais, embora o potássio sanguíneo tenha aumentado em animais com tumores senescentes — provavelmente refletindo a liberação massiva de potássio à medida que as células tumorais eram destruídas.
O que isso significa para o futuro do cuidado contra o câncer
Este trabalho introduz “senotoxinas”: proteínas inspiradas em venenos e engenheiradas que exploram as peculiaridades únicas da membrana e do manejo iônico das células senescentes. Ao localizar lipídios alterados e forçar desequilíbrios iônicos fatais, StnIG pode limpar seletivamente células senescentes prejudiciais enquanto poupa a maior parte do tecido saudável. Usadas em conjunto com a quimioterapia, tais senotoxinas podem um dia ajudar a varrer as células zumbis que alimentam recaídas e inflamação crônica, tornando os tratamentos contra o câncer mais duradouros e potencialmente aliviando alguns efeitos colaterais a longo prazo.
Citação: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
Palavras-chave: senescência celular, senolíticos, terapia contra o câncer, fármacos derivados de veneno, canais iônicos