Clear Sky Science · pt
Edição de base em PIK3CD adaptada a CAR aumenta a potência antitumoral de células T
Reprogramando células de combate ao câncer
A terapia com células T com receptor quimérico de antígeno (CAR) transformou o tratamento de alguns cânceres sanguíneos, mas muitos pacientes ainda recaem ou nunca respondem. Um problema central é que essas células imunes modificadas podem se exaurir ou não persistir no organismo por tempo suficiente. Este estudo faz uma pergunta simples, porém poderosa: em vez de redesenhar completamente os CARs, e se pudéssemos “reajustar” sutilmente a fiação interna das células T para que permaneçam potentes por mais tempo, e o façam de maneira segura?
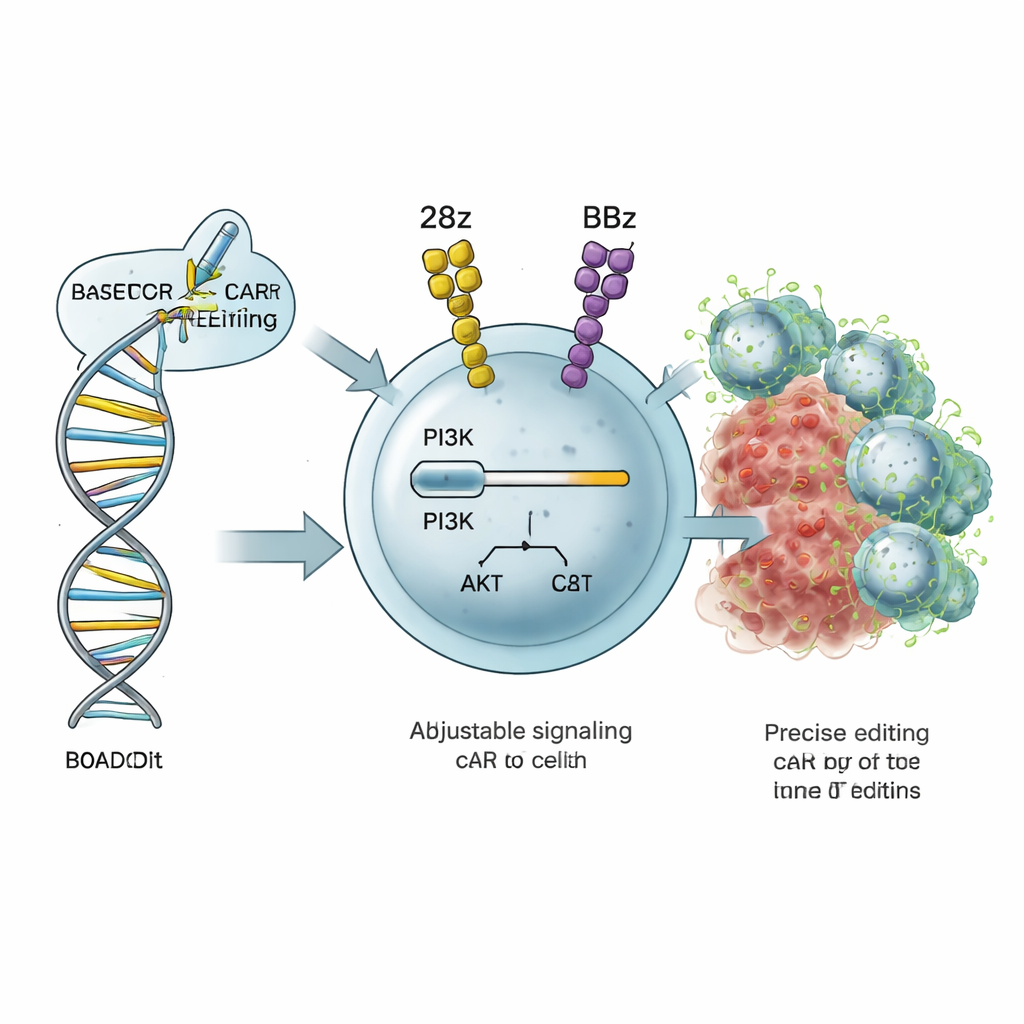
Apontando o botão de volume da célula T
As células T que matam o câncer dependem de circuitos de sinalização internos que lhes dizem quão fortemente ativar, quão rapidamente se dividir e se tornar combatentes de curta duração ou células de memória de longa duração. Um circuito principal é a via PI3K–AKT, na qual uma proteína chamada PI3Kδ—codificada pelo gene PIK3CD—age como um botão de volume para ativação e metabolismo. Os autores desenvolveram uma estratégia que chamam ROADSTAR, que usa edição de base, uma forma altamente precisa de engenharia genômica por CRISPR, para alterar letras individuais em PIK3CD. Em vez de ligar ou desligar totalmente a via, o ROADSTAR busca pequenas mutações que aumentem ou diminuam a sinalização de modo sutil, combinando melhor com o desenho específico do CAR dentro da célula T.
Descobrindo mutações úteis
A equipe construiu uma biblioteca de 34 alterações de uma única letra na região regulatória de PIK3CD e as introduziu em células T humanas que já carregavam um de dois desenhos comuns de CAR: 28z (baseado na molécula CD28) e BBz (baseado em 4‑1BB). Esses CARs diferem em como estimulam as células T: 28z tende a induzir um ataque forte e rápido, porém também exaustão, enquanto BBz promove melhor sobrevivência e formação de memória, mas pode ser menos agressivo. As CAR T editadas foram submetidas a um “teste de estresse” ao serem expostas repetidamente a células de leucemia. Usando sequenciamento profundo, os pesquisadores acompanharam quais mutações permitiam que as CAR T superassem suas pares não editadas ao longo de várias semanas.
Duas mutações destacaram‑se claramente. Em CAR T BBz, uma alteração chamada E81K aumentou levemente a atividade da PI3Kδ, elevando os sinais pela via PI3K–AKT. Em CAR T 28z, uma alteração diferente, L32P, reduziu a atividade da PI3Kδ. Modelagem estrutural sugeriu que ambas as edições alteram sutilmente como a PI3Kδ interage com seu parceiro regulatório, afinando a intensidade da sinalização em vez de ligá‑la ou desligá‑la completamente. Importante, a mutação benéfica para um desenho de CAR não foi a mesma para o outro, ressaltando que cada arquitetura de CAR exige seu próprio ajuste interno ideal.
Células CAR T mais fortes, mais aptas e de ação mais duradoura
Quando as edições promissoras foram testadas individualmente, E81K tornou as CAR T BBz mais ativadas ao reconhecer células tumorais, melhores na proliferação e marcadamente mais eficientes em matar alvos cancerígenos, incluindo aqueles com baixos níveis de antígeno. Essas células desenvolveram‑se em células T de memória efectora que combinaram forte capacidade citotóxica com habilidade de persistir. Em modelos murinos de leucemia e neuroblastoma metastático, as CAR T BBz editadas com E81K controlaram os tumores de forma mais completa e por muito mais tempo do que as células BBz não editadas, chegando a derrotar múltiplas rodadas de nova exposição tumoral. Perfilagem detalhada por RNA de célula única e metabólica mostrou que as células E81K tinham função mitocondrial aprimorada, maior capacidade respiratória e glicolítica de reserva e menos sinais de exaustão—essencialmente, eram mais energéticas e resilientes.
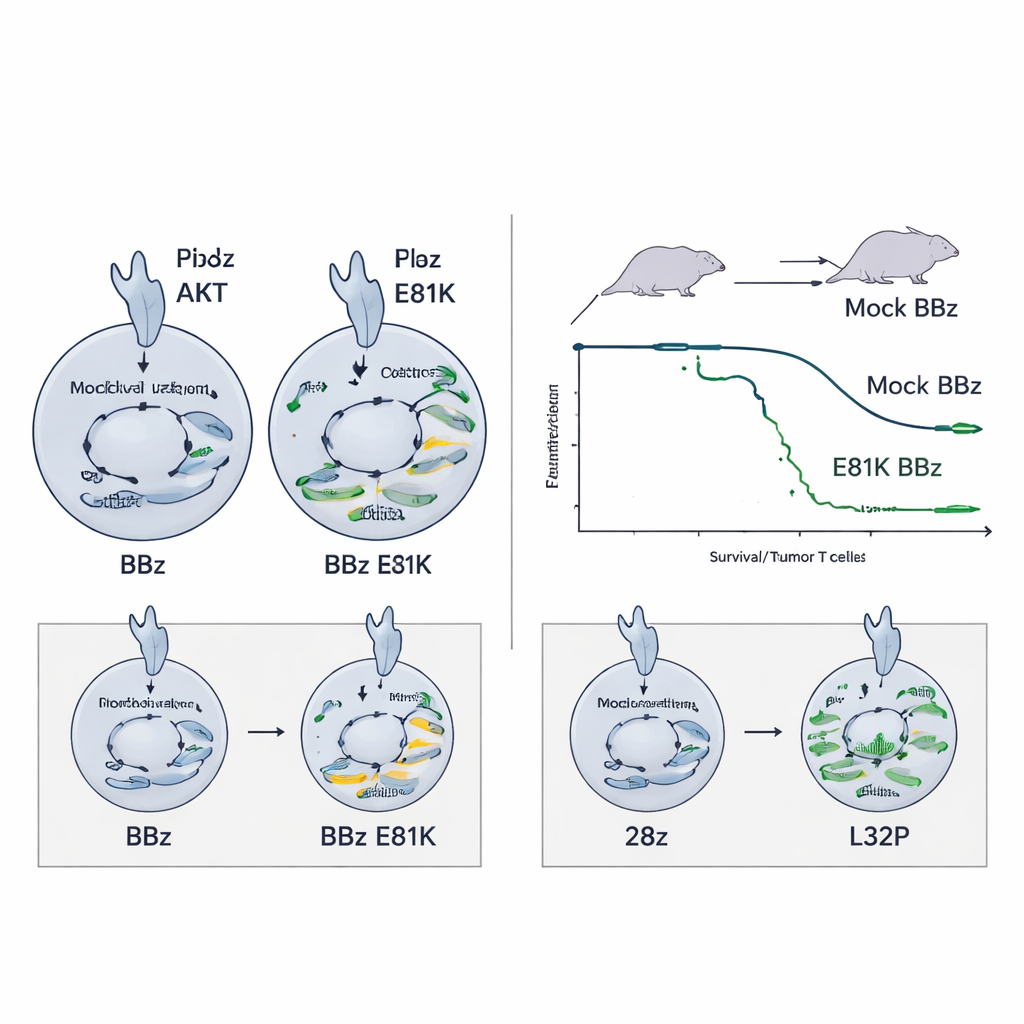
Prevenindo esgotamento em CARs altamente ativos
O mesmo impulso dado por E81K não ajudou—e poderia até prejudicar—as CAR T 28z, que já sinalizam intensamente. Nesse contexto, atividade adicional da PI3K aumentou marcadores de exaustão sem melhorar a função. Aqui, a mutação L32P mostrou‑se melhor ajustada: ao reduzir modestamente a sinalização PI3K–AKT, as CAR T 28z editadas com L32P exibiram menor ativação basal, mas mantiveram alta capacidade de matar e proliferaram mais ao longo do tempo. Elas também preservaram um estado menos diferenciado, com características de memória, incluindo um pool de memória similar a células‑tronco que se acredita sustentar respostas de longo prazo. Em um modelo desafiador de neuroblastoma, as CAR T 28z modificadas com L32P melhoraram a sobrevida em comparação com suas contrapartes não editadas.
Segurança e promessa futura
Uma preocupação central ao alterar permanentemente a sinalização imune é o risco de crescimento descontrolado ou de cânceres secundários. Os autores, portanto, realizaram verificações de segurança extensas. As CAR T BBz editadas com E81K não cresceram de forma anormal em cultura, não causaram dano a órgãos ou crises inflamatórias em camundongos e não mostraram sinais de linfoma ou invasão tecidual meses após a infusão. Bancos de dados clínicos também não mostram enriquecimento dessas mutações específicas em PIK3CD em leucemias de células T. No geral, o trabalho demonstra que alterações genômicas de uma única letra, escolhidas com cuidado, podem atuar como controles de precisão para o comportamento das células T—ampliando o poder antitumoral e a persistência ao mesmo tempo em que respeitam a biologia única de cada CAR. Essa abordagem ROADSTAR pode ajudar a criar a próxima geração de terapias CAR T que sejam mais eficazes e mais confiáveis contra cânceres sanguíneos e, potencialmente, tumores sólidos.
Citação: Bucher, P., Brückner, N., Kortendieck, J. et al. CAR-adapted PIK3CD base editing enhances T cell anti-tumor potency. Nat Cancer 7, 368–383 (2026). https://doi.org/10.1038/s43018-025-01099-7
Palavras-chave: células CAR T, sinalização PI3K, edição de base, imunoterapia contra o câncer, metabolismo de células T