Clear Sky Science · pt
Ácidos graxos promovem respiração desacoplada via transportadores ATP/ADP em adipócitos brancos
Por que as células de gordura podem ajudar a queimar energia
A maioria das pessoas pensa na gordura corporal como um depósito silencioso de calorias. Este estudo revela um lado surpreendentemente ativo das células de gordura branca: nas condições adequadas, elas podem desperdiçar combustível e gerar calor. Ao revelar uma nova forma pela qual as células de gordura permitem que a energia “vaze”, o trabalho aponta para estratégias inéditas para ajudar o corpo a queimar mais calorias e, potencialmente, combater a obesidade.
Quando a gordura armazenada volta a ser combustível
Na vida cotidiana, as células de gordura branca passam grande parte do tempo armazenando energia como triglicerídeos — grandes gotículas de gordura. Durante exercício, jejum ou exposição ao frio, sinais de estresse estimulam essas células a quebrar os triglicerídeos num processo chamado lipólise, liberando ácidos graxos e glicerol. Os pesquisadores confirmaram que, quando essa quebra é estimulada em adipócitos brancos cultivados em laboratório, as células aumentam acentuadamente o uso de oxigênio, um sinal de que suas usinas internas, as mitocôndrias, estão trabalhando mais. Bloquear a primeira etapa da lipólise interrompeu tanto a liberação de ácidos graxos quanto o aumento do consumo de oxigênio, mostrando que o processo depende dos próprios ácidos graxos.
Ácidos graxos livres como interruptores da queima de energia
Os ácidos graxos que saem da célula de gordura não deixam todo o tecido; alguns permanecem internamente. A equipe demonstrou que esses ácidos graxos livres remanescentes são fundamentais para aumentar a atividade mitocondrial. Quando uma proteína no meio de cultura foi usada para sequestrar os ácidos graxos, as células liberaram mais gordura ao todo, mas seu consumo de oxigênio caiu, indicando que altos níveis internos de ácidos graxos — não apenas a lipólise em si — impulsionam a respiração extra. Inversamente, bloquear a reesterificação de triglicerídeos, uma via que normalmente reempacota os ácidos graxos, elevou o consumo de oxigênio e reduziu ainda mais a diferença de potencial elétrico através da membrana mitocondrial. Em conjunto, esses achados sugerem que os ácidos graxos livres empurram as mitocôndrias para um modo “vazante”, desperdiçando energia.
Um novo agente na respiração geradora de calor
No tecido adiposo marrom termogênico clássico, uma proteína chamada UCP1 perfura a barreira mitocondrial para que a energia dos alimentos seja liberada como calor em vez de ser armazenada como combustível celular útil. As células de gordura branca têm pouco ou nenhum UCP1, então os autores buscaram outra via. Eles se concentraram no transportador ATP/ADP, uma proteína que normalmente troca a moeda energética da célula através da barreira mitocondrial. Usando tanto um bloqueador químico específico quanto ferramentas genéticas para reduzir esse transportador, mostraram que ele é necessário para o vazamento induzido por ácidos graxos: bloquear o transportador preservou a carga mitocondrial e impediu o aumento do consumo de oxigênio durante a lipólise, mesmo que a lipólise em si prosseguisse normalmente. Isso indica que os ácidos graxos livres atuam junto com o transportador para criar um vazamento controlado de prótons através da barreira mitocondrial, ativando a respiração desacoplada.
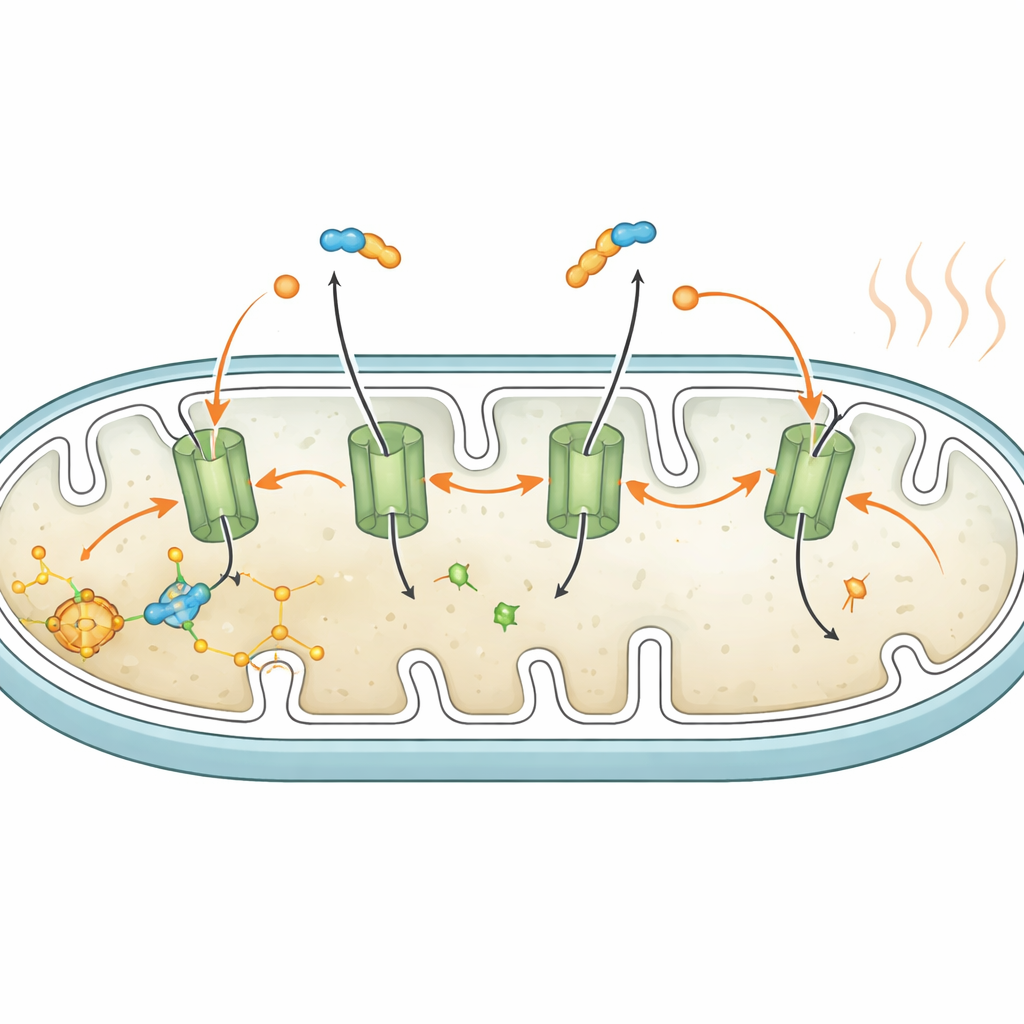
Da cultura celular a animais vivos
Para testar se esse vazamento de energia importa em animais inteiros, os pesquisadores usaram camundongos nos quais uma proteína de sinalização chamada STAT3 foi removida especificamente das células de gordura. Esses animais realizam a lipólise normalmente, mas apresentam respiração dirigida por ácidos graxos reduzida em sua gordura branca. Em condições laboratoriais habituais, nas quais o tecido marrom está ativo e responde pela maior parte da defesa contra o frio, esses camundongos permaneceram aquecidos como seus irmãos normais. No entanto, quando os animais foram tornados obesos e mantidos a uma temperatura em que o tecido marrom está largamente inativo, os animais sem STAT3 em sua gordura ficaram sensíveis ao frio e mostraram uma resposta menor no aumento global do consumo de oxigênio durante a exposição ao frio ou quando a lipólise foi induzida por drogas. Importante: mudanças semelhantes não foram observadas quando o STAT3 foi deletado apenas no tecido marrom, apontando para um papel específico da gordura branca.
Gordura branca como um aquecedor oculto
O estudo conclui que, nas células de gordura branca, os ácidos graxos livres gerados durante a lipólise ativa podem se ligar ao transportador ATP/ADP nas mitocôndrias e desencadear um vazamento energético que produz calor em vez de combustível celular útil. Em animais obesos mantidos aquecidos, essa respiração desacoplada na gordura branca contribui de forma significativa para manter a temperatura corporal e o gasto energético total, especialmente quando o tecido marrom e os tremores musculares são limitados. Como a gordura branca é abundante em adultos, particularmente na obesidade, aumentar suavemente esse vazamento poderia oferecer uma nova forma de elevar a queima diária de calorias e apoiar terapias de perda de peso, desde que isso possa ser feito com segurança e sem prejudicar outros tecidos.
Citação: Ahmadian, M., Aksu, A.M., Dhillon, P. et al. Fatty acids promote uncoupled respiration via ATP/ADP carriers in white adipocytes. Nat Metab 8, 572–586 (2026). https://doi.org/10.1038/s42255-026-01467-2
Palavras-chave: tecido adiposo branco, ácidos graxos, desacoplamento mitocondrial, termogênese, obesidade