Clear Sky Science · pt
PFKM governa mudanças metabólicas durante toda a diferenciação do músculo esquelético
Por que as células musculares precisam usar o açúcar com inteligência
Quando nos exercitamos ou simplesmente nos levantamos de uma cadeira, nossos músculos esqueléticos entram em ação, queimando açúcar para alimentar cada contração. Mas células‑tronco musculares jovens e fibras musculares totalmente formadas não processam a glicose da mesma forma. Este estudo revela um sistema de comutação embutido — centrado em uma única enzima chamada PFKM — que decide se a glicose será queimada para energia imediata ou redirecionada para proteger e reconstruir as células. Entender esse interruptor pode abrir novos caminhos para tratar fraqueza muscular, músculos envelhecidos e doenças metabólicas hereditárias.
Um semáforo para o combustível celular
A glicose que entra na célula pode seguir várias rotas. Uma via principal, a glicólise, converte rapidamente o açúcar em energia e blocos de construção para fibras musculares em crescimento. Outra rota, a via das pentoses fosfato, produz moléculas que defendem as células contra o estresse oxidativo e dão suporte à síntese de DNA e lipídios. Os pesquisadores focaram na PFKM, uma versão da enzima fosfofrutoquinase‑1 que fica num ponto de decisão chave na glicólise. Ao medir centenas de metabólitos ao longo de minutos a horas após ativar um sinal de crescimento chamado Wnt, eles descobriram que as células acumulavam rapidamente intermediários iniciais da glicólise enquanto o produto da PFKM caía e os metabólitos da via das pentoses fosfato aumentavam. Isso sugeriu que as células estavam ativamente reduzindo a atividade da PFKM para desviar a glicose para uma química protetora em vez de pura produção de energia. 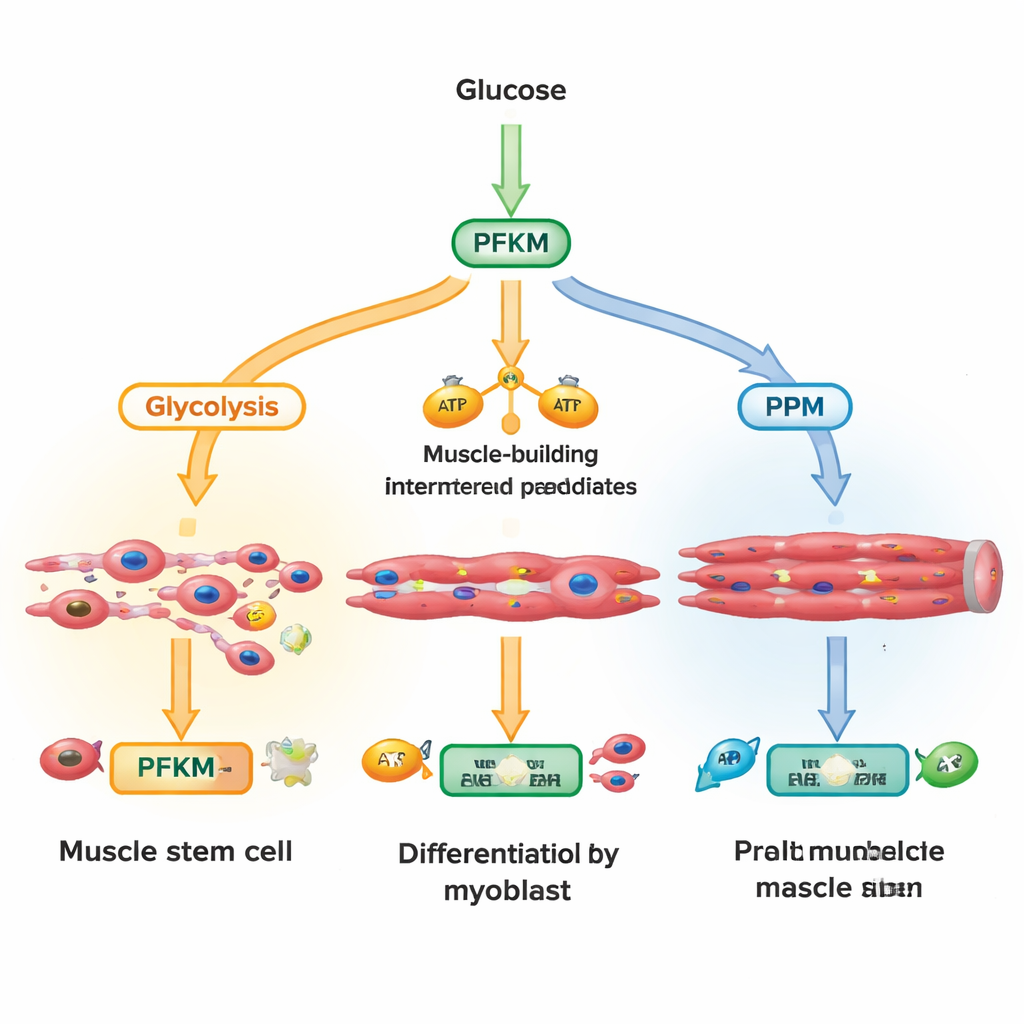
Marcando e removendo a enzima guardiã
Para entender como a PFKM é controlada, a equipe rastreou onde a proteína se localiza dentro das células. Em condições de repouso, a PFKM flutuava por todo o citoplasma. Em minutos após a estimulação por Wnt, ela se agrupou em pontos brilhantes que se sobrepunham aos lisossomos, os compartimentos de degradação proteica da célula. Duas enzimas irmãs, PFKL e PFKP, não se moveram nem alteraram seus níveis, revelando que apenas a forma muscular PFKM era alvo. Testes bioquímicos mostraram que bloquear a função lisossomal impedia a perda de PFKM, enquanto inibir o proteassoma — o outro grande sistema de descarte de proteínas — não teve efeito. Análises de sequência descobriram um curto motivo “methyl arginine degron” único da PFKM. A enzima PRMT1 adicionou uma marca de metilação específica em uma arginina dentro desse motivo, e essa etiqueta permitiu que a maquinaria de microautofagia, incluindo a proteína VPS4, levasse a PFKM aos lisossomos para degradação. Desabilitar PRMT1 ou VPS4 estabilizou a PFKM e bloqueou sua remoção.
Do tronco ao fibra muscular ativa
Usando grandes conjuntos de dados de célula única humana, os autores mapearam os níveis de PFKM entre muitos tipos de células musculares. Células‑tronco musculares, que ficam dormentes até serem necessárias para reparo, tinham pouquíssima PFKM, mas expressavam muitos genes da via das pentoses fosfato e componentes lisossomais. À medida que as células se comprometiam a se tornar músculo e se fundiam em fibras multinucleadas, os transcritos e a proteína PFKM aumentaram drasticamente, enquanto genes-alvo de Wnt e genes lisossomais diminuíram. Em culturas de células musculares humanas e de camundongo, o Wnt rapidamente direcionou a PFKM para os lisossomos em células iniciais mononucleadas, mas não em fibras maduras multinucleadas. Esse padrão apoia um modelo em que células indiferenciadas mantêm baixa PFKM — via degradação lisossomal — para favorecer um metabolismo protetor, reapresentando a enzima à medida que transitam para fibras contráteis exigentes em energia.
O que acontece quando o interruptor emperra
Para testar quão crucial a PFKM é para formar músculo, a equipe reduziu seus níveis com interferência de RNA. Células com pouca PFKM tiveram dificuldade em ativar genes característicos do músculo, produziram menos proteína miosina e formaram fibras multinucleadas menos numerosas e menores, embora o número total de células permanecesse inalterado. O perfil de metabólitos revelou redução de intermediários glicolíticos a jusante e combustíveis do ciclo do ácido tricarboxílico, mas aumento de genes e marcadores da via das pentoses fosfato, juntamente com maior resistência ao estresse oxidativo. Importante, fornecer às células 3‑fosfoglicerato — um intermediário glicolítico que normalmente está a montante da PFKM — resgatou muitos dos defeitos de diferenciação. Marcadores musculares e a formação de fibras se recuperaram, mostrando que os metabólitos ausentes, e não a perda da proteína PFKM em si, eram o principal gargalo. 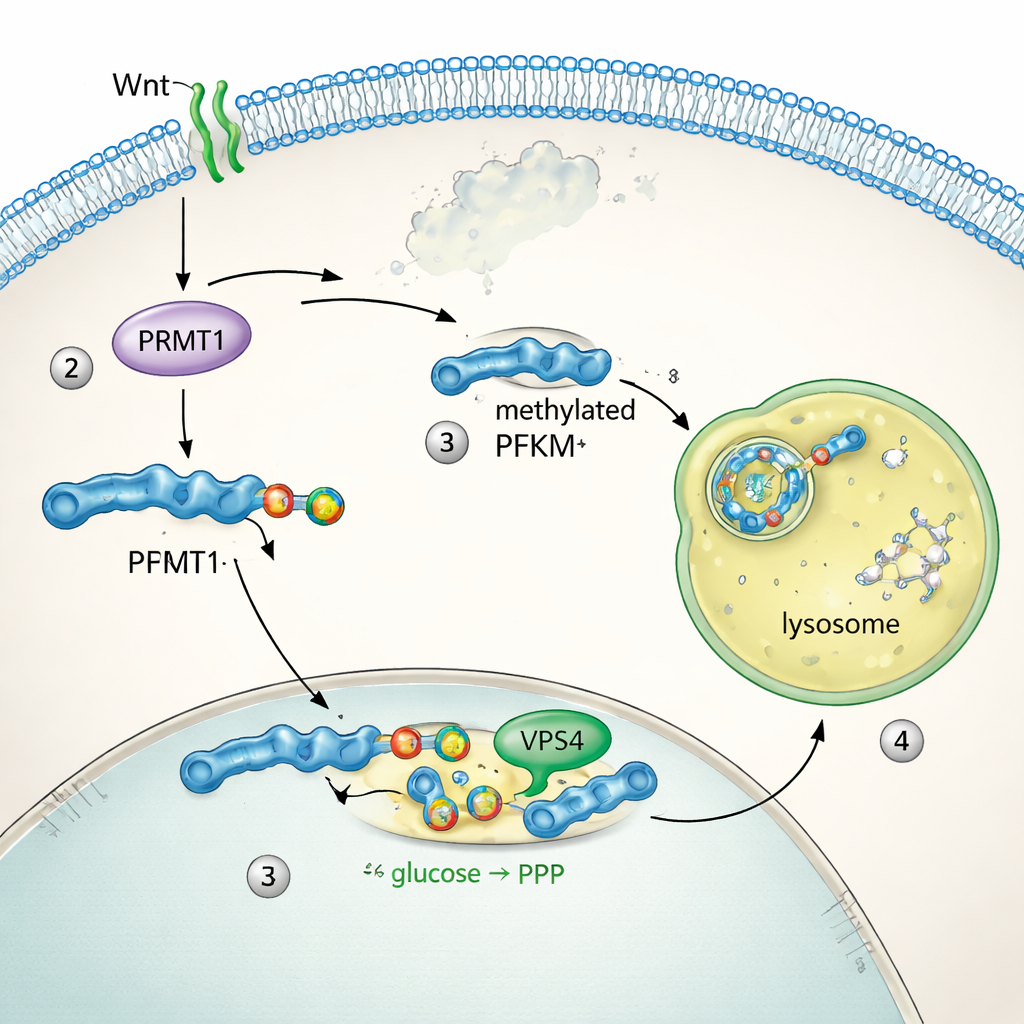
Implicações para saúde e reparo muscular
Para não especialistas, a mensagem central é que as células musculares não apenas “queimam açúcar” mais ou menos; elas redirecionam cuidadosamente a glicose entre produção de energia e proteção celular dependendo de seu estágio de vida. A PFKM age como uma válvula ajustável nesse ponto de decisão. Em células com características de tronco, a marcação dirigida por Wnt e a destruição lisossomal da PFKM redirecionam a glicose para uma via que protege as células e as prepara para crescimento futuro. À medida que as células amadurecem em fibras atuantes, elas reconstruem os estoques de PFKM e inclinam o metabolismo para um uso energético de alta capacidade. Disruptar esse equilíbrio, como visto em raras desordens de deficiência de PFKM, compromete o desenvolvimento muscular normal. Ao revelar o controle molecular desse interruptor, o estudo sugere que terapias futuras poderiam ajustar finamente a regeneração muscular ou proteger músculos em doenças e envelhecimento ao modular modestamente a atividade da PFKM ou suprir os metabólitos apropriados a jusante.
Citação: Campos, M., Nguyen, S.T., Kong, X. et al. PFKM governs metabolic shifts throughout skeletal muscle differentiation. Nat Metab 8, 489–505 (2026). https://doi.org/10.1038/s42255-026-01457-4
Palavras-chave: diferenciação do músculo esquelético, metabolismo da glicose, enzima PFKM, via das pentoses fosfato, degradação proteica lisossomal