Clear Sky Science · pt
Desvendando os mecanismos moleculares causais do diabetes tipo 2 em populações globais e tecidos relevantes para a doença
Por que entender as raízes do diabetes importa
O diabetes tipo 2 afeta centenas de milhões de pessoas no mundo, e ainda sabemos surpreendentemente pouco sobre quais interruptores moleculares no corpo realmente causam a doença em vez de apenas acompanhá‑la. Este estudo mergulha em nosso DNA e em múltiplos órgãos para identificar quais genes e proteínas realmente empurram a glicemia rumo ao diabetes e quais ajudam a protegê‑la. Ao incluir pessoas de diferentes ancestralidades e examinar vários tecidos-chave, os pesquisadores nos aproximam de estratégias de prevenção e terapias mais precisas que podem funcionar para diversas populações, e não apenas para aquelas de ascendência europeia.
Vendo pelo mundo e pelo corpo
A equipe começou com dados genéticos de mais de 2,5 milhões de pessoas reunidos pela Iniciativa Global de Genômica do Diabetes Tipo 2. Em vez de apenas perguntar quais variantes do DNA estão associadas ao diabetes, fizeram uma pergunta mais poderosa: quais variantes alteram a atividade de genes ou proteínas específicos no organismo, e essas alterações por sua vez mudam o risco de diabetes? Para isso, usaram uma abordagem estatística chamada randomização mendeliana, que trata diferenças genéticas naturais como uma espécie de ensaio randomizado embutido. Analisaram mais de 20.000 medidas de atividade gênica e mais de 1.600 proteínas sanguíneas em pessoas de quatro grupos de ancestralidade — europeia, africana, americano admisturado e leste-asiática — e depois repetiram as análises em sete tecidos centrais para o controle da glicemia, incluindo pâncreas, ilhotas produtoras de insulina, fígado, músculo e diferentes depósitos de gordura.
Encontrando alavancas moleculares que aumentam ou reduzem o risco
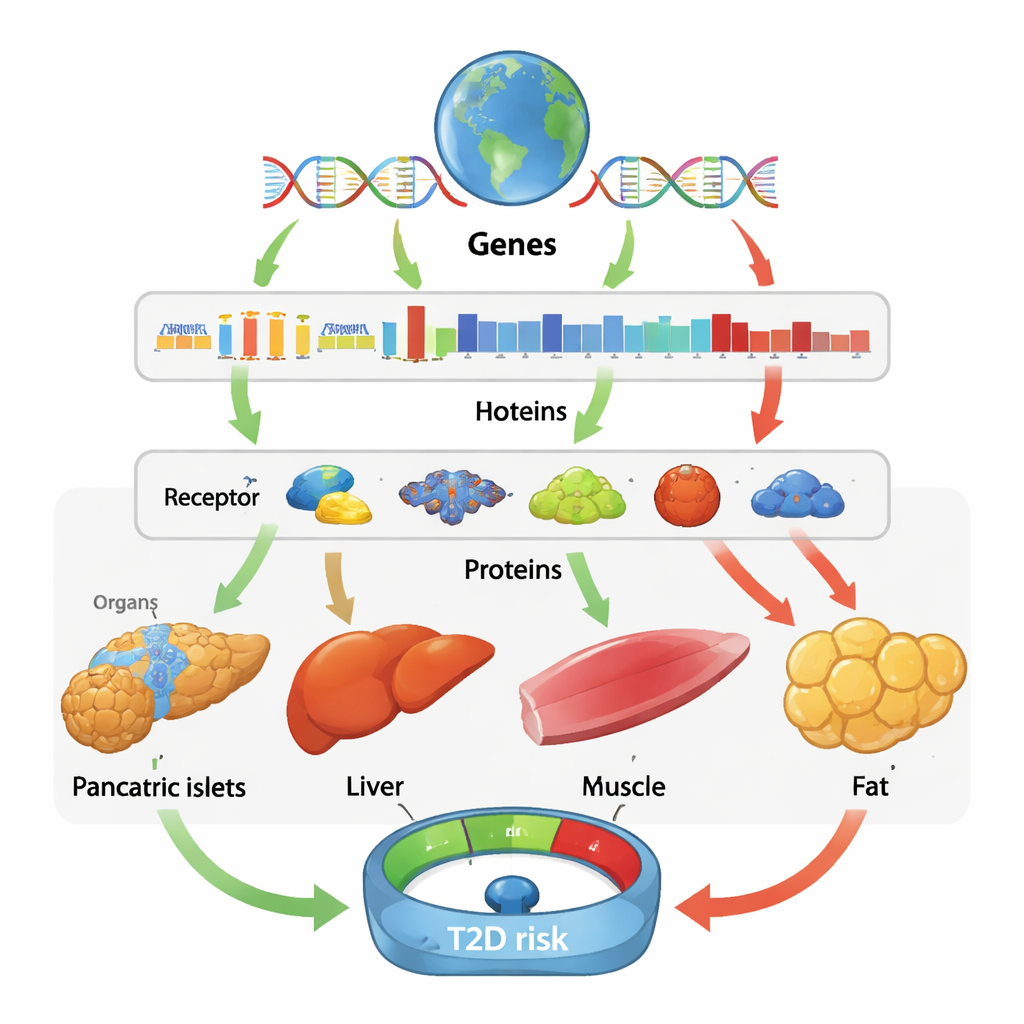
Ao traçar essas vias genéticas, os pesquisadores identificaram 335 genes e 46 proteínas sanguíneas cujos níveis preditos geneticamente têm impacto causal no risco de diabetes tipo 2, e confirmaram muitas dessas descobertas em coortes independentes. Algumas das alavancas moleculares já eram suspeitas, como MTNR1B, um gene envolvido na liberação de insulina pelas células das ilhotas pancreáticas, e BAK1, que influencia a morte celular no pâncreas e na gordura. Outras foram jogadores novos ou menos apreciados, incluindo CPXM1, uma proteína ligada ao desenvolvimento do tecido adiposo e à resistência à insulina, e HIBCH, um gene envolvido na função mitocondrial. No total, catalogaram 923 genes e 46 proteínas com evidência de que alterar sua atividade em pelo menos um tecido pode modificar as chances de desenvolver diabetes.
Mesmos genes, histórias diferentes entre tecidos e populações
Uma lição marcante é que o efeito de um gene costuma ser altamente específico ao tecido. Por exemplo, maior atividade de BAK1 no pâncreas e nas ilhotas parece aumentar o risco de diabetes, provavelmente ao contribuir para a perda de células produtoras de insulina, enquanto maior BAK1 na gordura e no músculo parece ser protetor. HIBCH mostrou um padrão igualmente misto: em alguns tecidos, mais atividade reduzia o risco de diabetes, enquanto em outros o aumentava. Esses achados mostram que olhar apenas para o sangue pode perder biologia crucial que ocorre dentro dos órgãos, e que a mesma molécula pode ser benéfica em um tecido e prejudicial em outro. Em contraste, quando a equipe comparou resultados entre ancestralidades, observou relativamente pouca diferença nos tamanhos de efeito, sugerindo que muitos dos mecanismos causais subjacentes são compartilhados globalmente, embora certos sinais — como proteínas protetoras ou de risco específicas em grupos leste-asiáticos ou africanos — só tenham sido detectáveis graças a dados não europeus.
Conectando novos achados à biologia conhecida do diabetes
Para verificar se a abordagem fazia sentido biológico, os autores cruzaram seus genes causais com listas curadas de genes relacionados ao diabetes provenientes de estudos humanos e experimentos em camundongos. Genes com as evidências prévias mais fortes de envolvimento no diabetes foram muito mais propensos a mostrar efeitos causais em suas análises do que genes escolhidos ao acaso. Além disso, os tecidos em que esses efeitos causais apareciam correspondiam a mecanismos de doença conhecidos: genes ligados à falha de células beta tendiam a importar mais nas ilhotas pancreáticas, enquanto genes associados à síndrome metabólica mostravam seus efeitos mais fortes na gordura visceral (gordura abdominal profunda). Esse alinhamento apoia a ideia de que o pipeline estatístico está identificando mecanismos, e não apenas correlações.
O que isso significa para tratamento e prevenção futuros
Para quem não é especialista, a conclusão principal é que este trabalho transforma longas e impessoais listas de variantes de DNA em um mapa mais claro de genes, proteínas e órgãos que realmente impulsionam o diabetes tipo 2. Ao distinguir causa de efeito e revelar quando a mesma molécula tem papéis opostos em diferentes tecidos, fornece aos desenvolvedores de medicamentos alvos mais precisos e alerta para onde uma terapia única para todos pode sair pela culatra. Importante, ao incluir deliberadamente populações diversas, o estudo ajuda a garantir que quaisquer medicamentos futuros ou scores de risco construídos com base nesses insights tenham maior probabilidade de funcionar amplamente, e não apenas para pessoas de ascendência europeia.
Citação: Bocher, O., Arruda, A.L., Yoshiji, S. et al. Unravelling the molecular mechanisms causal to type 2 diabetes across global populations and disease-relevant tissues. Nat Metab 8, 506–520 (2026). https://doi.org/10.1038/s42255-025-01444-1
Palavras-chave: diabetes tipo 2, mecanismos genéticos, genômica multi-ancestral, expressão gênica específica por tecido, inferência causal