Clear Sky Science · pt
O fluxo catabólico de cisteína regulado por Lamin A/C modula o destino de células‑tronco por meio da reprogramação do epigenoma
Como o esqueleto da célula conversa com seu metabolismo
Por que algumas células permanecem jovens e flexíveis em relação ao que podem se tornar, enquanto outras envelhecem ou travam numa identidade errada? Este estudo revela uma conversa surpreendente dentro das células entre o “andaime” nuclear que organiza o DNA e um nutriente contendo enxofre, a cisteína. Ao mostrar como esse diálogo direciona as células‑tronco para destinos saudáveis — ou para envelhecimento precoce — o trabalho sugere que o que as células “comem” e como o metabolizam poderia um dia ser ajustado para prevenir certas doenças genéticas e talvez até desacelerar aspectos do envelhecimento.
O papel oculto da casca nuclear
Dentro de cada célula, o DNA fica apoiado numa malha proteica chamada lâmina nuclear, formada em parte por proteínas chamadas lamin A e C. Essas lamínas não apenas dão forma ao núcleo; elas também ajudam a decidir quais genes ficam bloqueados e quais permanecem acessíveis. Os autores estudaram células‑tronco embrionárias de camundongo em seu estado mais flexível, ou “naive”, e descobriram que lamin A/C normalmente reprime duas enzimas metabólicas, CBS e CTH, que participam da síntese e degradação da cisteína. Quando lamin A/C está presente e ativa, essas enzimas são contidas e o processamento da cisteína permanece baixo, sustentando um estado estável e jovem da célula‑tronco. 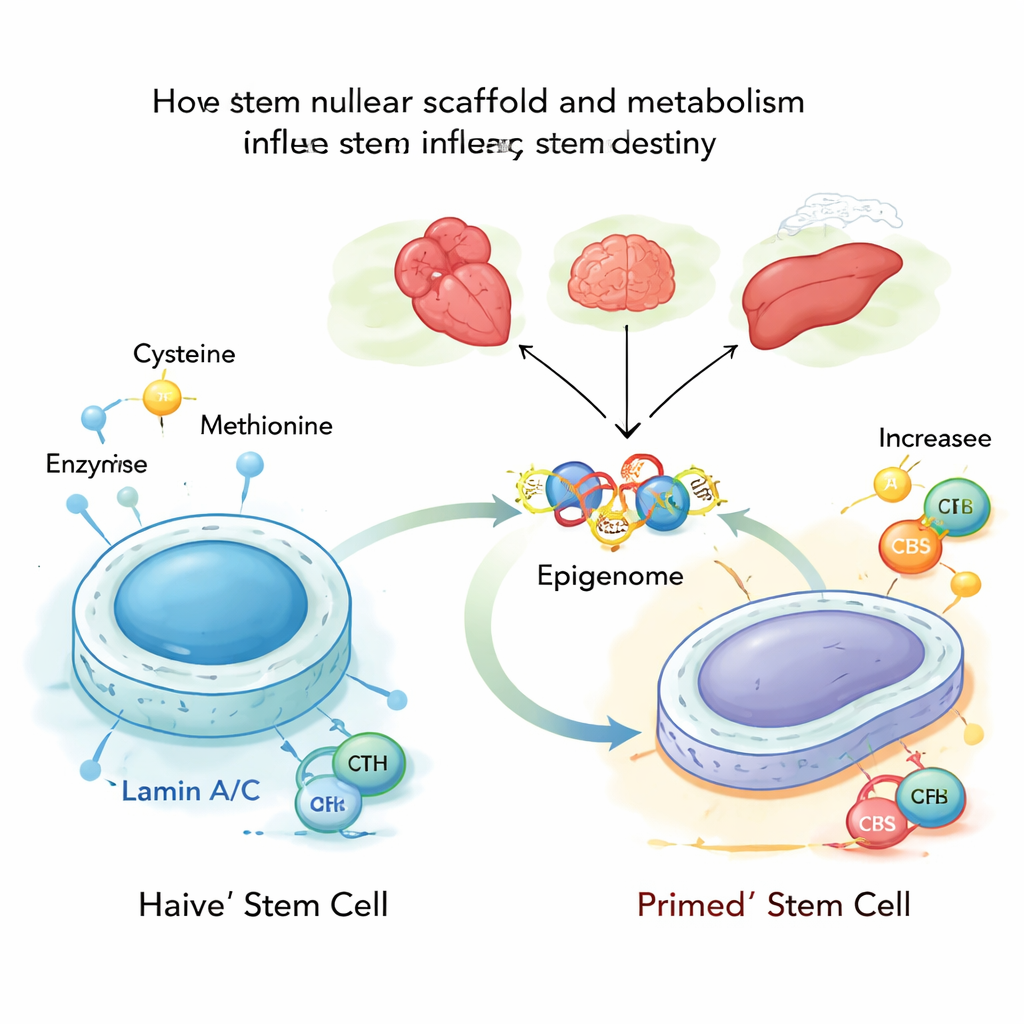
Quando a estrutura falha, o metabolismo acelera
Em seguida, os pesquisadores removeram lamin A/C ou introduziram uma mutação ligada a doença que imita um distúrbio humano de envelhecimento precoce chamado progeria de Hutchinson–Gilford. Sem lamin A/C normais, os genes CBS e CTH tornam‑se mais acessíveis e mais fortemente ligados por um fator de transcrição chamado SP1, sendo ativados. Essa mudança empurra mais cisteína por uma via metabólica que termina em acetil‑CoA, uma pequena molécula que carrega grupos acetil usados para afrouxar o empacotamento do DNA. À medida que mais cisteína é canalizada para acetil‑CoA, os grupos acetil passam a ser adicionados preferencialmente em locais específicos das histonas — especialmente em duas posições da histona H3 conhecidas como K9 e K27 — tornando genes próximos mais fáceis de serem ativados.
Das marcas químicas às decisões de destino celular
Essas mudanças nas “etiquetas” das histonas atuam como uma retificação global do painel de controle da célula. Em células‑tronco naive, aumentar CBS e CTH, ou simplesmente fornecer mais cisteína, empurra as células para um estado mais avançado, “primed”, mais próximo de formar tecidos reais. Genes envolvidos no desenvolvimento cardíaco e em outras linhagens tornam‑se mais ativos, e o dobramento tridimensional do DNA muda para favorecer esses programas. Inversamente, reduzir CBS e CTH ou limitar a cisteína ajuda a restaurar uma identidade mais naive e jovem, mesmo quando a lâmina nuclear está danificada. Em modelos embrionários, esse desvio metabólico levou à formação desequilibrada das três camadas germinativas — os primeiros blocos de construção de todos os órgãos — e a um viés anômalo em direção a células do músculo cardíaco, a menos que CBS e CTH fossem reequilibradas. 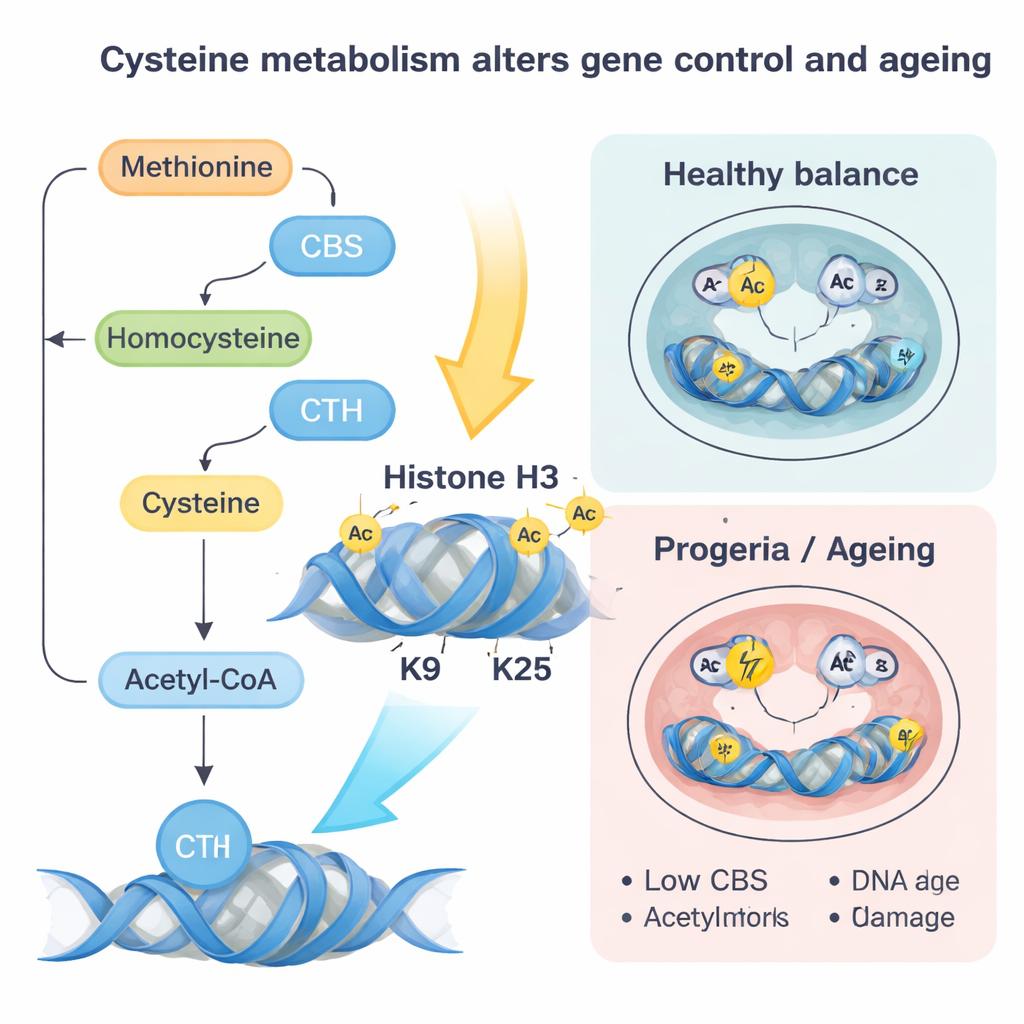
Metabolismo, marcas no DNA e envelhecimento precoce
A mutação tipo progeria em lamin contou uma história complementar. Aqui, os níveis de CBS e CTH caem, reduzindo o fluxo de cisteína e a produção de acetil‑CoA por essa via. Ao mesmo tempo, a homocisteína é redirecionada de volta para o ciclo da metionina, aumentando os níveis de SAM, o doador universal de grupos metil. Isso favorece marcas de metil extras, especialmente uma chamada H3K9me3 colocada pela enzima SUV39H1, que compacta a cromatina e está associada à reparação de DNA prejudicada. Os autores mostraram que restaurar suavemente CBS ou restringir metionina reduziu o SAM, diminuiu essas marcas metílicas repressoras, melhorou a reparação do DNA, reduziu o estresse oxidativo e marcadores de senescência, e resgatou parcialmente a diferenciação em cardiomiócitos. Quedas semelhantes em CBS e aumentos em marcas repressoras foram observados em corações envelhecidos de camundongo e em fibroblastos humanos de pessoas idosas e pacientes com progeria, sugerindo que esse circuito também opera no envelhecimento natural.
O que isso significa para saúde e envelhecimento
Para um leitor não especializado, a mensagem é que a estrutura celular e seu metabolismo estão intimamente ligados: quando a “casca” nuclear feita de lamin A/C é perturbada, a forma como a cisteína é utilizada muda, o que por sua vez reescreve marcas químicas nas proteínas que empacotam o DNA. Essas marcas decidem quais genes são ativados enquanto as células‑tronco constroem o corpo e influenciam quão bem as células repararam danos ao longo da vida. Ao ajustar cuidadosamente enzimas como CBS e CTH — ou alterando a oferta de nutrientes como metionina e cisteína — pode ser possível corrigir parte da escrita incorreta dessas marcas em doenças ligadas à lamina e, talvez, mitigar aspectos do envelhecimento precoce ou normal.
Citação: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
Palavras-chave: células‑tronco, lámina nuclear, metabolismo da cisteína, epigenética, envelhecimento