Clear Sky Science · pt
ABEL-FRET elimina o hiato de escala temporal em medidas de molécula única da dinâmica estrutural do receptor de adenosina A2A
Observando minúsculos interruptores celulares em tempo real
Muitos medicamentos atuais atuam ao ativar ou desativar “interruptores” moleculares na superfície das células chamados receptores. Esses interruptores mudam constantemente de forma ao ligar e desligar sinais, mas a maioria das ferramentas enxerga apenas os movimentos muito mais rápidos ou os muito mais lentos — não ambos. Este artigo apresenta um método para observar um único receptor alvo de fármaco em solução por muito mais tempo do que antes, revelando como ele permanece em determinadas conformações que são cruciais para a ação dos medicamentos.
Por que essas proteínas que mudam de forma importam
O estudo foca em uma classe importante de proteínas de superfície celular conhecidas como receptores acoplados a proteína G, ou GPCRs. Essas proteínas controlam processos vitais, incluindo visão, humor, pressão arterial e respostas imunes, e mais de um terço dos medicamentos aprovados age sobre elas. Um membro bem estudado, o receptor de adenosina A2A, ajuda a regular sono, dor, inflamação e sinalização cerebral, sendo um alvo promissor para tratar distúrbios como a doença de Parkinson e câncer. Os GPCRs são altamente flexíveis: quando diferentes moléculas se ligam, elas empurram o receptor para conformações distintas que favorecem algumas vias de sinalização em detrimento de outras. Essa própria flexibilidade, contudo, torna difícil projetar fármacos com base em imagens estáticas de raios X ou criomicroscopia eletrônica.
Acompanhando um único receptor sem imobilizá‑lo
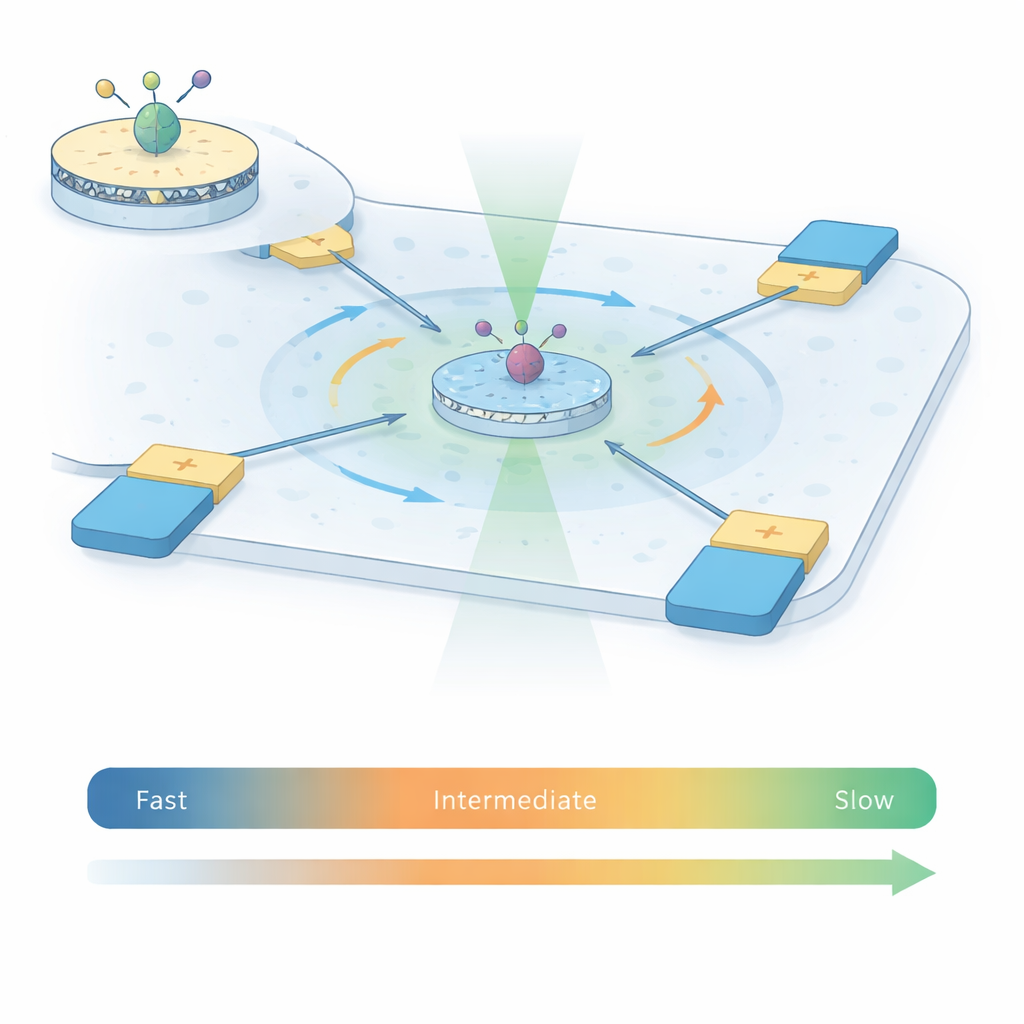
Para capturar como os receptores A2A se movem, os autores combinam duas técnicas poderosas no que chamam ABEL‑FRET. Primeiro, eles reconstituem receptores individuais em pequenos fragmentos de membrana artificial chamados nanodiscos, fornecendo a cada proteína um ambiente mais natural do que detergente isolado. Eles prendem um par de corantes fluorescentes a duas partes móveis no interior do receptor. À medida que o receptor muda de forma, a distância e a orientação relativa entre esses corantes variam, alterando a transferência de energia entre eles — um fenômeno conhecido como transferência de energia por ressonância de Förster (FRET). Segundo, em vez de fixar o receptor a uma superfície, usam uma armadilha anti‑Browniana eletrocinética (ABEL): uma câmara microfluídica com eletrodos que detectam onde está uma partícula fluorescente e a empurram suavemente de volta ao centro, contra‑atacando a movimentação aleatória browniana.
Preenchendo a janela de tempo ausente
Experimentos tradicionais de FRET de molécula única observam receptores que se difundem livremente por apenas alguns milésimos de segundo, ou receptores imobilizados em superfície por segundos a minutos. Cada abordagem cobre uma janela de tempo diferente. Usando a armadilha ABEL, este trabalho mantém receptores A2A individuais visíveis por um a dois segundos enquanto permanecem livres em solução — cerca de 100 vezes mais do que em experimentos limitados pela difusão. Esse tempo de observação estendido permite à equipe medir como o sinal de FRET flutua dentro de cada período de captura e entre milhares de receptores, sob quatro condições: sem ligante, com um antagonista e com dois diferentes ativadores (agonistas). Ferramentas estatísticas emprestadas da análise de sinais — variância, correlação e análises de recorrência — permitem distinguir o ruído aleatório de fótons de verdadeiras alterações estruturais lentas no receptor.
Conformações longas e escondidas reveladas
As leituras de FRET mostram que os receptores ocupam várias conformações distintas que não se interconvertem totalmente durante os tempos típicos de observação de algumas centenas de milissegundos. Em todas as condições, a dispersão dos valores de FRET é bem mais ampla do que o esperado apenas pelo ruído, revelando heterogeneidade estrutural: moléculas diferentes permanecem em conformações longas distintas. Quando moléculas ativadoras se ligam, o nível médio de FRET desloca‑se para cima, indicando que o receptor passa mais tempo em um arranjo “semelhante ao ativo” de suas hélices internas. Ainda assim, as análises de correlação mostram que, uma vez que um receptor está em um estado de FRET alto ou intermediário, há grande probabilidade de permanecer ali por pelo menos centenas de milissegundos. Esses resultados atualizam estimativas anteriores baseadas em experimentos mais rápidos, estendendo os tempos característicos de permanência em estados de longa duração de meros milissegundos para bem acima de um décimo de segundo.
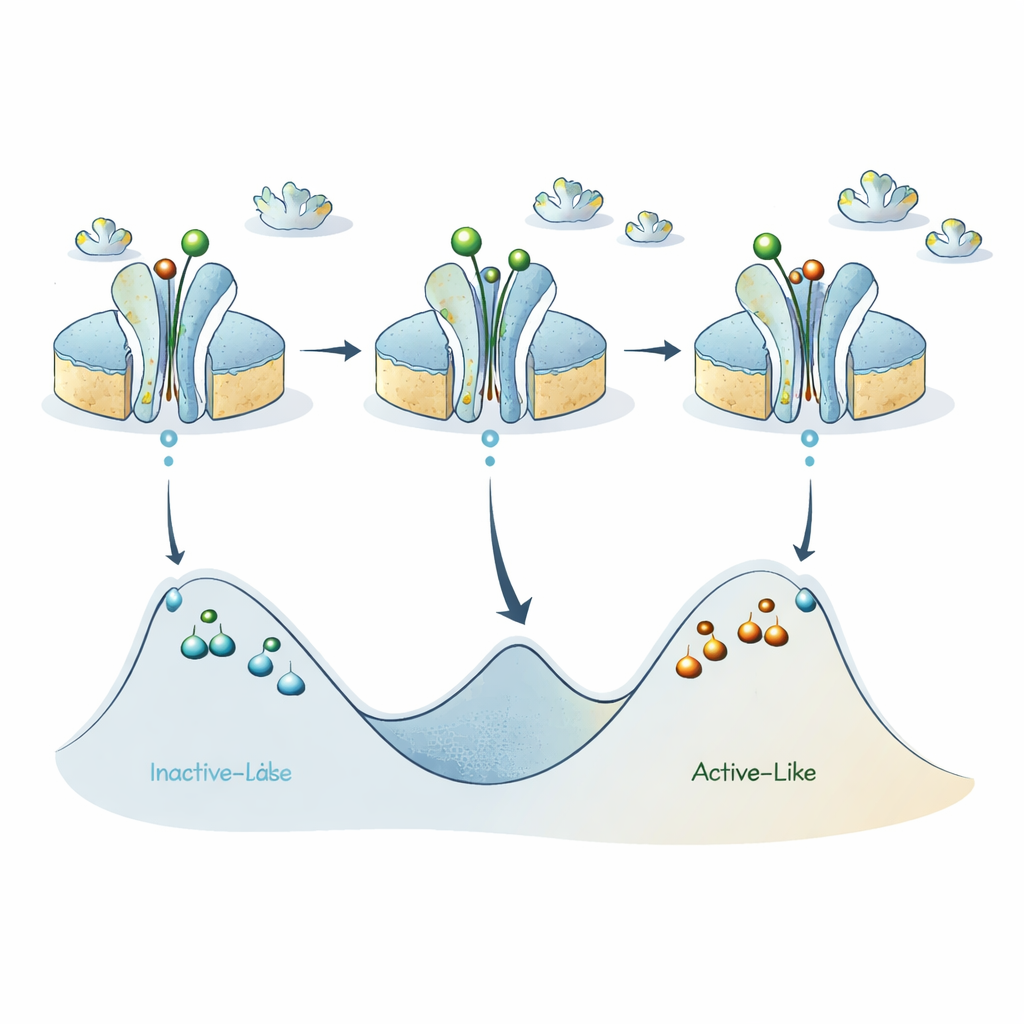
Um novo mapa da paisagem energética do receptor
Ao juntar essas peças, os autores refinam um modelo anterior em que o receptor A2A alterna principalmente entre um estado semelhante ao inativo e um estado semelhante ao ativo. Seus novos dados sugerem que cada uma dessas duas categorias amplas, na verdade, oculta vários subestados separados por barreiras energéticas consideráveis, de modo que receptores individuais podem ficar “presos” em uma versão ativa‑parecida ou inativa‑parecida por tempos surpreendentemente longos. Ligantes ativadores abaixam a barreira entre as bacias principais inativa e ativa, promovendo alternância rápida em escala sub‑milissegundo, mas as barreiras internas dentro de cada bacia permanecem altas, dando origem aos subestados de longa duração que o ABEL‑FRET detecta.
O que isso significa para medicamentos futuros
Para não‑especialistas, a mensagem principal é que um alvo de fármaco como o receptor A2A não simplesmente alterna entre “desligado” e “ligado”. Em vez disso, ele explora uma paisagem rugosa de conformações, algumas das quais persistem tempo suficiente para influenciar como os sinais são transmitidos dentro das células e como os medicamentos atuam ao longo do tempo. Ao estender o tempo durante o qual receptores individuais podem ser observados em seu estado natural, não fixado, o ABEL‑FRET preenche uma lacuna crucial entre medidas ultrarrápidas e muito lentas. Essa abordagem pode agora ser aplicada a muitas proteínas de membrana, oferecendo uma imagem mais completa e temporalmente resolvida de como alvos potenciais de medicamentos respiram, mudam e respondem a compostos terapêuticos.
Citação: Maslov, I., Borshchevskiy, V., Pérez, I. et al. ABEL-FRET bridges the timescale gap in single-molecule measurements of the structural dynamics in the A2A adenosine receptor. Commun Chem 9, 114 (2026). https://doi.org/10.1038/s42004-026-01941-8
Palavras-chave: receptores acoplados a proteína G, FRET de molécula única, receptor de adenosina A2A, dinâmica conformacional de proteínas, armadilha ABEL