Clear Sky Science · pt
Estudo mecanístico sobre a migração de sulfato em glicosaminoglicanos durante a fragmentação em EM
Por que a mudança de marcadores químicos em açúcares importa
Nossas células são revestidas por longas cadeias de açúcares que ajudam a controlar processos tão diversos quanto coagulação sanguínea, defesa imunológica e a forma como vírus se ligam às células. Muitas dessas cadeias carregam pequenos marcadores químicos chamados grupos sulfato, cujas posições exatas ao longo da espinha dorsal do açúcar funcionam como um código molecular, indicando quando e onde proteínas devem se ligar. Os cientistas dependem fortemente da espectrometria de massas, uma técnica poderosa de pesagem, para ler esses códigos. Este estudo revela que, durante tais medições, os grupos sulfato podem silenciosamente deslocar-se de posição, potencialmente enganando os pesquisadores sobre a verdadeira arquitetura desses açúcares biologicamente cruciais.
Cadeias de açúcar complexas com marcadores críticos
Os glicosaminoglicanos são longas cadeias lineares de açúcares frequentemente ligadas a proteínas na superfície celular. Suas decorações de sulfato não são aleatórias; pequenas mudanças na posição de um grupo sulfato em uma unidade de açúcar podem alterar radicalmente como a cadeia interage com fatores de crescimento, proteínas da coagulação ou patógenos. Por isso, os cientistas tentam determinar não apenas quantos sulfatos existem, mas exatamente onde eles se localizam. A espectrometria de massas, frequentemente combinada com fragmentação controlada das cadeias de açúcar, é uma das principais maneiras de fazer isso. No entanto, indícios anteriores sugeriam que grupos carregados como os sulfatos podem se mover durante a medição, complicando os esforços para decifrar o padrão real de modificações.
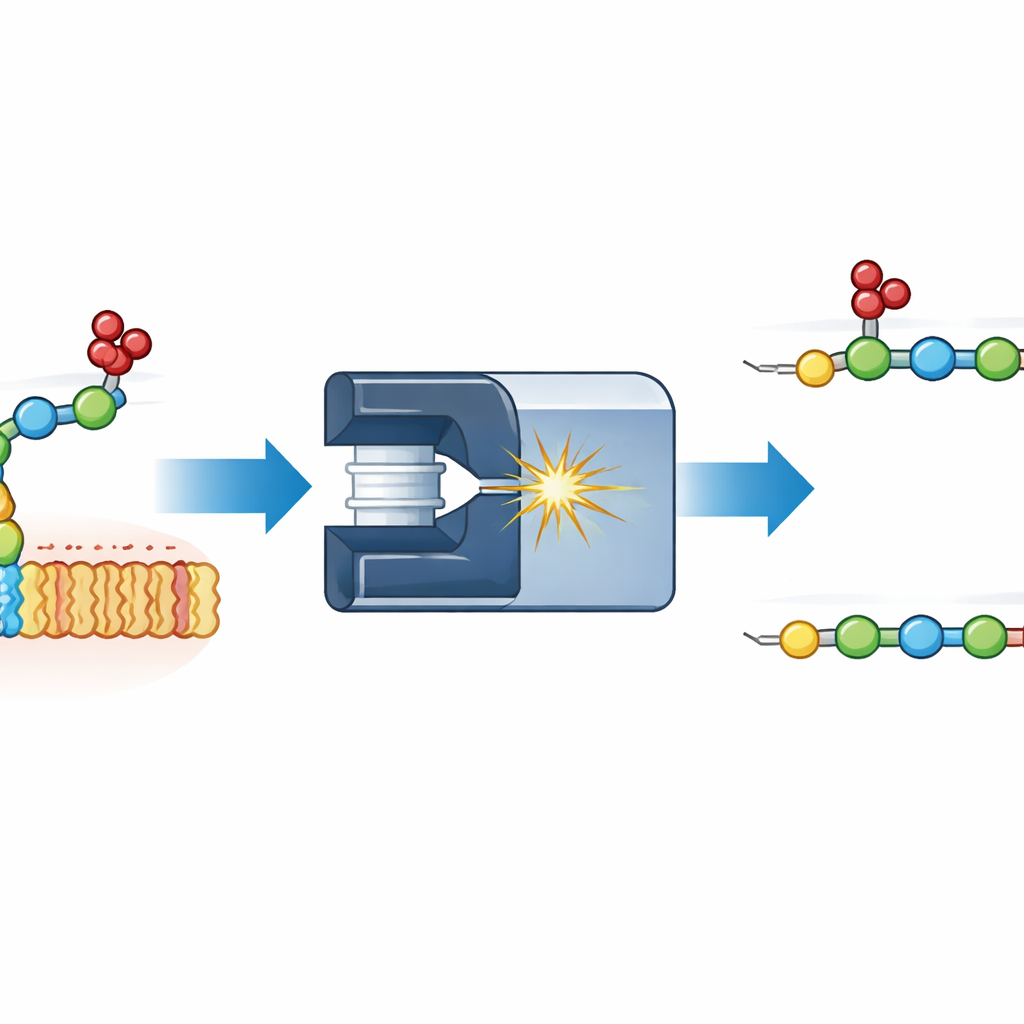
Observando sulfatos moverem-se durante a medição
Os autores focaram em um modelo simples: um fragmento de dois açúcares do heparan sulfato, um dos glicosaminoglicanos mais conhecidos. Eles anexaram diferentes rótulos fluorescentes a uma extremidade do dissacarídeo e o fragmentaram dentro de um espectrômetro de massas. Medindo como os pedaços resultantes derivavam através de um gás sob um campo elétrico — uma técnica chamada mobilidade iônica — eles puderam distinguir conformações que, de outra forma, teriam a mesma massa. Surgiu um fragmento inesperado que era exatamente mais pesado por um grupo sulfato no lugar errado: em vez de permanecer no primeiro açúcar, o sulfato havia migrado para o segundo. Comparações com compostos de referência cuidadosamente sintetizados mostraram que o sulfato migrante podia pousar em dois pontos distintos do segundo açúcar, gerando duas conformações diferentes que foram claramente resolvidas pela mobilidade iônica.
Localizando novos pontos de aterrissagem e testando rótulos
Para entender melhor onde o sulfato terminou e se outras posições eram possíveis, a equipe combinou suas medições com simulações computacionais detalhadas. Eles calcularam muitas formas tridimensionais possíveis para as estruturas candidatas e previram como cada uma deveria se deslocar na fase gasosa. Apenas sulfatos localizados em dois sítios específicos do segundo açúcar — conhecidos entre especialistas como posições 6O e 3O — corresponderam ao comportamento experimental, enquanto outras localizações hipotéticas pareceram improváveis. Os pesquisadores então testaram se os próprios rótulos anexados poderiam estar impulsionando a reorganização, substituindo o rótulo original por três mais simples. Em todos os casos, a migração de sulfato persistiu e produziu fragmentos de natureza semelhante, indicando que a escolha do rótulo tem pouco efeito sobre se a migração ocorre, embora possa alterar sutilmente quão facilmente os diferentes produtos podem ser distinguidos.
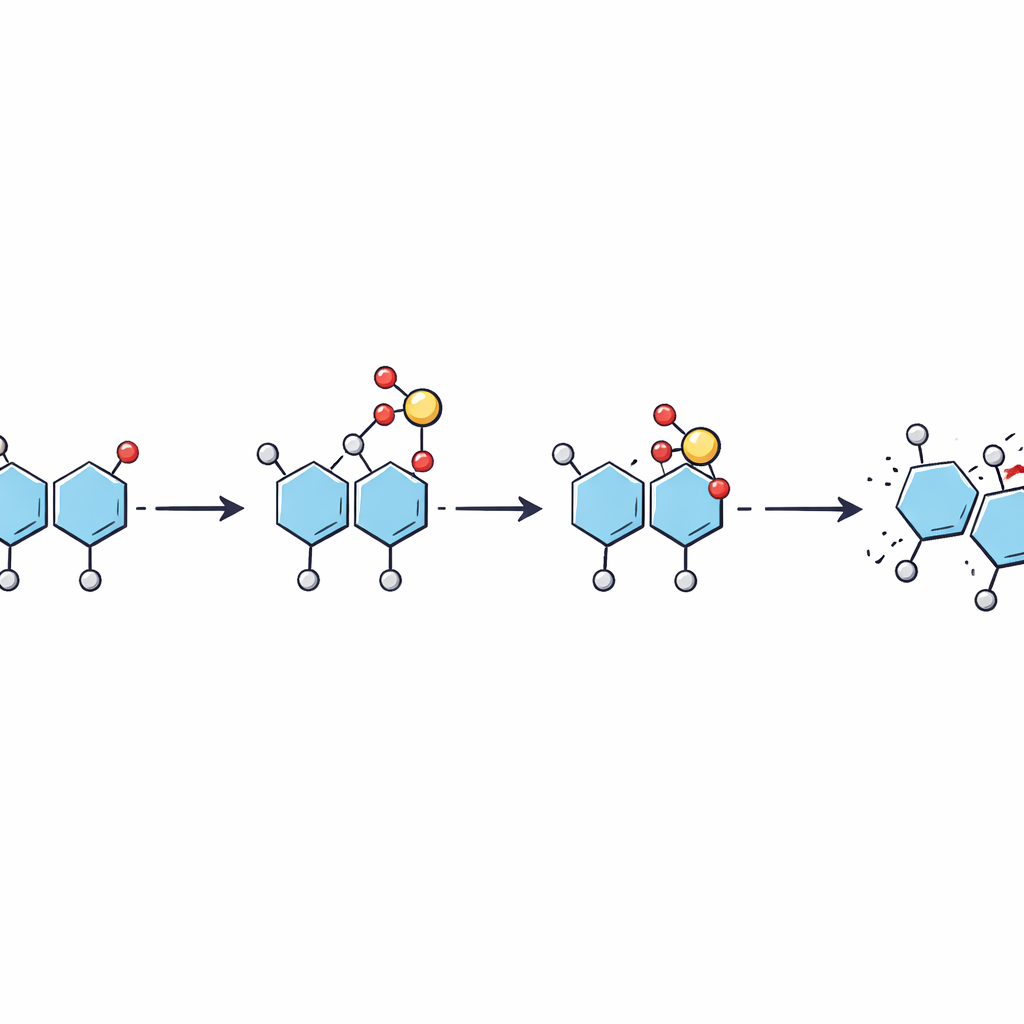
Salto em etapas em vez de um único pulo
Usando experimentos de fragmentação com energia ajustada juntamente com novas simulações, os autores montaram um quadro passo a passo de como o sulfato se move. À medida que o íon é energizado no espectrômetro de massas, um próton móvel primeiro ativa o grupo sulfato, que então salta do açúcar original para um sítio particular no açúcar vizinho enquanto a ligação entre eles se rompe. Isso produz um fragmento no qual o sulfato se encontra em uma posição intermediária. Com energia adicional, o sulfato pode deslocar-se novamente ao longo do mesmo açúcar até um sítio mais estável. O trabalho sugere que esses rearranjos podem ocorrer a energias inferiores às necessárias para quebrar a espinha dorsal do açúcar, o que significa que eles podem acontecer discretamente em análises rotineiras.
O que isso significa para decodificar estruturas de açúcares
Para não especialistas, a mensagem principal é que os marcadores químicos em açúcares biológicos importantes nem sempre estão congelados no lugar durante a análise; eles podem deslizar ao longo da cadeia enquanto a molécula voa pelo espectrômetro de massas. O estudo mostra em detalhe que, ao menos para um fragmento representativo de heparan sulfato, um grupo sulfato pode migrar de uma unidade de açúcar para outra e então se estabelecer em novas posições, produzindo fragmentos enganadores que imitam características estruturais genuínas. Isso significa que algumas medições passadas e futuras podem interpretar mal o código do sulfato, a menos que técnicas adicionais, como mobilidade iônica e modelagem avançada, sejam usadas para detectar esses movimentos ocultos. O trabalho pede estudos mais sistemáticos para avaliar quão disseminada é essa migração de sulfato, para que os pesquisadores possam associar de forma mais confiável os padrões de açúcares na superfície celular à saúde e à doença.
Citação: Polewski, L., Yaman, M., Tokić, M. et al. Mechanistic study on the sulfate migration in glycosaminoglycans during MS fragmentation. Commun Chem 9, 130 (2026). https://doi.org/10.1038/s42004-026-01939-2
Palavras-chave: heparan sulfato, glicosaminoglicanos, espectrometria de massas, migração de sulfato, mobilidade iônica