Clear Sky Science · pt
A profundidade da pose de ligação modula a eficácia de ligantes fotosswitch no receptor 5-HT2A
Iluminando drogas cerebrais comutáveis
Imagine um medicamento que você pudesse ligar e desligar com um flash de luz, direcionando receptores cerebrais com precisão e evitando efeitos colaterais. Este estudo explora exatamente essa ideia para um receptor de serotonina-chave ligado ao humor, percepção e drogas psicodélicas. Os pesquisadores investigaram por que duas moléculas fotossensíveis quase idênticas se comportam de forma tão diferente — uma age quase como um interruptor perfeito liga/desliga, enquanto a outra se recusa teimosamente a apagar totalmente. A resposta se reduz a um fator surpreendentemente simples: quão profundamente a molécula se aloja dentro do receptor.
Medicamentos acionados por luz no cérebro
Drogas ativadas por luz, também chamadas de ferramentas fotofarmacológicas, são projetadas de modo que um feixe de luz vire parte da molécula entre duas formas, como uma versão dobrada e outra esticada. Essas formas podem alterar a força com que a droga se liga ao alvo. Neste trabalho, o alvo é o receptor humano 5-HT2A, uma proteína nas células cerebrais que responde à serotonina e é central tanto para efeitos antipsicóticos quanto psicodélicos. As moléculas estudadas são derivados da N,N-dimetiltriptamina (DMT), modificados com uma unidade fotossensível azobenzeno. Duas versões diferem apenas em onde um pequeno grupo metoxi é colocado em um anel — na posição “para” ou “meta” —, e ainda assim seu comportamento biológico sob luz é dramaticamente diferente.
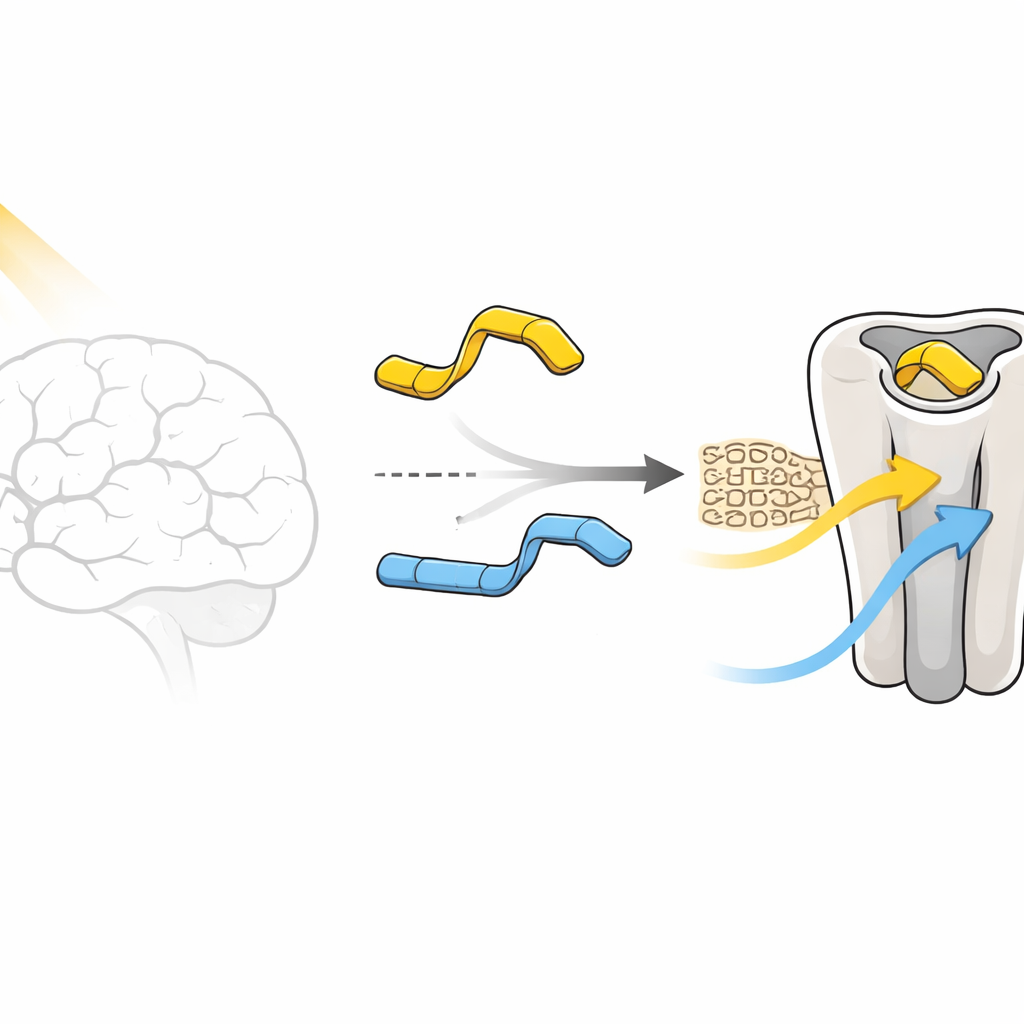
Duas moléculas quase gêmeas, comutadores muito diferentes
Em testes celulares, a versão para, chamada composto 1, comporta-se quase como um interruptor digital. No escuro, sua forma “trans” mal ativa o receptor e até o bloqueia ligeiramente, atuando como um antagonista fraco. Quando a luz a transforma na forma “cis”, a mesma molécula torna-se um ativador moderado, ligando parcialmente o receptor. A versão meta, composto 2, recusa cooperar dessa maneira: tanto sua forma à luz quanto a do escuro mantêm o receptor razoavelmente ativo, nunca entregando um verdadeiro estado “desligado”. O quebra-cabeça central deste trabalho é por que uma alteração química tão mínima — apenas mover um pequeno grupo ao redor de um anel — muda tão fortemente a resposta do receptor.
Espiando por dentro com filmes ao nível atômico
Para resolver isso, a equipe utilizou extensas simulações de dinâmica molecular tudo-átomo, rodando efetivamente filmes detalhados de cada átomo no receptor, a membrana circundante, a água e cada ligante ao longo de um total de cerca de 80 microssegundos. Eles simularam ambas as moléculas em cada uma de suas formas controladas por luz e nas formas inativa e ativa do receptor 5-HT2A. Ao rastrear “microswitches” estruturais conhecidos dentro da proteína — como um triptofano-chave que muda de posição, uma ponte salina que se rompe e o movimento de sódio e água no núcleo profundo — puderam determinar quando o receptor tendia a um estado desligado ou ligado. Também compararam o quão perto as novas moléculas imitavam a postura de ligação do LSD, um ativador parcial bem estudado, usando a sobreposição de seus sistemas de anel como guia.
Profundidade importa mais do que só a forma
O insight central é que a eficácia das moléculas é governada principalmente por quão profundamente elas se inserem no bolso de ligação do receptor. No receptor inativo, a forma trans do composto para faz um conjunto especial de ligações de hidrogênio que a puxam incomumente para baixo, abaixo da região onde ocorrem os contatos típicos ativadores. Essa “sobre-inserção” impede que toque resíduos polares chave que ajudam a ligar o receptor, de modo que estabiliza o estado desligado. A forma trans do composto meta não pode fazer os mesmos contatos de ancoragem e, em vez disso, fica mais acima em uma pose mais parecida com a do LSD, compatível com ativação, explicando sua atividade residual. Quando a luz transforma ambas as moléculas em suas formas cis, elas em geral migram para posições mais rasas, mais parecidas com ativadores. Ainda assim, mesmo aí, a geometria importa: no receptor ativo, o cis do composto 2 pode deslizar mais fundo em um túnel hidrofóbico entre duas hélices e formar uma ligação de hidrogênio persistente que reforça seu comportamento fortemente agonista, enquanto o cis do composto 1 é estorvado estéricamente de fazê-lo.
Controle fino de água interna e íons
As simulações também mostram que a profundidade de ligação ajusta sutilmente um bolso interno de sódio e uma via de água que são conhecidos por influenciar a ativação do receptor. A ligação profunda e rígida pelo composto para em sua forma trans mantém um íon sódio fortemente confinado e a região circundante relativamente seca, características associadas a um estado desligado. Em contraste, a ligação mais móvel do composto meta ou das formas cis permite que mais água invada e afrouxe o ambiente do sódio, preparando o receptor para ativação. Um resíduo aromático chave que funciona como “interruptor” pode inverter sua orientação mais facilmente quando os ligantes são flexíveis e não excessivamente ancorados, empurrando ainda mais o receptor para um estado tipo ligado, especialmente com o cis do composto 2.
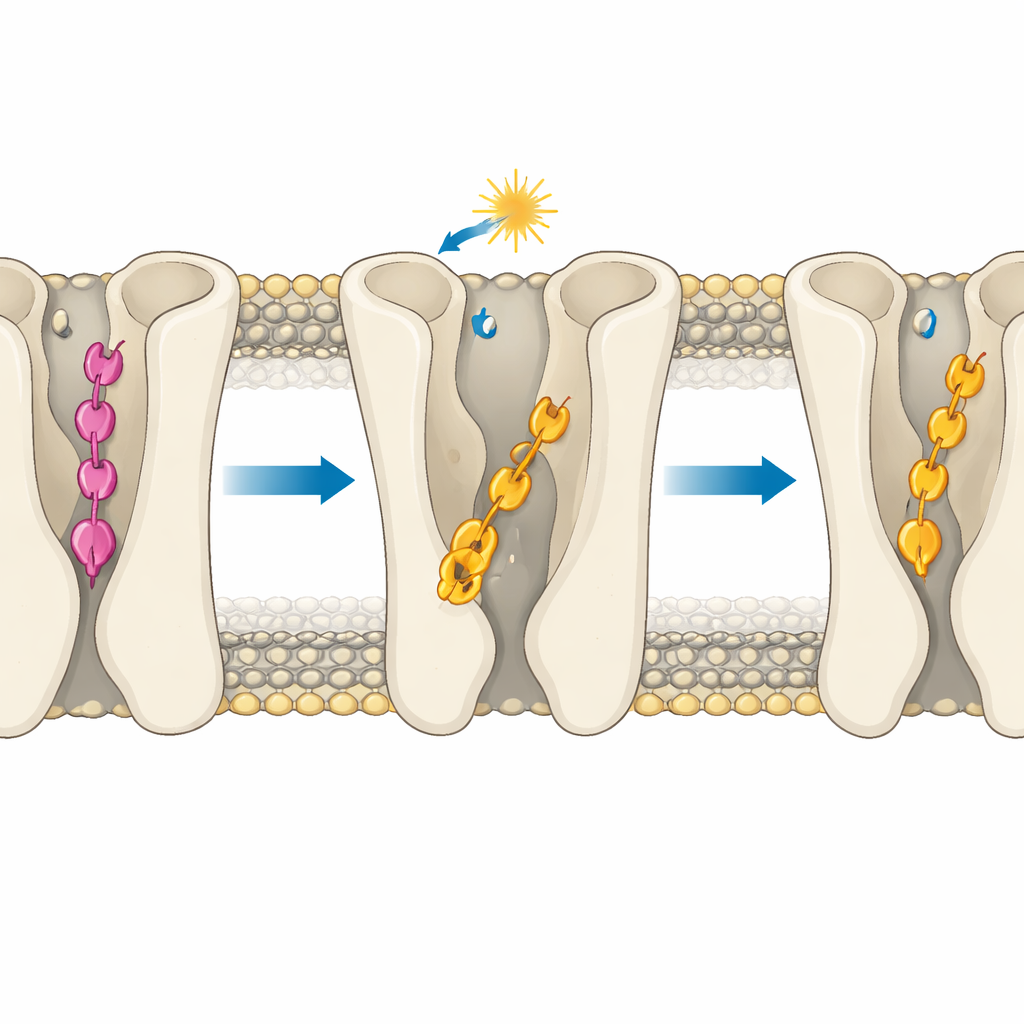
Regras de projeto para futuras drogas controladas por luz
Para um público não especializado, a mensagem é que a profundidade exata em que um fármaco se posiciona no bolso do receptor pode fazer a diferença entre desligado, parcialmente ligado e fortemente ligado — mesmo quando a mudança química parece mínima no papel. Ao mostrar como um ligante fotosswitch pode se sobre-inserir e travar o receptor desligado, enquanto outro estreitamente relacionado permanece em uma profundidade favorável à ativação, o estudo oferece uma regra clara de projeto: controle a profundidade de inserção com tanto cuidado quanto controla as mudanças de forma induzidas por luz. Esses insights podem guiar a criação de compostos sensíveis à luz de próxima geração que tratem distúrbios cerebrais com precisão sem precedentes, aumentando ou reduzindo vias de sinalização de maneira controlada e reversível, minimizando efeitos colaterais.
Citação: Weber, V., Salvadori, G., Natale, F. et al. Binding pose depth modulates photoswitchable ligands’ efficacy at the 5-HT2A receptor. Commun Chem 9, 121 (2026). https://doi.org/10.1038/s42004-026-01936-5
Palavras-chave: fotofarmacologia, receptor da serotonina 5-HT2A, ligantes fotosswitch, ativação de GPCR, simulações de dinâmica molecular