Clear Sky Science · pt
Comportamento scaffold-client e organização estrutural em condensados proteicos multicomponentes revelados pelo estudo de gotículas de tau/TDP-43
Proteínas que se comportam como minúsculas gotas de óleo
Dentro de nossas células, muitas proteínas não permanecem homogêneas no interior aquoso. Em vez disso, elas se agrupam em pequenas gotas líquidas, um pouco como óleo na água. Este estudo examina como duas dessas proteínas, tau e TDP-43, fortemente associadas à doença de Alzheimer e outras demências, se juntam em gotículas. Ao revelar como essas gotículas se formam, se misturam e se organizam, o trabalho oferece pistas sobre por que agregados proteicos nocivos surgem em cérebros envelhecidos e como poderíamos um dia controlá-los.
Por que essas duas proteínas cerebrais importam
Tau e TDP-43 são conhecidas por formar agregados tóxicos em doenças neurodegenerativas. Tradicionalmente, os cientistas estudavam cada uma isoladamente, mas autópsias de cérebros humanos mostram cada vez mais que ambas as proteínas podem acabar nas mesmas regiões danificadas. Isso levanta uma questão central: quando tau e TDP-43 estão presentes juntas nas células, como elas compartilham espaço dentro das gotículas, e esse ambiente compartilhado incentiva a agregação relacionada à doença? Os autores escolheram um modelo simplificado, porém realista, usando tau e a cauda de baixa complexidade do TDP-43 (LCD), que é a porção mais responsável pela formação das gotículas e pela eventual solidificação.
Gotas, “scaffolds” e “clients”
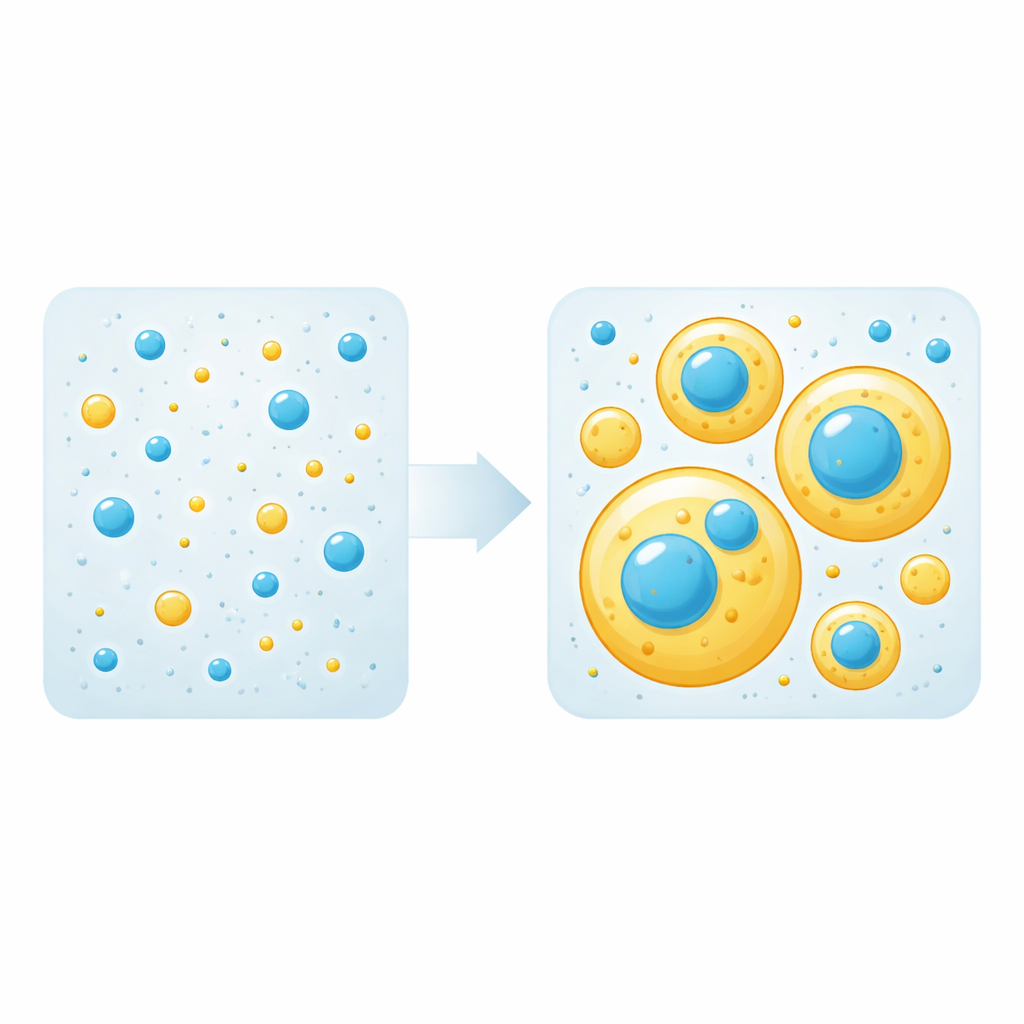
Gotas líquidas como essas se formam quando as atrações proteína–proteína superam as atrações proteína–água, fazendo a solução se dividir em uma fase densa (gotículas) e uma fase diluída. Em misturas, apenas algumas proteínas são necessárias para construir as gotículas; essas são chamadas de “scaffolds” (andaimes). Outras simplesmente pegam carona nas gotículas como “clients” (clientes). A equipe primeiro mediu o limiar de concentração no qual cada proteína isolada começa a formar gotículas. Em seguida, misturaram diferentes quantidades de tau e do LCD de TDP-43 e observaram, por microscopia de fluorescência, se as gotículas apareciam e como as proteínas se dispunham. De forma notável, descobriram que qualquer uma das proteínas pode atuar como scaffold ou client dependendo puramente de sua concentração: acima do seu próprio limiar ela constrói gotículas; abaixo desse limiar é recrutada passivamente para as gotículas formadas pela outra.
Gotas em camadas e um halo misterioso
Quando ambas as proteínas estavam em quantidade suficiente para formar gotículas por si só, elas não se misturavam numa gotícula única e uniforme. Em vez disso, gotículas maiores ricas em tau envolviam gotículas menores ricas em TDP-43, criando uma estrutura em múltiplas fases e em camadas. Medições de como as gotículas se espalham sobre vidro mostraram que as gotículas de TDP-43 têm tensão superficial maior, de modo que é energeticamente favorável que elas fiquem dentro das gotas mais molhantes de tau. Uma característica chamativa emergiu nessas interfaces: tau se acumulou em níveis especialmente altos como um brilhante “halo” revestindo a superfície das gotículas de TDP-43, mesmo quando o próprio tau estava abaixo do seu limiar de formação de gotículas. Com o tempo, as regiões ricas em TDP-43 tendiam a enrijecer em um material mais sólido, enquanto as regiões ricas em tau permaneciam líquidas, sugerindo diferentes propensões para se transformar em agregados duradouros.
Ajustando interações e sondando o mecanismo microscópico
Os autores testaram em seguida como forças moleculares específicas controlam qual proteína atua como scaffold ou client. Eles enfraqueceram seletivamente interações hidrofóbicas (repelentes à água) que impulsionam a condensação do LCD de TDP-43 usando 1,6-hexanodiol, e separadamente enfraqueceram as interações eletrostáticas (baseadas em cargas) que dirigem a condensação de tau elevando os níveis de sal. Em cada caso, desabilitar as interações-chave de uma proteína impediu que ela formasse gotículas e a tornou um client dentro das gotículas da outra, imitando o que acontece quando sua concentração é reduzida. Para entender melhor o halo, variaram o sal para ver quanto tau penetrava nas gotículas de TDP-43 e usaram simulações computacionais que tratam cada aminoácido como uma esfera simplificada. Essas simulações reproduziram o halo e mostraram que os primeiros ~40 aminoácidos da região N-terminal carregada negativamente de tau se ancoram na superfície da gotícula, enquanto o restante da molécula se estende para fora no líquido circundante, criando uma capa “anfifílica” (parte que gosta da gotícula, parte que gosta da água). Experimentos com um fragmento encurtado de tau sem esse trecho N-terminal confirmaram que, sem ele, o halo desaparece.

O que isso significa para doenças cerebrais
Em conjunto, os resultados revelam um conjunto geral de regras sobre como gotículas proteicas multicomponentes se montam e se organizam. Neste sistema tau/TDP-43, que espelha situações em neurônios doentes, concentração e força das interações determinam em conjunto quais proteínas constroem as gotículas e quais simplesmente as ocupam. Tensão superficial e arranjos anfifílicos então esculpem gotículas em camadas e halos que podem concentrar múltiplas proteínas associadas à doença no mesmo espaço confinado, potencialmente incentivando-as a endurecer em agregados. Para um leitor leigo, a mensagem-chave é que tau e TDP-43 não se aglomeram aleatoriamente; elas se autoorganizam em gotículas líquidas estruturadas cuja arquitetura é governada por princípios físicos simples. Entender e, eventualmente, manipular esses princípios pode abrir novas vias para retardar ou prevenir o acúmulo proteico nocivo em doenças neurodegenerativas.
Citação: Monnaka, V.U., Shipley, B., Boyko, S. et al. Scaffold-client behavior and structural organization in multicomponent protein condensates as revealed by studying tau/TDP-43 droplets. Commun Chem 9, 126 (2026). https://doi.org/10.1038/s42004-026-01933-8
Palavras-chave: condensados proteicos, separação de fase líquido-líquido, tau, TDP-43, neurodegeneração