Clear Sky Science · pt
Explorando a estabilidade de BOx em diversos suportes inorgânicos
Combustíveis mais limpos a partir de um elemento comum
Transformar o propano comum — o gás dos botijões de churrasco — em blocos de construção mais valiosos para plásticos normalmente exige processos quentes e consumidores de energia que também geram muito dióxido de carbono. Este estudo investiga como compostos de boro, um elemento relativamente abundante, podem ajudar a realizar essa transformação de forma mais branda e limpa. Ao revelar como o boro se comporta em diferentes superfícies sólidas em altas temperaturas, os autores apontam novas maneiras de projetar catalisadores que produzem produtos químicos úteis com menos desperdício e menor consumo de energia.
Por que a química de propano para plásticos importa
A vida moderna depende fortemente de olefinas leves como propeno e eteno, que são ingredientes-chave para plásticos, fibras e inúmeros materiais do dia a dia. Hoje, a maior parte desses compostos é produzida a partir de petróleo ou gás natural por rotas intensivas em energia que liberam grandes quantidades de CO₂. Um processo alternativo, chamado desidrogenação oxidativa do propano, pode em princípio gerar essas olefinas a temperaturas mais baixas e com menos subprodutos indesejados. Materiais à base de boro surgiram recentemente como catalisadores promissores para essa reação porque são altamente seletivos: favorecem a transformação do propano em olefinas em vez de oxidá-lo completamente até CO₂. Ainda assim, os pesquisadores não compreendem totalmente como são as espécies ativas de boro nem onde exatamente a reação ocorre — na superfície do catalisador, na fase gasosa ou em ambos.
Mobilidade surpreendente do boro em reatores quentes
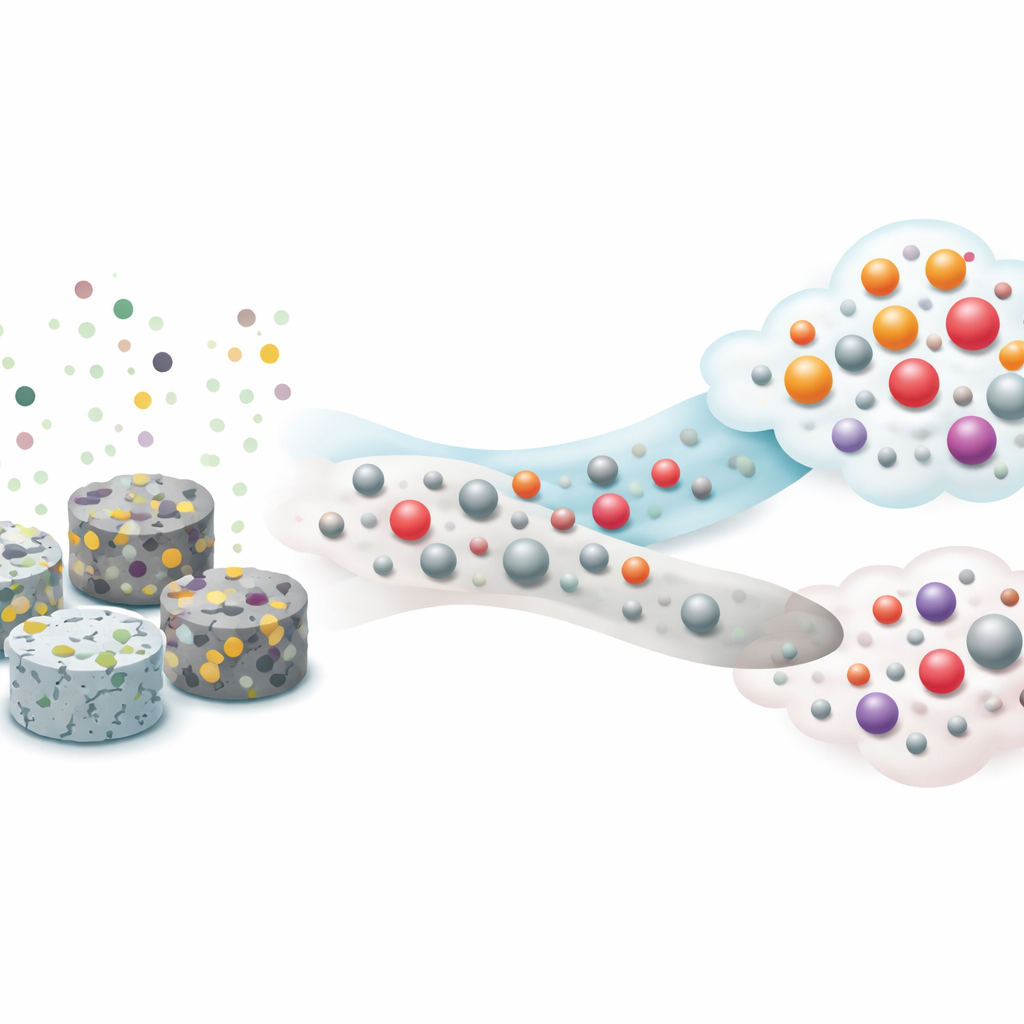
Os autores focaram no óxido de boro, um composto simples boro–oxigênio frequentemente representado como BOx, suportado em três materiais inorgânicos comuns: sílica pura, alumina pura e uma mistura sílica–alumina. Usando uma combinação de técnicas que monitoram gases liberados da superfície durante o aquecimento, assim como métodos que sondam a estrutura local dos átomos em sólidos, eles mostraram que o boro nem sempre permanece fixo. Na sílica, o óxido de boro tende a formar aglomerados fracamente ligados que podem evaporar, gerando espécies voláteis contendo boro no fluxo gasoso. Em suportes ricos em alumina, por outro lado, o boro se liga mais fortemente a átomos de oxigênio conectados ao alumínio, formando uma rede mais estável, tipo vidro, que resiste à lixiviação para a fase gasosa. Testes simples de lavagem reforçaram esse quadro: a maior parte do boro pôde ser enxaguada das amostras suportadas em sílica, mas muito menos saiu das amostras à base de alumina.
Ligando a estabilidade do boro ao comportamento catalítico
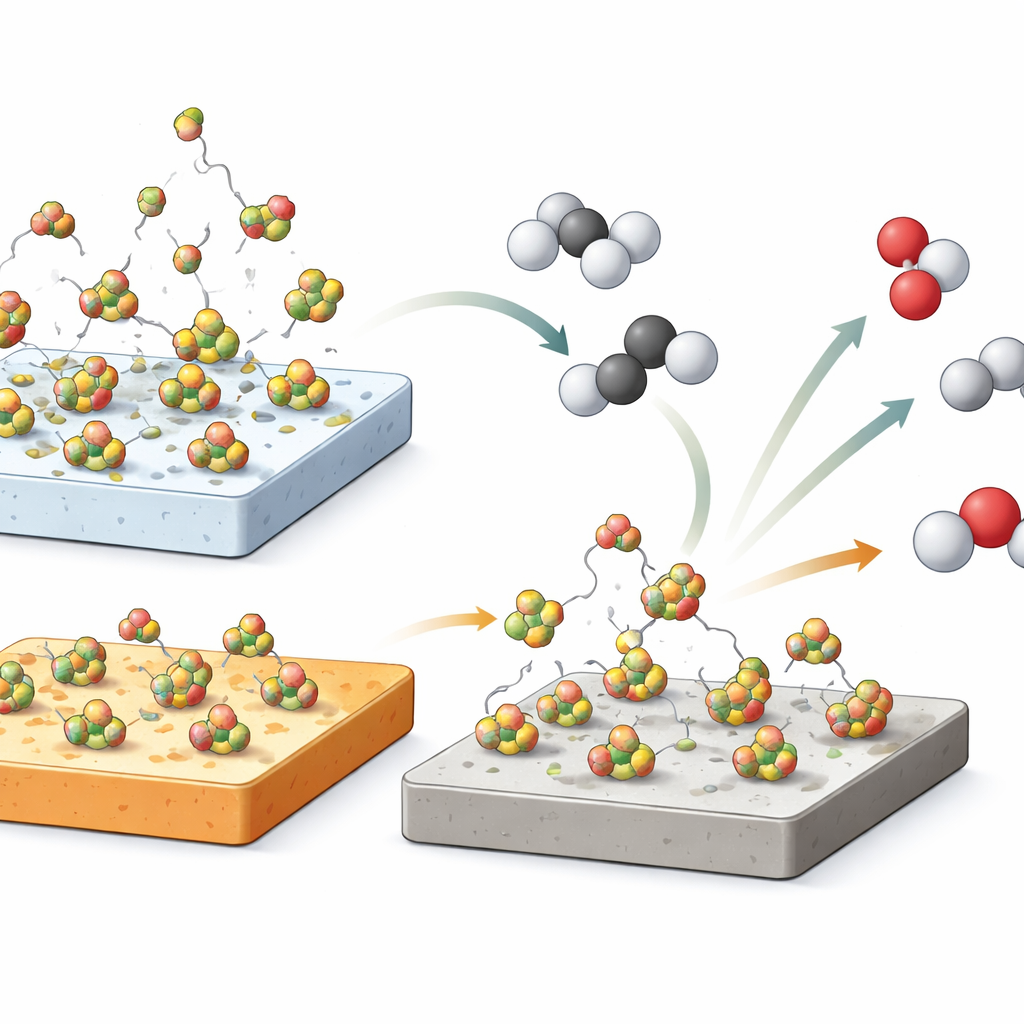
Essas diferenças na mobilidade do boro mostraram forte correlação com o comportamento dos catalisadores na reação do propano. O óxido de boro suportado em sílica começou a converter propano em olefinas a temperaturas cerca de 80 °C mais baixas do que os catalisadores contendo alumina, embora os três sistemas tenham apresentado, no fim, relações muito semelhantes entre a conversão de propano e a seletividade para olefinas. Aquecer as amostras enquanto se monitoravam fragmentos contendo boro na fase gasosa revelou que a sílica liberou muito mais óxido de boro e espécies relacionadas nas temperaturas de reação do que a alumina. Isso sugere que suportes que permitem que o boro escape com mais facilidade podem desencadear a reação mais cedo, porque intermediários reativos contendo boro entram na fase gasosa onde podem iniciar reações em cadeia que transformam o propano.
Boro em fase gasosa como um ajudante invisível
Para testar se o boro apenas na fase gasosa poderia conduzir a química, os pesquisadores realizaram um experimento marcante: removeram o catalisador sólido por completo e simplesmente injetaram um pequeno pulso de solução de ácido bórico, equivalente a cerca de um septuagésimo do boro normalmente presente em um catalisador, diretamente em um reator quente vazio. À medida que a solução se decompôs rapidamente em óxido de boro a 500 °C, a conversão do propano aumentou em cerca de 20%, com seletividade para olefinas semelhante à observada sobre os catalisadores sólidos. Um teste de controle com água pura produziu apenas um efeito pequeno e de curta duração. Junto às medições de dessorção, esse resultado indica fortemente que espécies voláteis de boro na fase gasosa desempenham um papel importante, provavelmente iniciando cadeias de radicais que convertem propano em propeno e eteno.
O que isso significa para catalisadores futuros
Para não especialistas, a principal conclusão é que o suporte sólido sob um catalisador à base de boro não é apenas um arcabouço inerte — ele controla ativamente quanto boro pode escapar para a fase gasosa e, com isso, com que facilidade a reação se inicia. Suportes como a sílica, que liberam boro mais prontamente, levam à ativação do propano a temperaturas mais baixas, enquanto suportes ricos em alumina retêm o boro com mais firmeza e requerem temperaturas mais altas, embora todos acabem por apresentar seletividades de produto semelhantes uma vez que a reação esteja em andamento. Essa visão sugere que ajustar cuidadosamente o grau de ancoragem do boro ao seu suporte pode permitir aos químicos projetar catalisadores que equilibrem estabilidade e atividade, possibilitando rotas mais limpas e energeticamente eficientes do propano e outros combustíveis simples para as moléculas que sustentam os materiais modernos.
Citação: Johánek, V., Wróbel, M., Knotková, K. et al. Exploring the stability of BOx at various inorganic supports. Commun Chem 9, 116 (2026). https://doi.org/10.1038/s42004-026-01926-7
Palavras-chave: catalisadores de óxido de boro, desidrogenação oxidativa do propano, química de radicais em fase gasosa, suportes de sílica e alumina, produção de olefinas