Clear Sky Science · pt
Cristalização desencadeada por difusão de massa em uma supersaturação local menor
Por que isso importa além do laboratório
Cristais de sal podem parecer banais, mas a forma como se formam tem consequências enormes — desde a fabricação de medicamentos até a recuperação de recursos a partir de águas residuais salinas. Este estudo revela que cristais podem começar a se formar mais cedo, e em locais diferentes, quando o líquido é sutilmente perturbado por gradientes de temperatura e concentração. Compreender esse comportamento sutil pode ajudar a projetar maneiras mais limpas e baratas de manejar salmouras, fabricar materiais melhores e controlar incrustações indesejadas em tubos e equipamentos.

Como os cristais geralmente surgem
A cristalização ocorre quando uma substância dissolvida, como cloreto de potássio (KCl) em água, ultrapassa a quantidade que pode permanecer dissolvida confortavelmente. Esse estado é chamado de supersaturação. As teorias clássicas dizem que cristais aparecem apenas quando a supersaturação é alta o suficiente para vencer uma barreira energética, e que a nucleação deve começar onde a solução está mais supersaturada. Na indústria, costuma-se levar soluções a esse estado resfriando-as, evaporando o solvente ou adicionando um "anti-solvente". Nestas condições convencionais e quase uniformes, os pesquisadores mapearam uma zona metastável — uma janela onde o líquido está supersaturado, mas ainda não se formaram cristais visíveis.
Três maneiras diferentes de fazer o mesmo sal cristalizar
Os autores examinaram como cristais de KCl aparecem em três cenários cuidadosamente controlados dentro de uma célula plana construída sob medida, com controle de temperatura independente no topo e na base. Primeiro, realizaram experimentos de resfriamento padrão, reduzindo a temperatura uniformemente a partir de 20 °C e observando quando os primeiros cristais surgiam. Isso estabeleceu uma fronteira de referência no mapa concentração–temperatura: abaixo de certa temperatura, cristais sempre se formavam; acima dela, a solução permanecia livre de cristais por horas. Em seguida, compararam esse referencial com dois cenários mais complexos nos quais a solução experimentava transporte direcional de massa em vez de simples resfriamento uniforme.
Quando o calor faz o sal se mover
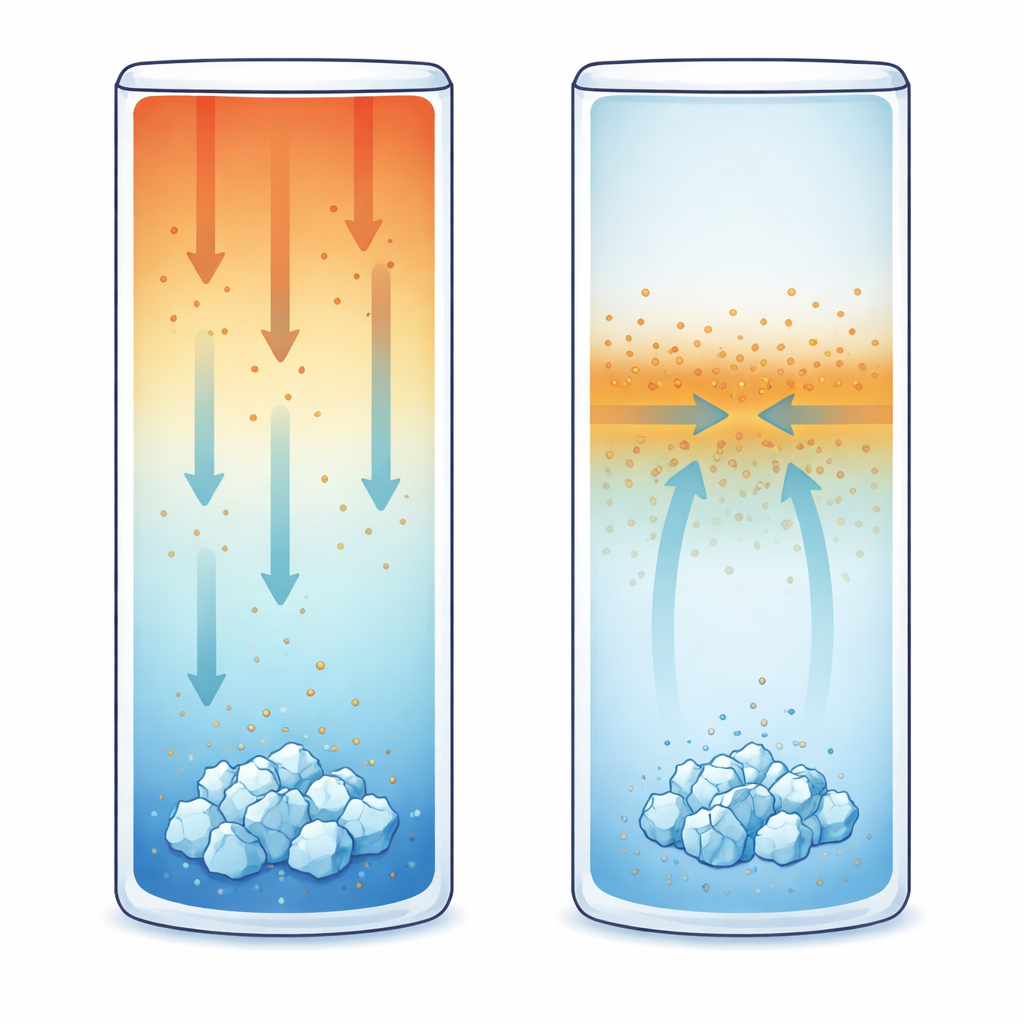
No segundo conjunto de experimentos, a solução começou com a mesma composição, mas manteve-se com o topo a 20 °C e a base resfriada a 15 °C. Esse gradiente vertical de temperatura causa termodifusão, o que significa que os íons dissolvidos migram em resposta à temperatura, não apenas à concentração. Para KCl na faixa testada, o comportamento é termofóbico: os íons tendem a se mover em direção à região mais fria, acumulando mais sal perto da base. Usando um método óptico sensível chamado interferometria por deslocamento de fase, os pesquisadores acompanharam pequenas mudanças no índice de refração que revelam como concentração e temperatura evoluem. Eles descobriram que os cristais se formavam consistentemente na parede fria inferior, em regiões onde o gradiente de concentração era mais acentuado — ainda que a supersaturação local ali fosse ligeiramente menor do que no caso de resfriamento uniforme. Em outras palavras, a presença de um fluxo de massa sustentado permitiu que a cristalização começasse mais cedo do que o esperado.
Quando o sal difunde em temperatura perfeitamente uniforme
O terceiro cenário eliminou diferenças de temperatura por completo. Toda a célula foi mantida a 17 °C uniforme, inicialmente preenchida com a solução de referência. Em seguida, um volume menor de solução de KCl mais diluída foi injetado suavemente a partir de um canto superior, criando um contraste acentuado de concentração mas quase nenhuma agitação do fluido. A difusão então suavizou esse contraste à medida que os íons migravam da região mais concentrada para a mais diluída. Novamente, a interferometria revelou como o campo de concentração evoluía ao longo do tempo. Surpreendentemente, os primeiros cristais visíveis não apareceram onde a solução estava mais supersaturada. Em vez disso, formaram-se aproximadamente na metade superior da célula, perto da interface onde o gradiente de concentração — e portanto o fluxo difusivo de massa — era mais forte.
O que isso significa para teoria e tecnologia
Em todos os três métodos — resfriamento, termodifusão e difusão isotérmica — os primeiros cristais a aparecer eram muito semelhantes: principalmente cristais cúbicos de KCl com formas de crescimento familiares. O que mudou não foi a estrutura cristalina, mas as condições que desencadearam seu nascimento. Sob fluxos de massa impostos, cristais emergiram em supersaturação local menor e em locais governados por gradientes, em vez de picos de concentração. Isso sugere que o tráfego molecular direcional no líquido pode ajudar os íons a se alinhar em manchas densas que atuam como núcleos iniciais, estreitando efetivamente a zona metastável. Embora a teoria clássica da nucleação não consiga explicar totalmente esse comportamento, ideias mais recentes de nucleação em múltiplas etapas são compatíveis com os achados. Na prática, o trabalho aponta para um controle mais inteligente da cristalização em processos como dessalinização sem rejeito líquido, onde aproveitar a termodifusão poderia ajudar a transformar salmouras residuais em sais sólidos usando menos energia e menos químicos.
Citação: Xu, S., Torres, J.F. Crystallisation triggered by mass diffusion at a lower local supersaturation. Commun Chem 9, 125 (2026). https://doi.org/10.1038/s42004-026-01925-8
Palavras-chave: cristalização, termodifusão, supersaturação, dessalinização, transporte de massa