Clear Sky Science · pt
Efeitos sinérgicos de cátions e faces aumentam a cinética da evolução de hidrogênio em meio alcalino em superfícies de Pt com degraus
Por que isso importa para a energia limpa
Produzir hidrogênio limpo a partir da água é uma peça-chave de muitos planos de energia com emissões líquidas zero, mas os dispositivos mais práticos hoje ainda desperdiçam energia porque a reação que gera bolhas de hidrogênio pode ser surpreendentemente lenta em soluções alcalinas (básicas). Este estudo investiga até o nível de átomos individuais e moléculas de água para explicar por que algumas superfícies de platina funcionam melhor do que outras e como íons dissolvidos comuns no líquido podem cooperar com a superfície metálica para acelerar a produção de hidrogênio.
Moldando superfícies metálicas para orientar a água
Os pesquisadores concentram-se na platina, o material de referência para dividir a água, e comparam dois tipos de paisagens atômicas em sua superfície. Uma é plana, como um terraço liso (chamada Pt(111)); a outra é com degraus, como uma pequena escada (Pt(311)). Usando simulações quântico‑mecânicas avançadas que incluem tanto elétrons quanto moléculas de água em movimento, eles modelam como essas diferentes superfícies se comportam sob tensões operacionais realistas em um eletrólito alcalino. O objetivo é ver como o ambiente local bem ao lado do metal — onde água, íons e elétrons se encontram — controla a velocidade do primeiro passo na formação do hidrogênio.
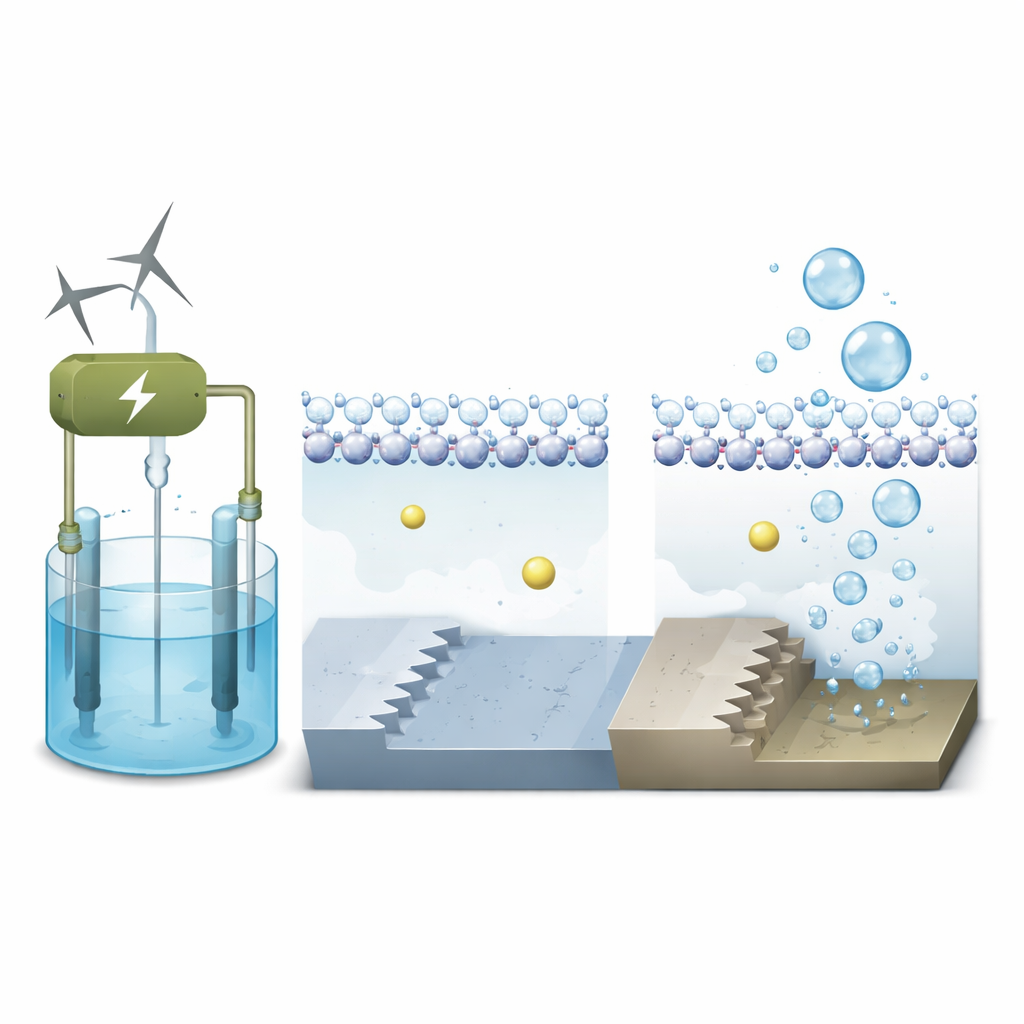
Íons de sal como ajudantes ocultos
Em eletrólitos alcalinos, o líquido contém íons de metais alcalinos como sódio. Esses íons positivamente carregados fazem mais do que simplesmente flutuar; eles podem se agrupar perto do eletrodo e remodelar sutilmente o campo elétrico na interface. As simulações mostram que, na superfície plana de platina, a água forma uma camada compacta e ordenada com átomos de hidrogênio apontando para baixo, em direção à superfície carregada negativamente. Os íons de sódio ficam mais afastados, separados do metal por essa película de água, de modo que sua influência na reação é modesta. Na superfície com degraus, porém, os átomos com subcoordenção na aresta do degrau ligam a água mais fortemente e criam uma estrutura de água local mais rugosa e desordenada.
Um aglomerado especial perto da superfície que puxa íons para mais perto
Nessas arestas de degrau, a equipe descobre um motivo estrutural recorrente: uma molécula de água ligada diretamente ao degrau de platina que, por sua vez, segura um íon de sódio próximo cercado por moléculas de água adicionais. Esse aglomerado compacto platina–água–sódio efetivamente arrasta o íon cerca de 2,3 angstroms mais perto do metal do que na superfície plana. Estar mais próximo fortalece muito o campo elétrico local nessa pequena região, o que polariza fortemente as moléculas de água vizinhas. As simulações revelam que uma ligação O–H nessas moléculas se alonga mais do que o habitual, indicando que ela está parcialmente prestes a se romper mesmo antes da progressão formal da reação.
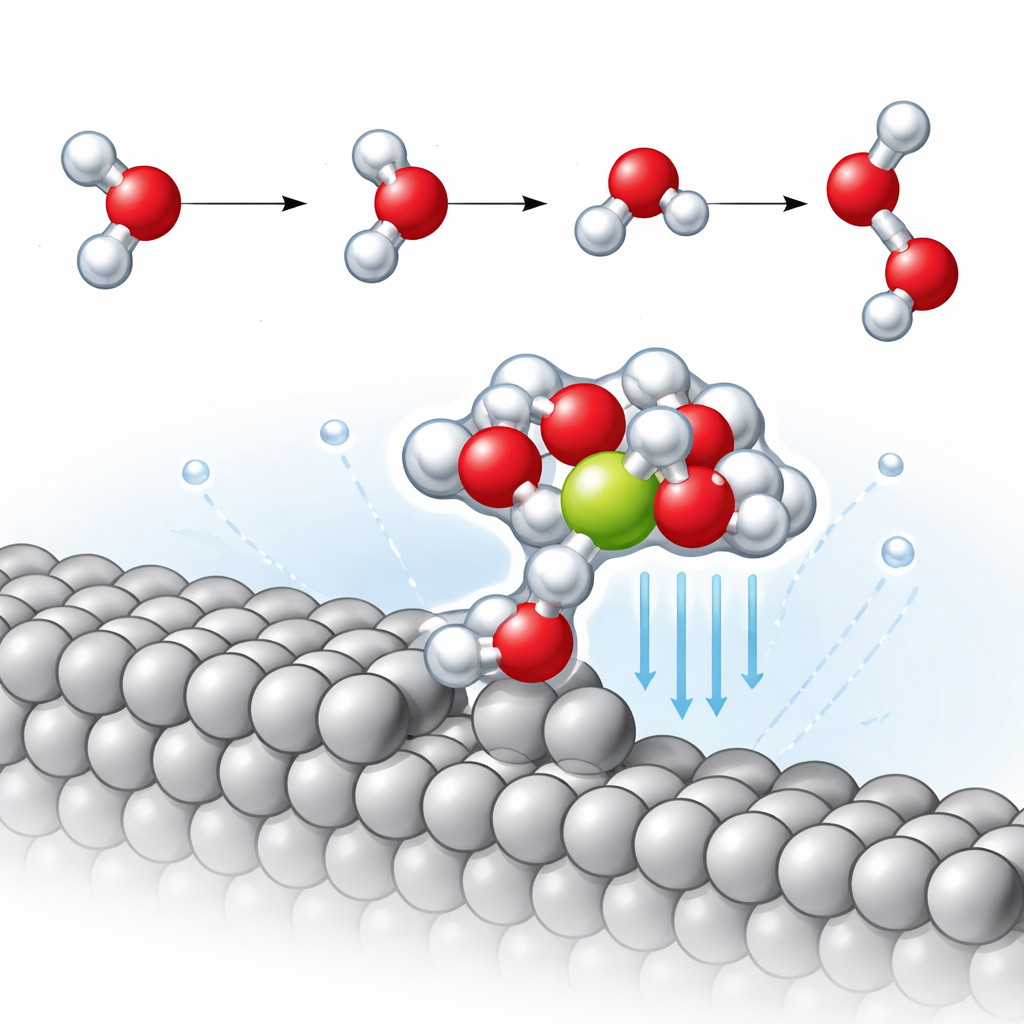
Reduzindo a barreira para produzir hidrogênio
O passo lento chave na evolução alcalina do hidrogênio é conhecido como passo de Volmer, onde uma molécula de água se divide: o hidrogênio se liga ao metal enquanto o hidróxido restante migra para o líquido. Ao traçar o caminho reacional de energia mínima, os autores constataram que, na superfície plana de platina, o sódio tem apenas um efeito pequeno na barreira energética desse passo. Em contraste, na superfície com degraus, o aglomerado estabilizado pelo sódio reduz a energia de ativação em cerca de 0,14 elétron‑volt — aproximadamente três vezes a melhoria observada na face plana. Análises detalhadas dos modos vibracionais mostram que a ligação O–H apontada para a superfície torna‑se significativamente mais fraca na presença do íon próximo, facilitando sua ruptura e, portanto, acelerando a formação de hidrogênio.
Uma regra de projeto para catalisadores de hidrogênio melhores
No geral, o estudo conclui que o melhor desempenho na produção alcalina de hidrogênio não vem apenas da superfície metálica ou do eletrólito isoladamente, mas de sua sinergia. Sítios de platina com degraus que podem ancorar aglomerados especiais água–íon puxam cátions alcalinos para perto, intensificam o campo elétrico local, pré‑rompem parcialmente ligações de água e aceleram fortemente o passo inicial crucial da evolução do hidrogênio. Para um leitor leigo, a conclusão é que, ao esculpir cuidadosamente a forma microscópica das superfícies dos catalisadores e escolher eletrólitos que levem os íons certos aos locais certos, os engenheiros podem superar algumas das limitações fundamentais dos dispositivos alcalinos e projetar sistemas mais eficientes e economizadores de energia para a produção de hidrogênio limpo.
Citação: Zhang, Q., Sun, P., Li, H. et al. Synergistic cation-facet effects boost alkaline hydrogen evolution kinetics on stepped Pt surfaces. Commun Chem 9, 113 (2026). https://doi.org/10.1038/s42004-026-01924-9
Palavras-chave: evolução do hidrogênio, eletrólise alcalina, catalisador de platina, água interfacial, cátions de metais alcalinos