Clear Sky Science · pt
Base estrutural para a formação do filamento humano RegⅢα
Como nosso intestino combate germes
Nosso intestino está constantemente exposto a bilhões de bactérias, muitas das quais são inofensivas ou até benéficas. Mas quando micróbios perigosos aparecem, o corpo precisa de formas rápidas e precisas de atacá-los sem danificar seus próprios tecidos. Este estudo examina de perto uma dessas proteínas de defesa natural, chamada RegIIIα, e revela como ela muda de forma para matar bactérias e depois se transforma em uma forma mais segura e menos agressiva. Entender esse ato de mudança conformacional pode ajudar os cientistas a compreender melhor como mantemos o equilíbrio dos microrganismos intestinais e o que dá errado em doenças.
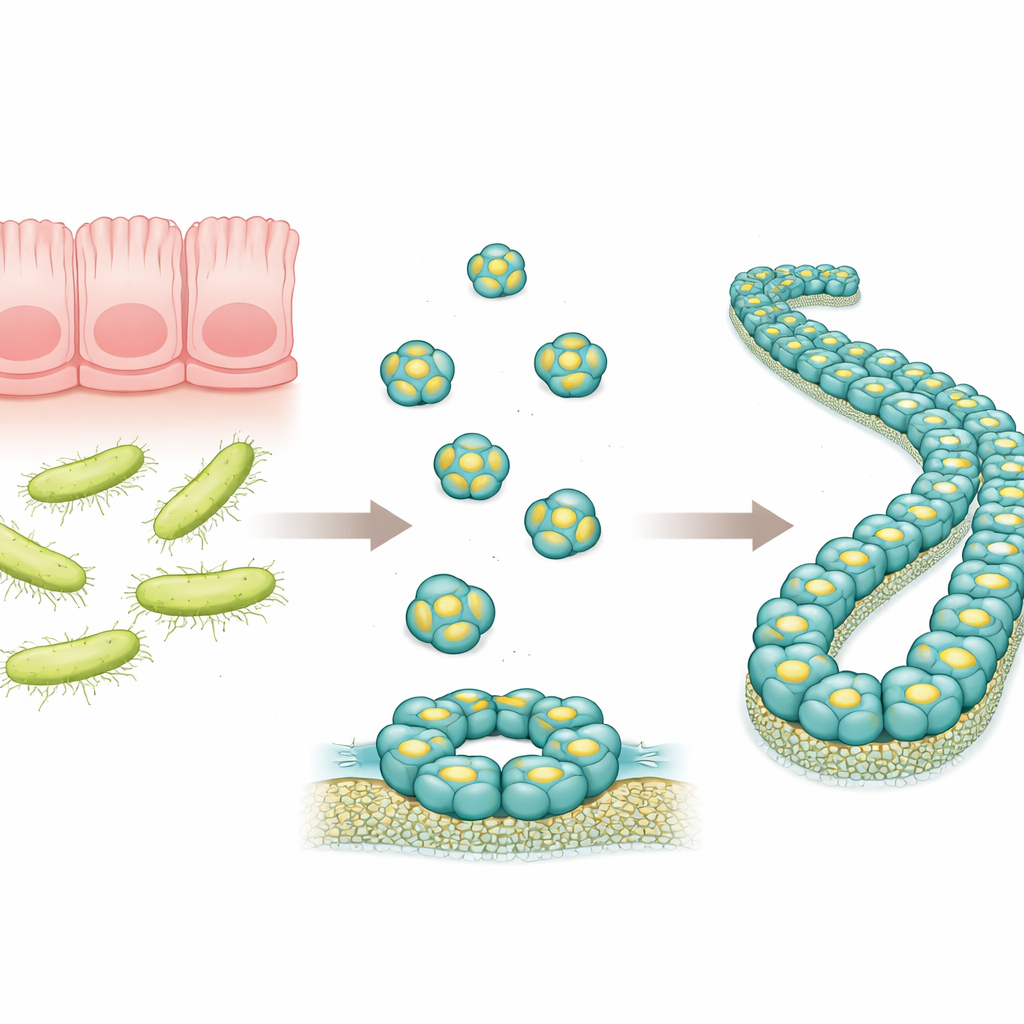
Um pequeno defensor no intestino
RegIIIα é uma proteína produzida no trato digestivo que mira certas bactérias, especialmente aquelas com paredes externas espessas conhecidas como bactérias Gram-positivas. Trabalhos anteriores sugeriram que RegIIIα pode perfurar membranas bacterianas formando estruturas em anel, permitindo que o conteúdo do micro-organismo vaze e levando-o à morte. Pesquisadores também observaram que, com o tempo, essas estruturas em anel podem empilhar-se em longos filamentos, o que parece reduzir o poder letal da proteína. Entretanto, o arranjo exato das moléculas de RegIIIα nessas montagens maiores não era conhecido em detalhe, dificultando a compreensão de como a proteína funciona e como sua atividade é controlada.
Vendo o filamento em detalhe atômico
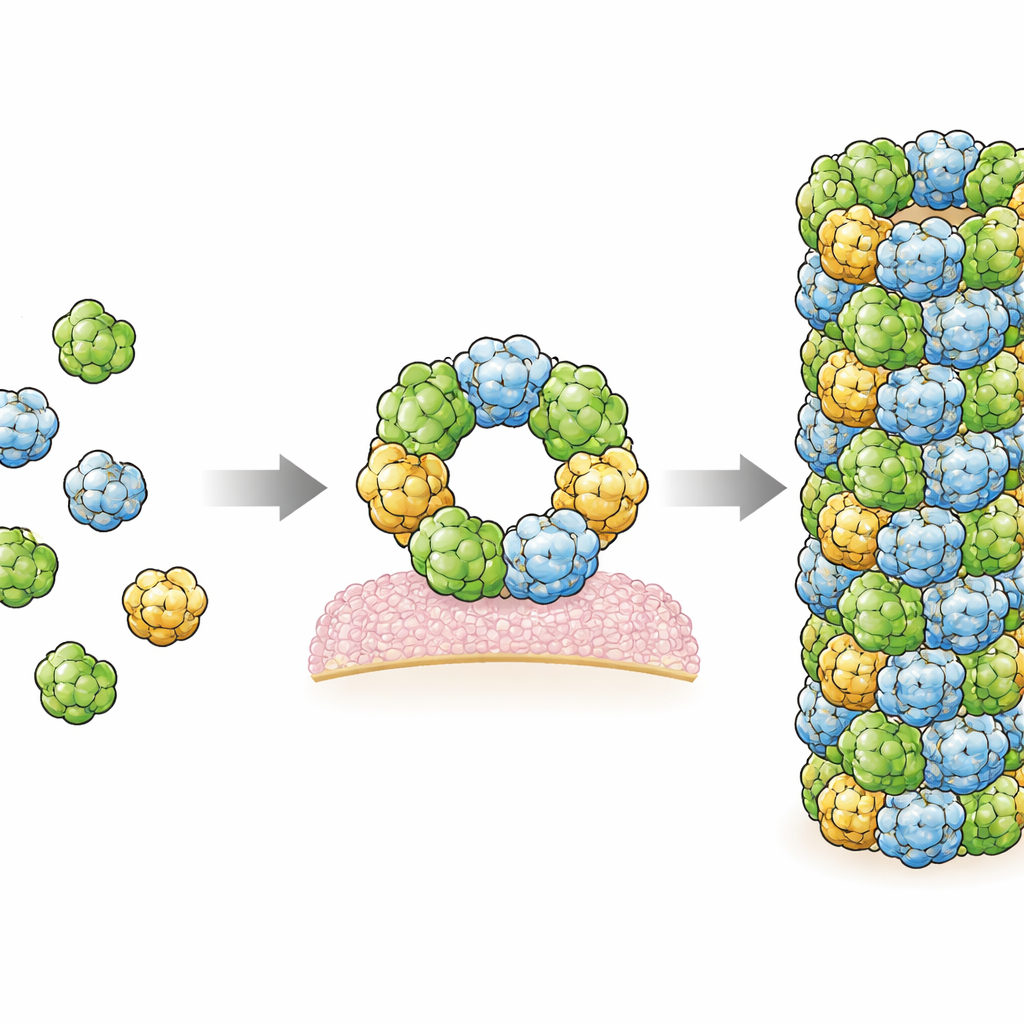
Neste estudo, os autores produziram RegIIIα humano em bactérias e então o induziram a se montar em filamentos sob condições controladas. Eles usaram um método de imagem poderoso chamado crio-microscopia eletrônica, que pode visualizar moléculas biológicas congeladas em uma fina camada de gelo em resolução quase atômica. Eles descobriram que os filamentos são construídos a partir de conjuntos repetidos de três unidades idênticas de RegIIIα, chamadas trimers, que se empilham em um padrão helicoidal regular. Cada molécula individual de RegIIIα se parece muito com o que já havia sido visto em estruturas cristalográficas, mas sua orientação dentro do filamento difere de um modelo anterior de menor resolução. Essa orientação corrigida altera como os cientistas pensam que a proteína interage com membranas bacterianas e com seu próprio segmento regulatório.
Como as proteínas se conectam e por que os lipídios importam
Ao examinar a estrutura de perto, os pesquisadores identificaram duas regiões principais de contato, ou interfaces, onde moléculas vizinhas de RegIIIα se tocam e mantêm o filamento unido. Eles então alteraram aminoácidos específicos nessas interfaces e mostraram que essas mudanças impediam a formação do filamento, confirmando que esses pontos de contato são essenciais. Curiosamente, em ambas as interfaces, os mapas de crio-EM mostraram regiões adicionais difusas que provavelmente representam pequenas moléculas alongadas encaixadas entre superfícies proteicas. Sua forma e ambiente químico sugerem que podem ser lipídios, os mesmos tipos de moléculas oleosas que formam membranas celulares. Isso corrobora indícios anteriores de que lipídios ajudam a promover a montagem de RegIIIα, possivelmente atuando como uma espécie de cola molecular que estabiliza as conexões entre as subunidades.
O interruptor liga–desliga: pH e um segmento oculto
A equipe também investigou o que controla quando RegIIIα pode se montar. Antes de se tornar ativa, a proteína carrega um curto “pró-segmento” que deve ser removido por enzimas digestivas. Em sua estrutura de filamento em alta resolução, não há espaço no centro da montagem para acomodar essa peça extra, o que implica que o pró-segmento bloqueia a capacidade de RegIIIα de formar os anéis formadores de poros e os filamentos desde o início. Eles descobriram que a tendência a formar filamentos também depende da acidez: filamentos se formam facilmente em um pH semelhante ao do intestino delgado, mas pouco em um pH mais ácido. Um único aminoácido, histidina 50, parece atuar como um interruptor sensível ao pH; quando é alterado para outro resíduo, a formação de filamentos torna-se muito menos sensível ao pH. Juntas, essas características — clivagem enzimática, ligação a lipídios e pH — criam um sistema de controle em camadas que ajusta quando e onde RegIIIα está ativo.
O que isso significa para a saúde intestinal
No conjunto, este trabalho fornece a imagem mais detalhada até agora de como moléculas de RegIIIα se montam em estruturas maiores que se relacionam tanto à sua ação antibacteriana quanto ao seu comportamento de auto-limitação. As mesmas interfaces que constroem os filamentos também formam os anéis hexaméricos considerados responsáveis por abrir poros nas membranas bacterianas, sugerindo um equilíbrio delicado entre uma forma potente de matar e um estado mais seguro e atenuado. Mapear mutações associadas a doenças nessa estrutura mostra que muitas delas se localizam em pontos de contato chave, sugerindo que perturbações na montagem podem estar na base de certos distúrbios intestinais ou pancreáticos. Ao esclarecer como esse antibiótico natural é ativado, guiado por lipídios e moldado pelo pH local, o estudo prepara o terreno para esforços futuros de modular nossas defesas inatas — seja reforçando-as contra infecções, seja acalmando-as quando ficam desreguladas.
Citação: Han, J., Cao, Q. Structural basis for human RegⅢα filament formation. Commun Chem 9, 117 (2026). https://doi.org/10.1038/s42004-026-01921-y
Palavras-chave: RegIIIα, imunidade intestinal, crio-microscopia eletrônica, filamentos proteicos, peptídeos antibacterianos