Clear Sky Science · pt
Glicosídeos janus anfifílicos ionizáveis com ponte de azobenzeno para entrega de pDNA controlada por luz, unicomponencial e modulável por órgão
Iluminando uma Entrega Gênica Mais Inteligente
Terapias gênicas prometem tratar doenças em sua raiz ao entregar trechos de código genético diretamente às nossas células. Mas conduzir essa carga frágil com segurança pela corrente sanguínea, para os órgãos certos e para dentro das células-alvo continua sendo um grande desafio. Este trabalho apresenta uma nova classe de partículas minúsculas à base de açúcar cuja atuação pode ser comutada com luz antes mesmo de entrarem no corpo, permitindo que os pesquisadores redirecionem onde um gene terapêutico termina e quão fortemente ele é expresso, tudo isso mantendo as células amplamente ilesas. 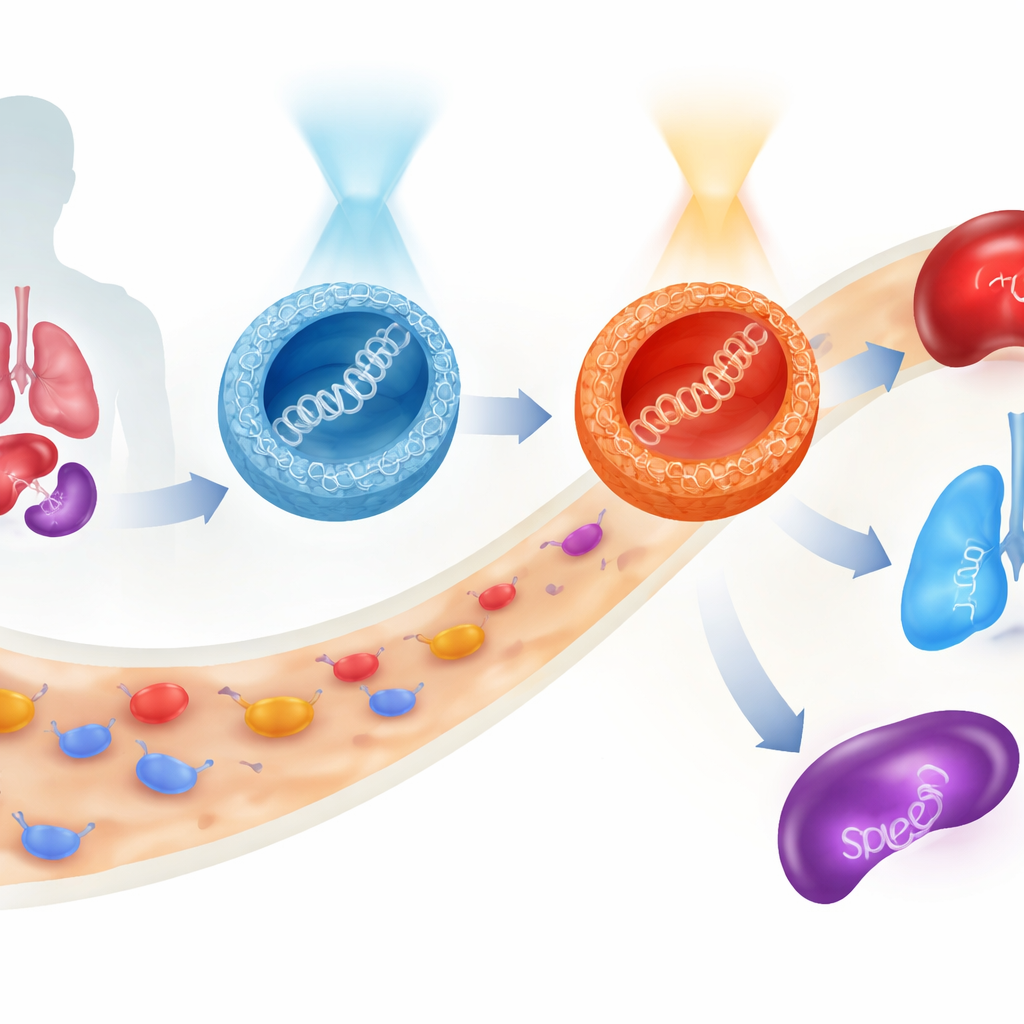
Uma Necessidade por Courieres Genéticos Precisos
Os veículos de entrega gênica mais bem-sucedidos hoje são nanopartículas lipídicas, que ajudaram a viabilizar as vacinas de mRNA contra a COVID-19. Essas gotículas multicomponentes envolvem e protegem os ácidos nucleicos, mas tendem a se acumular principalmente no fígado e liberam apenas uma pequena fração de sua carga dentro das células. Ajustar suas composições pode alterar quais órgãos elas preferem, porém as misturas são complexas e difíceis de controlar com precisão. A equipe por trás deste trabalho optou em vez disso por projetar moléculas únicas e bem definidas que se auto-organizam em nanopartículas com formas e comportamentos previsíveis — e que podem ser sintonizadas ativamente de fora por um gatilho simples de luz.
Uma Gangorra Molecular Controlada por Luz
No cerne do novo sistema estão glicosídeos “Janus” duplos: moléculas formadas por duas unidades de glicose, equipadas com cabeças carregadas hidrofílicas e caudas lipofílicas, ligadas por uma “dobradiça” central de azobenzeno. O azobenzeno pode alternar entre duas formas espelhadas, chamadas E e Z, quando exposto a diferentes cores de luz. Em água na presença de DNA, muitas cópias dessas moléculas se reúnem espontaneamente em partículas macias e em camadas que envolvem filamentos de DNA plasmidial. Os pesquisadores prepararam duas versões — uma com pontes de oxigênio e outra com pontes de enxofre entre o açúcar e a dobradiça — para ajustar sutilmente a estabilidade e o comportamento biológico. Ao pré-irradiar as soluções, puderam enriquecer seja a forma E, seja a Z e estudar como cada estado molda as partículas resultantes de entrega gênica.
Como se Comportam Partículas que Mudam de Forma
Medições de tamanho das partículas, carga de superfície e estrutura interna mostraram que a comutação induzida pela luz entre os estados E e Z tem consequências físicas claras. De modo geral, a forma Z produziu nanopartículas menores, de formato mais uniforme e com um interior mais ordenado e em camadas do que a forma E. Microscopia revelou que esses arranjos internos se assemelham a folhas alternadas de material lipídico e DNA. Importante: ambos os estados protegeram o DNA da degradação enzimática. Em células cultivadas de rins, fígado e tecido imunológico, os diferentes isômeros produziram níveis marcadamente distintos de expressão gênica, embora o DNA subjacente fosse idêntico. Pulsos de luz repetidos aplicados após a entrada das partículas nas células aumentaram a expressão gênica várias vezes, sugerindo que o impacto mecânico da comutação ajuda as partículas a afrouxar e liberar sua carga, e pode também favorecer sua fuga de compartimentos intracelulares. 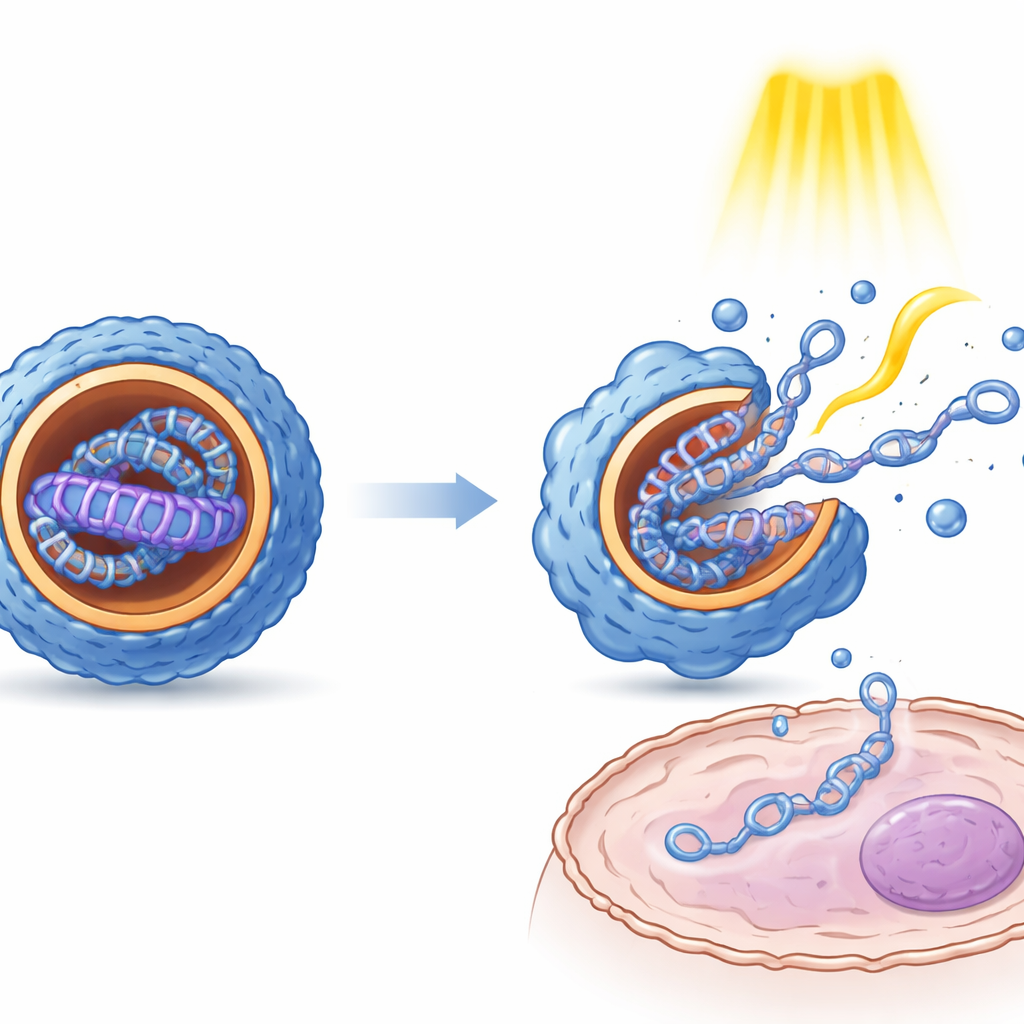
Guiando Genes para Órgãos Específicos
O comportamento mais surpreendente apareceu em camundongos. Quando as partículas com ponte de oxigênio foram administradas em sua forma rica em E, a expressão de um gene marcador ocorreu principalmente no fígado e com alguma ocorrência nos pulmões. Pré-alterná‑las para a forma Z antes da injeção não apenas aumentou a expressão total, mas também deslocou o equilíbrio em direção aos pulmões. As partículas com ponte de enxofre contaram outra história: sua forma Z favoreceu o baço, um órgão imunológico chave. Assim, com a mesma estrutura molecular básica — e sem alterar a carga de DNA — os pesquisadores puderam direcionar a atividade gênica predominantemente para fígado, pulmão ou baço simplesmente escolhendo a ligação (oxigênio ou enxofre) e a forma ativada pela luz (E ou Z) do transportador. Ao longo desses testes, a viabilidade celular permaneceu alta, sugerindo que o sistema é relativamente gentil.
Uma Rota Ajustável por Luz para Futuros Medicamentos Gênicos
Em termos práticos, a equipe construiu um minúsculo transporte de DNA com chave de luz. Antes da injeção, um breve tratamento luminoso “programa” os transportes em uma de duas formas. Cada forma se monta em nanopartículas com tamanho e sensação de superfície característicos, que por sua vez determinam com que afinco elas aderem a diferentes tipos celulares e onde acabam no organismo. Porque o mesmo arcabouço químico pode ser modificado de muitas pequenas maneiras, e porque a comutação é reversível e não altera o próprio DNA, essa plataforma oferece uma maneira flexível de ajustar onde e como terapias gênicas atuam. Embora muito trabalho ainda seja necessário antes do uso clínico, o estudo mostra que vetores moleculares únicos cuidadosamente desenhados e controlados por luz podem se tornar ferramentas poderosas para medicamentos genéticos mais seguros e precisos.
Citação: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
Palavras-chave: entrega gênica, nanopartículas responsivas à luz, chaves de azobenzeno, terapia de DNA direcionada, nanomedicina