Clear Sky Science · pt
A protease S9 WprP2 catalisa clivagem uniforme do peptídeo precursor na biossíntese de RiPPs
Por que pequenas ferramentas de corte nas células importam
No interior de bactérias, tesouras moleculares especializadas cortam longas cadeias de aminoácidos em fragmentos menores e ativos que frequentemente se tornam antibióticos ou outros produtos naturais úteis. Este estudo revela uma ferramenta de corte até então desconhecida — uma protease chamada WprP2 — que aparada seu peptídeo-alvo com precisão incomum. Compreender como essa enzima funciona pode ajudar cientistas a projetar novos peptídeos bioativos e uma nova geração de antibióticos.
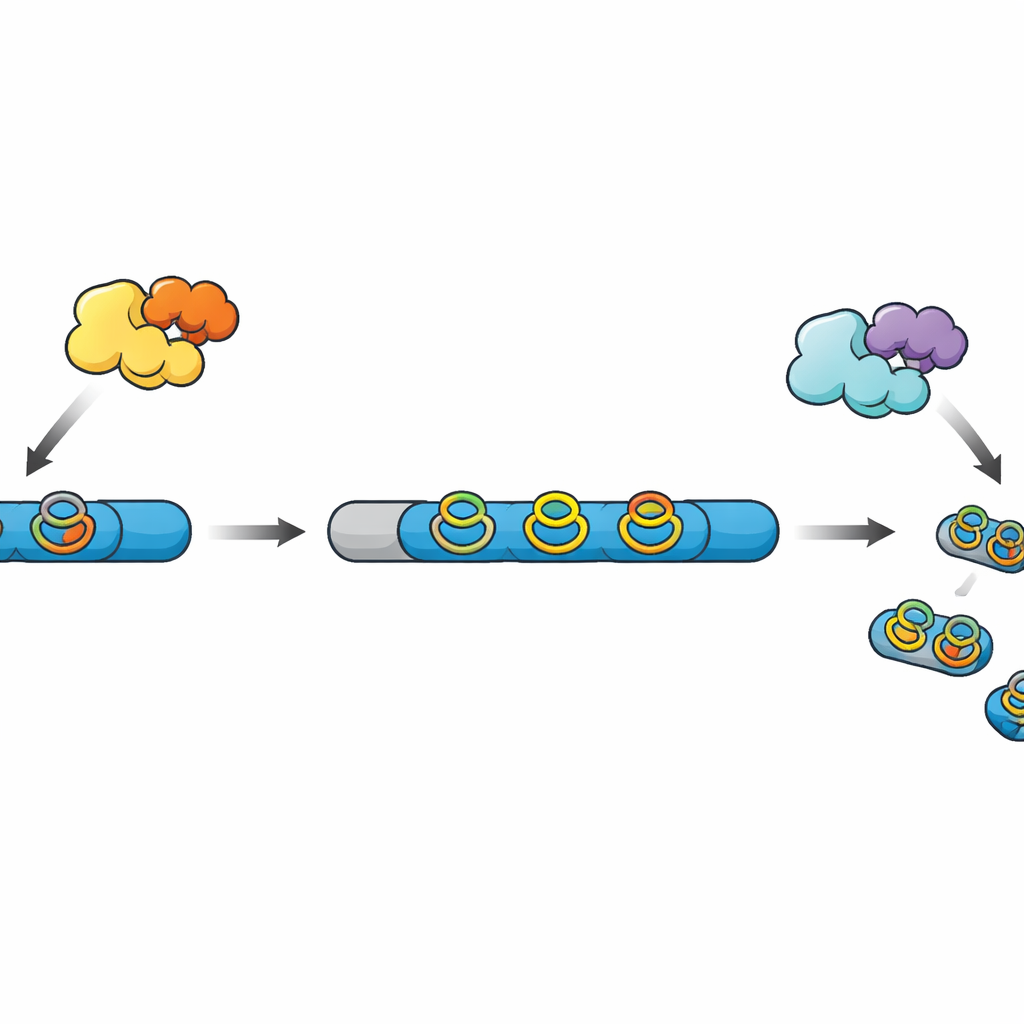
Das cadeias brutas aos mini-remédios prontos
Muitos produtos naturais modernos à base de peptídeos, conhecidos coletivamente como RiPPs, começam como cadeias simples sintetizadas no ribossomo. Essas cadeias contêm uma região líder que atua como uma alça e uma região central que se tornará o produto final após uma série de modificações químicas. Outras enzimas adicionam ligações cruzadas e anéis que tornam o peptídeo mais estável e mais ativo, e por fim uma protease corta a região líder, liberando a molécula madura. Em uma família recentemente descoberta de RiPPs, enzimas radical SAM constroem anéis compactos “ciclofanos” envolvendo aminoácidos aromáticos, mas na maioria dos clusters genéticos conhecidos a protease correspondente está ausente, deixando obscuros os passos finais do processamento.
Rastreando uma enzima parceira ausente
Os autores estudaram anteriormente uma enzima radical SAM chamada WprB1 que instalava ligações idênticas em três segmentos repetidos WPR de um peptídeo precursor. No novo trabalho, eles buscaram em genomas bacterianos parentes dessa enzima e procuraram próximos genes que pudessem codificar uma protease. Em Streptomyces venezuelae encontraram um cluster promissor que continha uma enzima de entrecruzamento semelhante, sua proteína auxiliar, um peptídeo precursor correspondente com três repetições WPR e uma candidata a protease de serina da família S9, que nomearam WprP2. Isso tornou o sistema um campo de testes ideal para descobrir como o peptídeo é finalmente cortado para liberar os fragmentos ativos.
Observando o peptídeo sendo fatiado
Para investigar a WprP2, a equipe produziu o peptídeo precursor em bactérias, tanto com quanto sem a enzima de entrecruzamento, purificou-o e então o misturou com a protease em reações in vitro controladas. Espectrometria de massa revelou que a WprP2 primeiro corta a cadeia imediatamente após cada segmento WPR e depois realiza um segundo corte a uma distância fixa antes de uma determinada prolina mais adiante na sequência. Esses dois passos geram uma série de fragmentos menores e uniformes. Notavelmente, a WprP2 executou esse padrão de cortes independentemente de a enzima de entrecruzamento já ter instalado os anéis ciclofanos, mostrando que os anéis não são necessários para o reconhecimento. Em comparação com tripsina comercial, que não consegue cortar em certos sítios entrecruzados, a WprP2 ainda funcionou, ressaltando sua robustez incomum.
Decodificando o que a enzima reconhece
Os pesquisadores então investigaram quais características do peptídeo a WprP2 realmente lê. Ao alterar sistematicamente aminoácidos individuais ao redor dos sítios de corte, descobriram que modificar muitos resíduos próximos teve pouco efeito, mas alterar uma arginina chave dentro do segmento WPR ou a glutamina ou prolina no segundo sítio de clivagem podia bloquear aquele passo específico. Experimentos com um peptídeo precursor relacionado carregando resíduos de flanco diferentes mostraram que a protease ainda cortava após repetições WPR, mas só realizava o segundo corte quando um par glutamina‑prolina estava presente. Modelos estruturais gerados por computador usando AlphaFold3 apoiaram esse quadro: nos complexos previstos, os sítios baseados em WPR e em glutamina‑prolina alinham-se por sua vez com o centro catalítico da enzima, consistente com um mecanismo sequencial em dois passos.
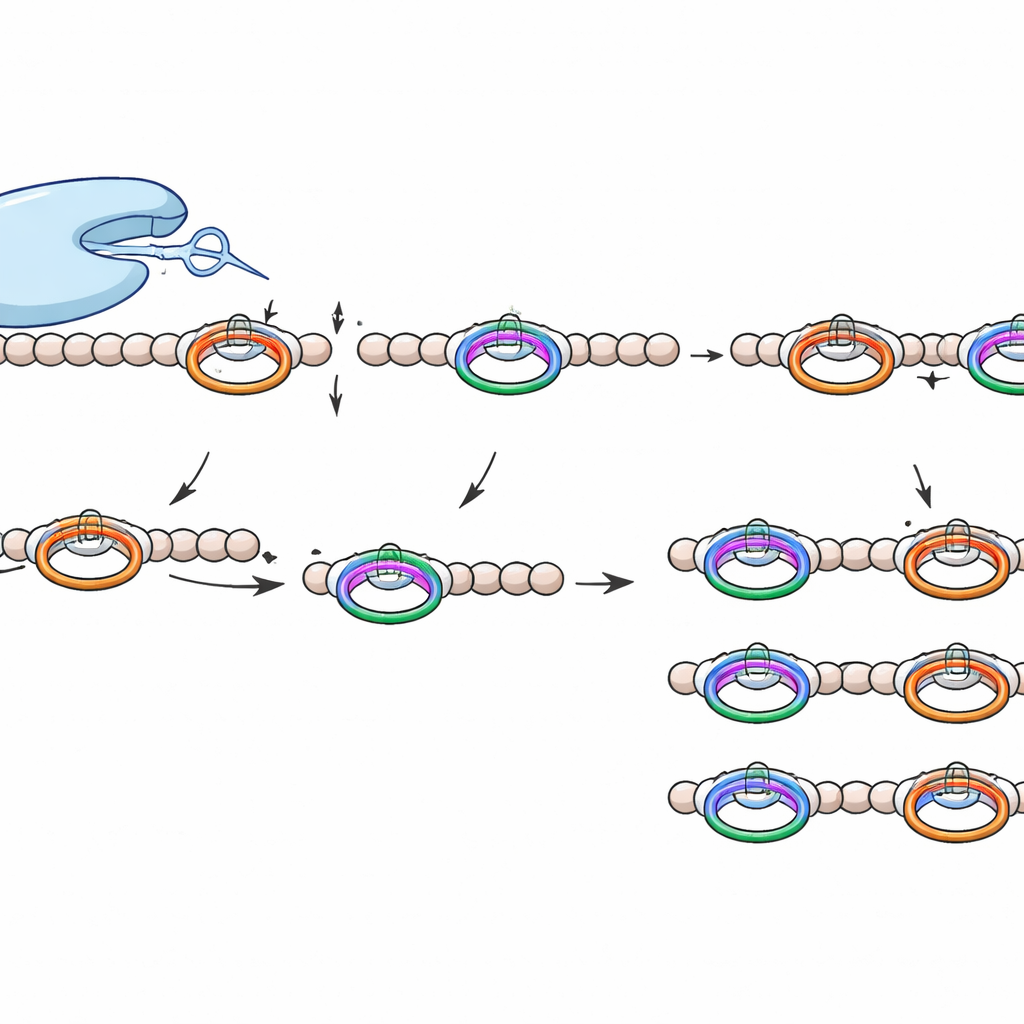
O que torna essa ferramenta de corte especial
A WprP2 pertence à ampla família S9 de proteases, que já inclui enzimas de relevância médica, mas destaca‑se em vários aspectos. Ela cliva no lado N‑terminal de uma prolina em vez de depois dela, atua sobre um motivo repetido para gerar fragmentos de tamanho uniforme ao longo de toda a cadeia precursora e mostra ampla tolerância aos aminoácidos que se situam entre seus dois sítios de reconhecimento. Essa combinação de precisão e flexibilidade não havia sido observada antes em proteases relacionadas a RiPPs.
Como essa descoberta pode ser usada
Ao revelar uma protease que reconhece sinais de sequência simples e realiza cortes repetidos e uniformes, este trabalho adiciona uma ferramenta poderosa ao crescente conjunto de recursos para engenharia de peptídeos. Em termos práticos, a WprP2 poderia ser aproveitada para liberar ou remodelar peptídeos projetados, incluindo aqueles com entrecruzamentos complexos que resistem a enzimas padrão como a tripsina. Para não especialistas, a conclusão-chave é que os cientistas descobriram um novo tipo de tesoura molecular que corta longas cadeias peptídicas em pedaços precisos e de tamanho uniforme, abrindo a porta para uma produção mais controlada de potenciais antibióticos e outras moléculas bioativas.
Citação: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
Palavras-chave: peptídeos RiPP, protease de serina, WprP2, produtos naturais ciclofanos, engenharia de peptídeos