Clear Sky Science · pt
Sonda de emissão induzida por confinamento estérico para monitorar conformações de proteínas em células vivas
Observando proteínas que mudam de forma em tempo real
Dentro de cada célula viva, as proteínas estão constantemente mudando de forma enquanto transmitem sinais, percebem o ambiente e executam funções vitais. Muitas doenças surgem quando essas mudanças conformacionais falham, mas tem sido notoriamente difícil observar esses movimentos diretamente em células vivas, especialmente ao longo de escalas de tempo muito rápidas e muito lentas. Este artigo apresenta uma nova sonda emissora de luz, chamada BIOSCE, que transforma movimentos microscópicos de proteínas em flashes visíveis, permitindo que pesquisadores rastreiem proteínas individuais enquanto elas dobram, torcem e interagem em tempo real dentro de células vivas. 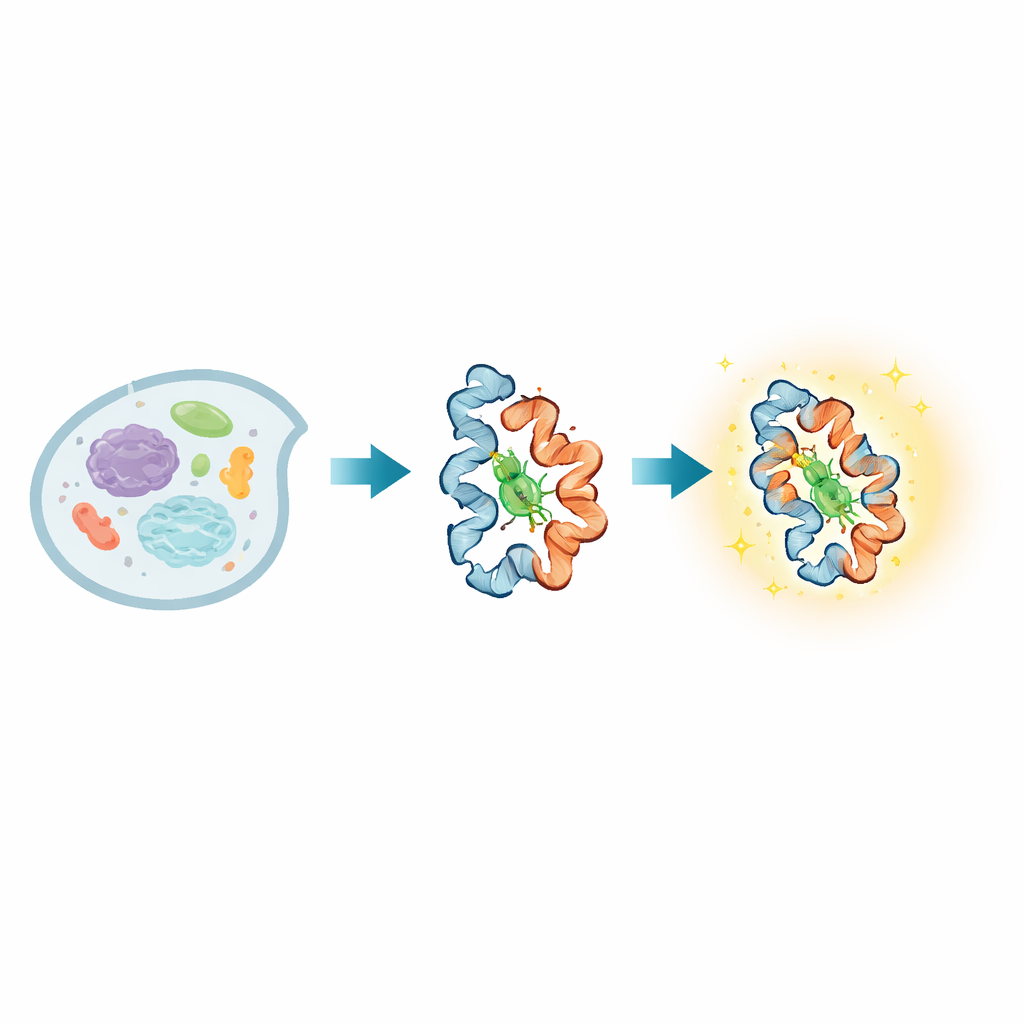
Um novo interruptor de luz para proteínas em movimento
No centro do BIOSCE está uma pequena molécula corante, MTPABP-Cl, que se torna mais brilhante quando é comprimida. Os pesquisadores ligam esse corante a uma etiqueta proteica amplamente usada chamada HaloTag, que pode ser fundida geneticamente a quase qualquer proteína de interesse. Quando a proteína etiquetada muda sua conformação ou se compacta com vizinhos, isso altera quanto “espaço” o corante tem para se mover. Em um ambiente frouxo, as partes internas do corante podem girar livremente e a maior parte da energia absorvida é dissipada em movimento; em um bolso mais apertado esses movimentos são bloqueados, e o corante libera mais dessa energia como luz. Essa “emissão induzida por confinamento estérico” transforma mudanças sutis no adensamento local ao redor de uma única proteína em uma variação contínua de brilho, em vez de um sinal simplesmente ligado/desligado, tornando a sonda altamente sensível a pequenas alterações conformacionais.
Construindo e testando o corante sensível à compressão
A equipe primeiro desenhou e sintetizou o MTPABP-Cl de modo que ele fosse pouco brilhante em solução, mas se iluminasse quando mantido no lugar pelo HaloTag ou por uma proteína de fusão mais compacta. Medições cuidadosas mostraram que o corante absorve luz azul e emite no vermelho distante, o que é favorável para imagem em profundidade dentro de células e para observação de longa duração. Quando ligado apenas ao HaloTag, sua emissão aumentou; quando o HaloTag foi fundido a uma proteína parceira que se dobrava ao redor do corante, o brilho aumentou ainda mais. Simulações por computador confirmaram que, em arranjos proteicos mais compactos, o corante experimenta maior aglomeração, uma superfície exposta menor e mais contatos estabilizantes, todos os quais restringem o movimento e aumentam a emissão. O corante também se liga rápida e especificamente ao HaloTag, apresenta ruído de fundo muito baixo em células que não possuem a etiqueta e permanece não tóxico nas concentrações de trabalho, apoiando seu uso em experimentos com células vivas. 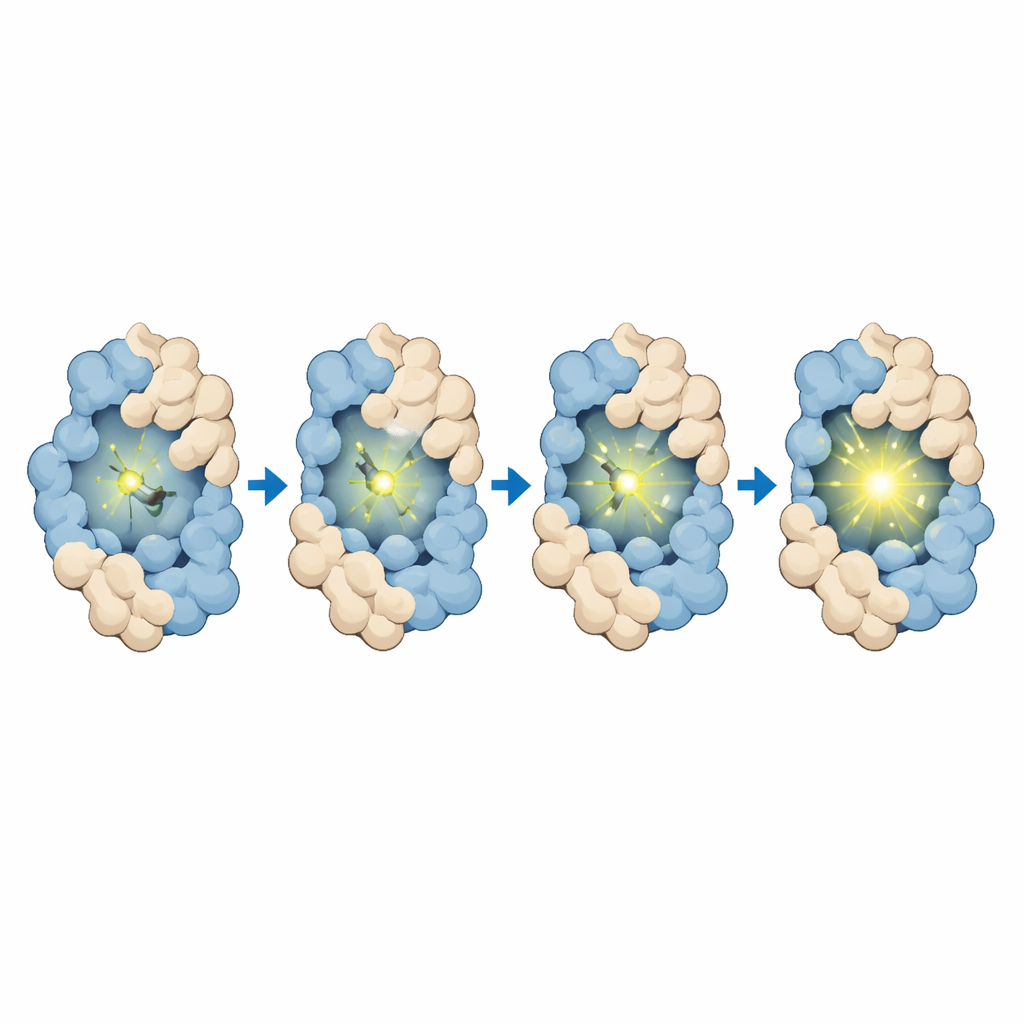
Acompanhando sinais rápidos e encontros entre proteínas
Para demonstrar o que o BIOSCE pode fazer, os autores o aplicaram a vários processos celulares bem conhecidos. Primeiro, adaptaram um sensor de cálcio baseado na calmodulina, uma proteína que muda de forma quando se liga a íons de cálcio, mensageiros centrais na atividade neuronal e em muitos outros eventos celulares. Ao fundir a calmodulina ao HaloTag e rotulá-la com MTPABP-Cl, criaram um indicador quimigenético chamado SCECaMP. Em células humanas e em células semelhantes a neurônios, esse indicador clareou e escureceu em sincronia com picos de cálcio induzidos por estimulação com potássio, com velocidades de resposta comparáveis às proteínas fluorescentes GCaMP amplamente usadas. Como o sinal do BIOSCE depende diretamente do adensamento local ao redor do corante, ele pode refletir fielmente as mudanças estruturais da calmodulina ao mesmo tempo em que fornece fluorescência estável e duradoura adequada para imageamento prolongado.
Vendo interações induzidas por fármacos e danos por toxinas
Os pesquisadores então investigaram se o BIOSCE poderia rastrear quando duas proteínas são aproximadas por um fármaco. Eles usaram um sistema clássico em que a rapamicina aproxima duas parceiras, FKBP e FRB, em uma via chave de controle de crescimento. Ao ligar HaloTag a FKBP ou FRB e rotular com MTPABP-Cl, observaram aumentos rápidos de fluorescência em escala de milissegundos quando a rapamicina induziu essas proteínas a se aproximarem e se rearranjarem. O aumento do brilho refletiu um microambiente mais apertado em torno do corante à medida que as parceiras ficavam em proximidade. Em um teste mais complexo, estudaram SNAP25, uma proteína terminal nervosa crucial para a liberação de neurotransmissores e alvo principal da neurotoxina botulínica A. Ao posicionar HaloTag em cada lado do sítio de clivagem da toxina e rotular com o corante, foi possível acompanhar separadamente os movimentos dos fragmentos N-terminal e C-terminal após a clivagem. O rastreamento de partículas únicas revelou que um fragmento permaneceu ancorado próximo à membrana celular, enquanto o outro difundiu-se mais livremente pelo citoplasma, e que o padrão exato dependia de o rótulo ter sido aplicado antes ou depois da exposição à toxina. A sonda até reportou ajustes conformacionais rápidos induzidos por zinco em SNAP25 durante esse processo.
O que isso significa para a biologia e a medicina
Em conjunto, esses resultados mostram que o BIOSCE é uma nova e versátil maneira de visualizar como proteínas individuais se movem, dobram e interagem dentro de células vivas ao longo de uma ampla gama de escalas temporais. Como o método depende de uma fusão geral com HaloTag e de uma única pequena molécula corante, ele pode, em princípio, ser aplicado a muitas proteínas diferentes sem a necessidade de redesenhar todo sensor a cada vez. A mudança contínua de brilho dependente do confinamento permite aos pesquisadores detectar deslocamentos estruturais sutis em vez de apenas eventos binários grandes. Olhando para frente, os autores planejam melhorar a entrega da sonda e a profundidade de imageamento para que o BIOSCE possa ser usado em tecidos e em animais inteiros. Se bem-sucedida, essa abordagem poderia se tornar uma ferramenta poderosa para relacionar onde as proteínas estão, como se movem e o que fazem em saúde e doença, e pode, em última instância, alimentar modelos computacionais detalhados do comportamento celular.
Citação: Jia, H., Yang, L., Yang, Y. et al. Steric confinement-induced emission probe for monitoring protein conformations in live cells. Commun Chem 9, 109 (2026). https://doi.org/10.1038/s42004-026-01914-x
Palavras-chave: dynamics conformacional de proteínas, imagem em células vivas, biossensores fluorescentes, sondas HaloTag, neurotoxina botulínica