Clear Sky Science · pt
Consumo de amostra minimizado para cristalografia serial resolvida no tempo aplicada ao ciclo redox da NQO1 humana
Observando enzimas em ação com menos amostras preciosas
A biologia moderna frequentemente depende de lasers poderosos de raios X para ver como as moléculas da vida se movem e mudam de forma, mas esses experimentos normalmente consomem grandes quantidades de proteína preparadas com esforço. Este estudo apresenta uma nova maneira de “alimentar” cristais proteicos microscópicos em um laser de elétrons livres de raios X de forma muito mais eficiente, reduzindo o material necessário em até 97%. Também demonstra que esse método mais econômico ainda consegue capturar os primeiros passos da atividade de uma enzima humana relevante para a medicina, abrindo caminho para filmes de rotina de proteínas em ação. 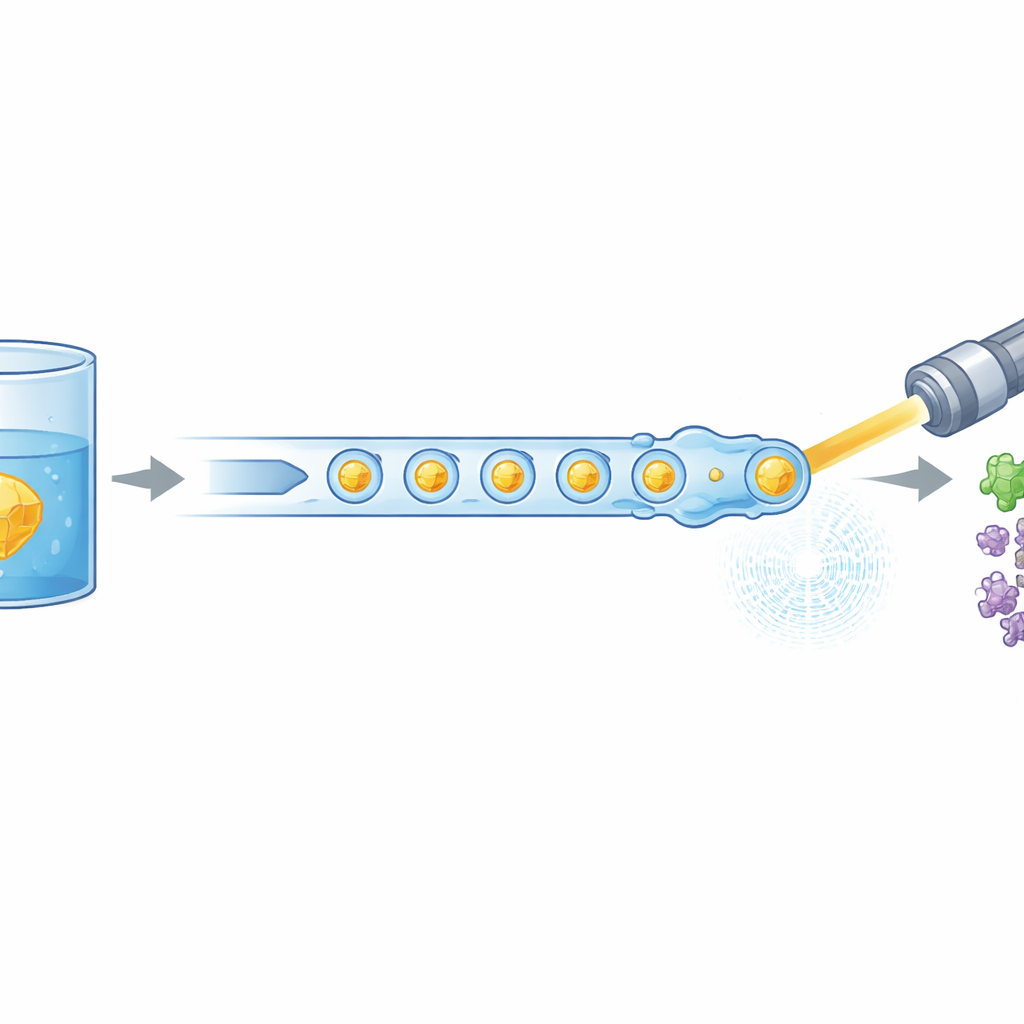
Por que fazer filmes moleculares sai caro
Para entender como as proteínas realmente realizam suas funções, os cientistas cada vez mais deixam de lado imagens estáticas e recorrem a “filmes” em lapso temporal que acompanham reações em tempo real. Uma abordagem de ponta, a cristalografia serial resolvida no tempo, pulveriza milhões de cristais microscópicos de uma proteína através de um feixe ultrabrilhante de raios X. Cada cristal é atingido apenas uma vez, fornecendo uma visão sem danos da estrutura, e milhares dessas imagens são combinadas para formar o quadro completo. O problema é que cada momento ao longo de uma reação — décimos de segundo, um segundo completo, e assim por diante — exige um novo lote de cristais. Como a preparação de proteínas pode ser lenta e cara, o consumo de amostra tornou-se um gargalo importante, especialmente em instalações de ponta como o European XFEL, onde os pulsos de raios X chegam em trens rápidos a taxas de megahertz.
Uma nova forma de entregar minúsculas gotículas no tempo certo
Os pesquisadores enfrentaram esse problema redesenhando como os cristais são entregues ao feixe de raios X. Em vez de um fluxo contínuo de líquido, eles geram um trem cuidadosamente espaçado de gotículas microscópicas, cada uma contendo cristais proteicos, separadas por uma fase de óleo. Um dispositivo em miniatura impresso em 3D combina dois fluxos — cristais de proteína e um parceiro de reação dissolvido — em pequenos volumes misturados, que são então destacadas em gotículas. Essas gotículas são conduzidas por um bico focalizado por gás que forma um jato estreito compatível com o vácuo e a velocidade do XFEL. Crucialmente, a produção de gotículas é sincronizada eletricamente com o tempo dos trens de pulsos de raios X, de modo que quase todo pulso útil atinge uma gotícula, em vez de líquido vazio. 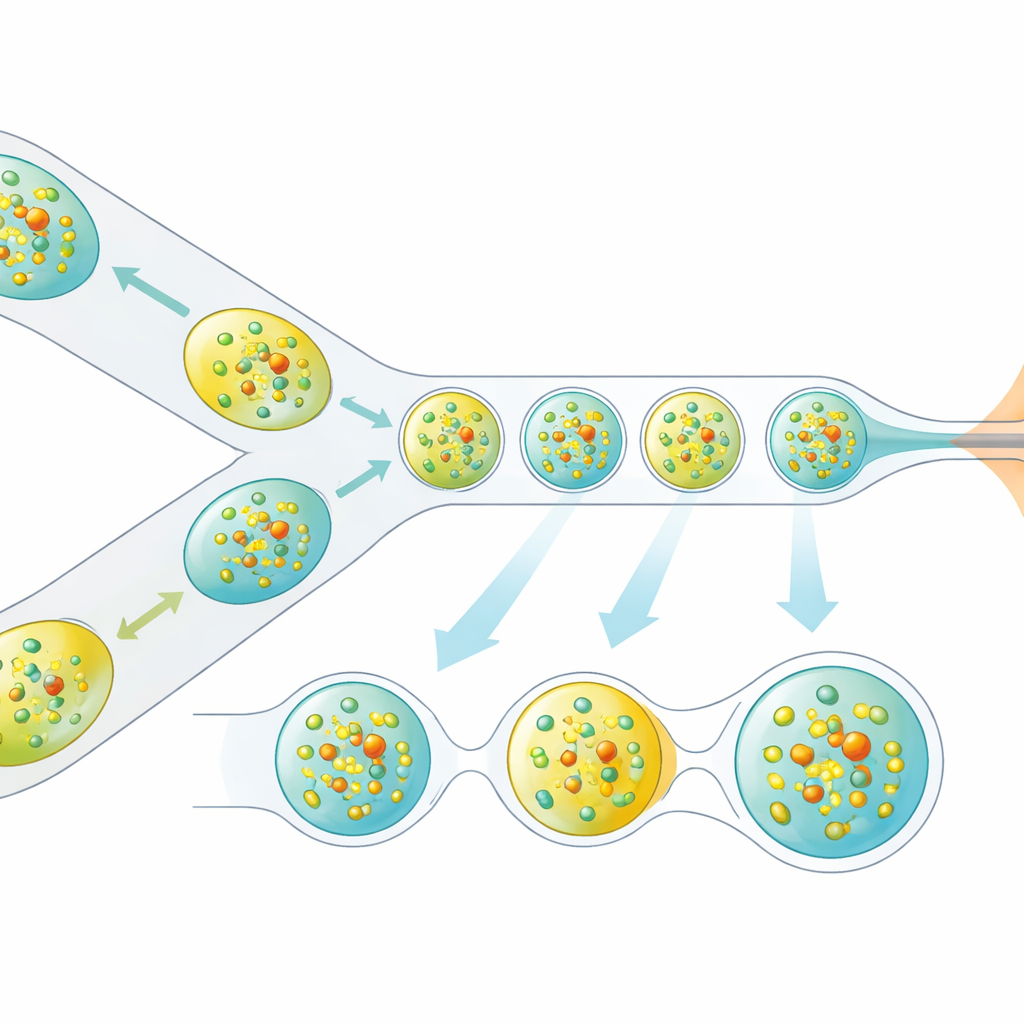
Testando o método com uma enzima humana
Para provar que essa abordagem baseada em gotículas funciona para questões biológicas reais, a equipe estudou a NAD(P)H:quinona oxidorredutase 1 (NQO1), uma enzima humana envolvida no equilíbrio redox celular e associada a doenças. Eles misturaram microcristais de NQO1 com seu cofator natural, NADH, e sondaram o sistema em dois pontos temporais iniciais: 0,3 segundos e 1,2 segundos após a mistura. Ao examinar os padrões de difração de raios X resultantes, reconstruíram estruturas tridimensionais da enzima para cada atraso. Apesar de usar dramaticamente menos proteína do que experimentos convencionais com fluxo contínuo, a qualidade dos dados foi suficiente para revelar sutis características de densidade eletrônica nos sítios ativos da enzima, consistentes com moléculas de NADH começando a se ligar em baixa ocupação.
O que as primeiras imagens estruturais revelam
As estruturas mostram que logo após a mistura nem todos os sítios ativos no cristal se comportam da mesma forma. Aos 0,3 segundos, sinais de NADH aparecem claramente em três dos quatro sítios ativos na cela unitária, e frequentemente em mais de uma conformação, sugerindo que o cofator explora várias posições antes de se acomodar. Aos 1,2 segundos, algumas dessas características se afinam em um modo de ligação dominante, mas o quadro geral permanece o de uma interação flexível e apenas parcialmente ocupada. Esse comportamento desigual e mutável está alinhado com evidências bioquímicas anteriores de que as duas unidades parceiras de um dímero de NQO1 não atuam em perfeita sincronia, mas apresentam atividade de “metade dos sítios”, onde um lado do par se envolve primeiro enquanto o outro fica para trás. Os dados resolvidos no tempo oferecem, assim, um vislumbre estrutural inicial de como essa assimetria se manifesta no espaço real.
Economizando amostra sem perder a ciência
Do ponto de vista prático, o método segmentado por gotículas reduziu o uso de proteína em cerca de seis vezes para as medições de 0,3 segundos e em até 97% para os experimentos de 1,2 segundos, em comparação com jatos contínuos tradicionais em condições semelhantes. Ainda assim, forneceu informações estruturais confiáveis em temperatura ambiente, compatíveis com a exigente estrutura de pulsos do European XFEL. Para não especialistas, a conclusão é que os pesquisadores agora podem observar enzimas como a NQO1 começarem seu trabalho em quase tempo real, usando apenas miligramas de amostra preciosa por ponto temporal. Isso torna muito mais viável investigar muitos tempos de reação e muitas proteínas diferentes, ajudando em última instância a revelar como enzimas de importância médica se movem, flexionam e cooperam enquanto realizam a química da vida.
Citação: Doppler, D., Grieco, A., Koh, D. et al. Minimized sample consumption for time-resolved serial crystallography applied to the redox cycle of human NQO1. Commun Chem 9, 107 (2026). https://doi.org/10.1038/s42004-026-01908-9
Palavras-chave: cristalografia serial, laser de elétrons livres de raios X, microfluídica de gotículas, dinâmica enzimática, NQO1