Clear Sky Science · pt
Variantes oncogênicas de PI3Kα revelam um espectro conformacional graduado com bolsos crípticos específicos de mutação
Quando Uma Mudança no DNA Não Basta
O câncer muitas vezes é descrito como uma doença de mutações, mas este estudo mostra que nem todas as mutações atuam sozinhas. Os pesquisadores examinaram uma enzima-chave de controle do crescimento, a PI3Kα, e descobriram que quando duas alterações específicas no DNA ocorrem juntas na mesma cópia do gene, elas podem empurrar essa proteína para conformações mais ativas do que qualquer uma das alterações isoladas. Isso importa porque a PI3Kα hiperativa não só impulsiona cânceres, como também está envolvida em síndromes de crescimento benigno e em distúrbios do desenvolvimento cerebral — e ajuda a explicar por que alguns tumores respondem mal aos medicamentos atuais.
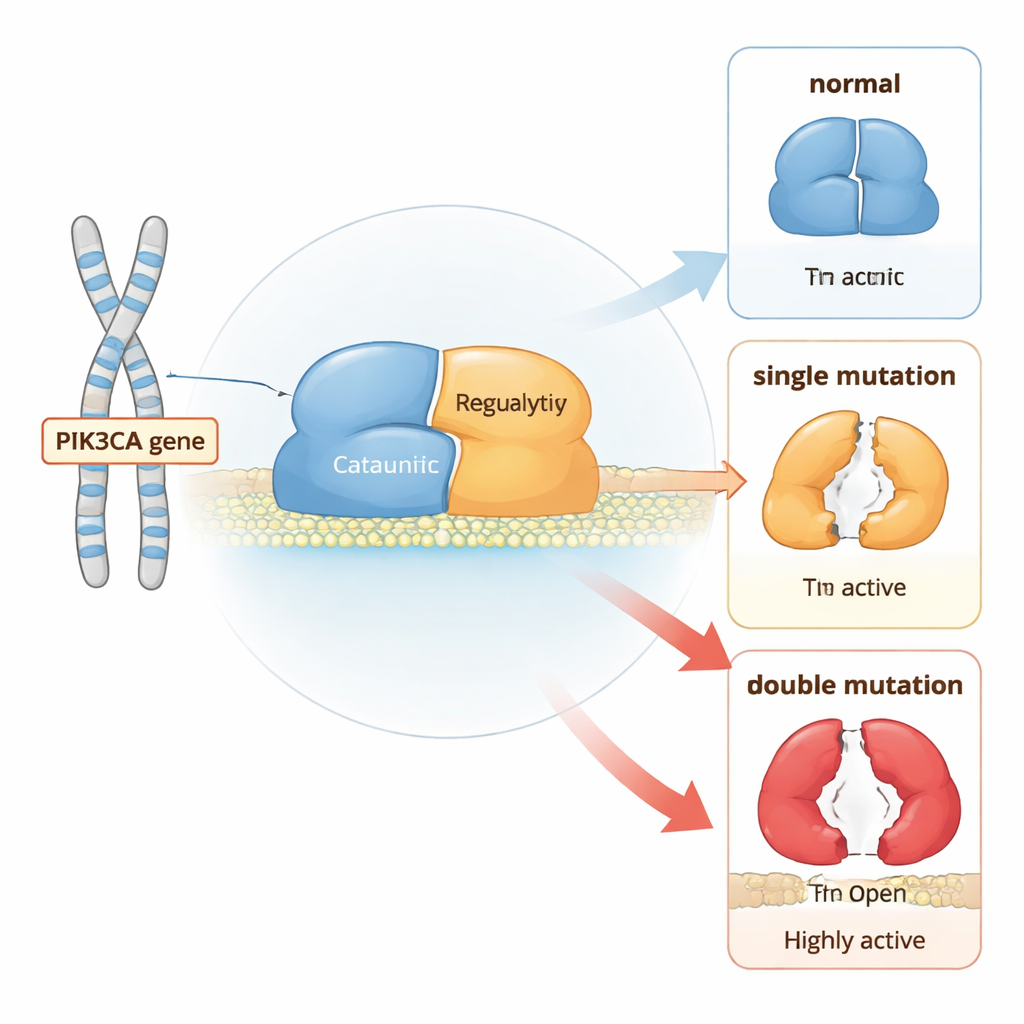
Um Interruptor Molecular para o Crescimento Celular
A PI3Kα é uma proteína composta por duas partes que se posiciona próxima à membrana celular e retransmite sinais de crescimento. Em condições normais, ela permanece majoritariamente na posição “desligada” até que receptores na superfície celular sejam estimulados. Então, a PI3Kα se move para a membrana e converte um lipídio chamado PIP2 em PIP3, que sinaliza à célula para crescer e se dividir. Para evitar crescimento descontrolado, várias partes da proteína atuam como freios internos: uma região prende o núcleo catalítico, outra mantém um laço de ativação flexível próximo, e uma subunidade parceira ajuda a manter todo o complexo sob controle.
Como Mutações Simples e Duplas Deslocam o Equilíbrio
Usando longas simulações computacionais ao nível atômico, os autores compararam a PI3Kα normal com versões que carregavam seja mutações simples “hotspot” encontradas em câncer, seja combinações de um hotspot com uma mutação mais fraca na mesma molécula. Eles descobriram que cada mutação altera com que frequência a proteína visita conformações mais abertas e ativas, mas mutações duplas deslocam o equilíbrio muito mais do que as simples. Em particular, alguns pares de mutações cooperam para afrouxar os contatos que mantêm uma peça regulatória (chamada nSH2) no lugar e para deslocar outro segmento (iSH2) para longe de seu sítio de acoplagem. Esse movimento coordenado destrava o núcleo catalítico, facilitando que a proteína se mova para a membrana e comece a sinalizar.
Facilitando que o Substrato Alcance o Local da Reação
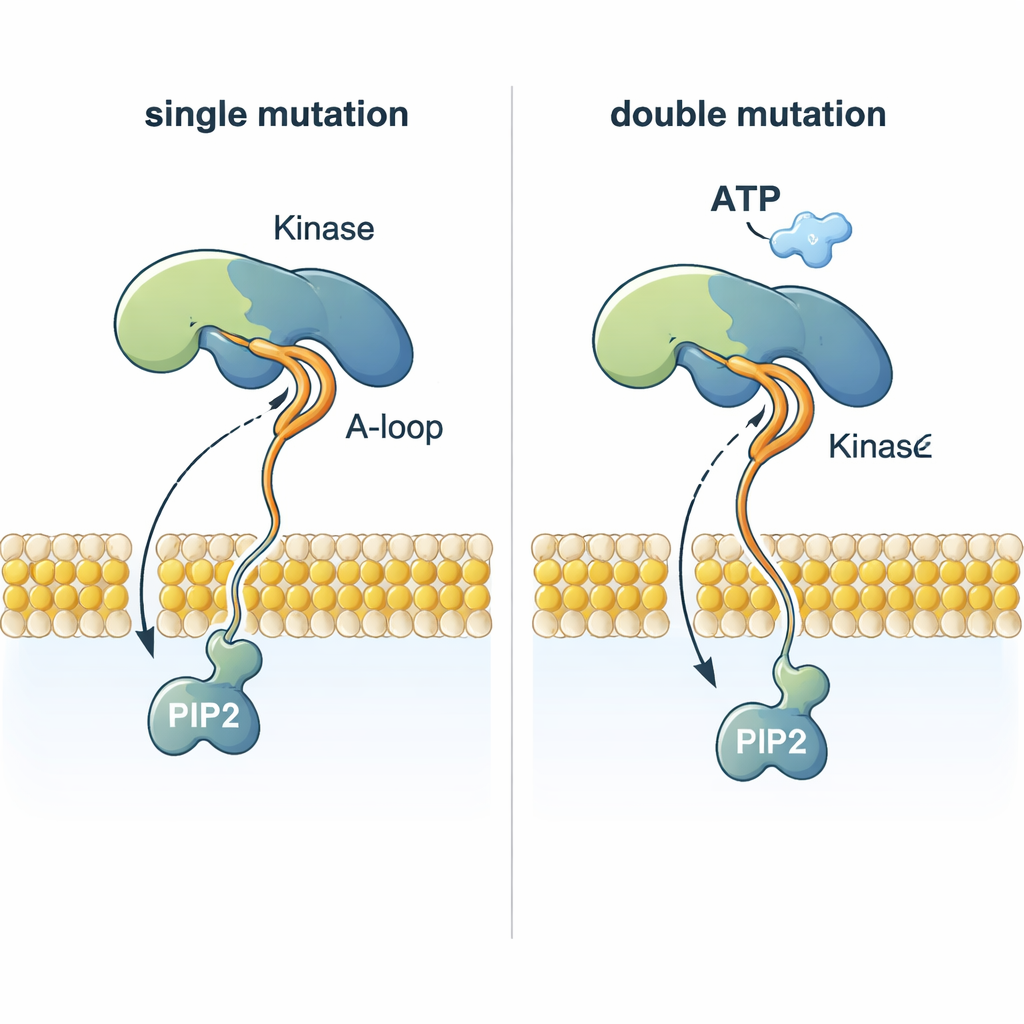
Um enigma marcante é como a PI3Kα pode transferir um grupo fosfato do ATP — que fica quase 2 nanômetros acima da membrana — para o PIP2, que está embutido na membrana. As simulações mostram que certas mutações remodelam um laço de ativação flexível de modo que um trecho altamente carregado positivamente se projeta em direção à membrana. Esse laço pode agarrar a cabeça negativamente carregada do PIP2, puxá-la para fora da bicamada lipídica e guiá-la em direção ao ATP. Mutações duplas que combinam uma alteração que ancora na membrana com outra que muda esse laço coordenam o PIP2 muito mais eficientemente do que a PI3Kα normal ou mutantes simples, oferecendo uma explicação estrutural de por que tumores com duas mutações em PI3Kα podem ser especialmente agressivos.
Sítios Ocultos para Drogas Revelados pelo Movimento
Porque a PI3Kα é grande e flexível, um único medicamento direcionado ao seu sítio ativo frequentemente tem dificuldade para funcionar em todas as formas mutantes e pode causar efeitos colaterais, como alterações severas na glicemia. Ao rastrear como a proteína “respira” e se flexiona ao longo do tempo, os pesquisadores descobriram bolsos “crípticos” — fendas temporárias que se abrem apenas em certas conformações mutantes e são invisíveis em estruturas cristalográficas estáticas. Esses bolsos aparecem em locais específicos às mutações, por exemplo próximos a regiões que se movem mais intensamente em determinados mutantes duplos. Isso sugere que drogas alostéricas cuidadosamente desenhadas, que se ligam longe do sítio ativo, poderiam ser adaptadas para travar variantes mutantes individuais de volta em conformações mais seguras e menos ativas.
Rumo a Tratamentos Combinados Mais Inteligentes
No conjunto, o trabalho sustenta uma visão de “um-dois” na genética do câncer: uma mutação forte em hotspot mais uma parceira mais fraca na mesma molécula de PI3Kα podem criar um espectro graduado de conformações mais ativas, frequentemente associadas a desfechos clínicos mais graves. Para a terapia, os autores argumentam que, em vez de depender de um único inibidor, pode ser mais eficaz combinar drogas que visem bolsos diferentes — uma no sítio ativo e uma ou mais em sítios alostéricos que existem apenas em mutantes específicos. Tales coquetéis poderiam, em princípio, reduzir com maior precisão a atividade da PI3Kα, diminuir efeitos tóxicos e melhor ajustar o tratamento ao padrão exato de mutações encontrado no tumor de cada paciente.
Citação: Jang, H., Yavuz, B.R., Zhang, M. et al. Oncogenic PI3Kα variants reveal graded conformational spectrum with mutation-specific cryptic pockets. Commun Chem 9, 100 (2026). https://doi.org/10.1038/s42004-026-01906-x
Palavras-chave: PI3K alfa, mutações oncogênicas, inibidores alostéricos, dinâmica molecular, transdução de sinal